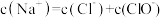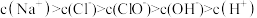常温下,向一定浓度邻苯二甲酸钠( 表示)溶液中通入
表示)溶液中通入 气体,保持溶液体积和温度不变,测得
气体,保持溶液体积和温度不变,测得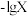 与
与 [X为
[X为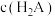 、
、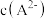 、
、 ;
;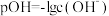 ]的变化关系如图所示,下列说法错误的是
]的变化关系如图所示,下列说法错误的是
 表示)溶液中通入
表示)溶液中通入 气体,保持溶液体积和温度不变,测得
气体,保持溶液体积和温度不变,测得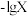 与
与 [X为
[X为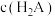 、
、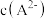 、
、 ;
;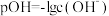 ]的变化关系如图所示,下列说法错误的是
]的变化关系如图所示,下列说法错误的是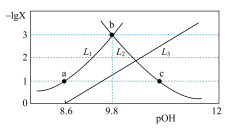
A.曲线 表示— 表示—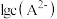 |
B.c点溶液中: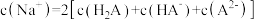 |
C.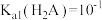 |
D.水的电离程度: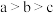 |
更新时间:2024-02-17 21:12:55
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】为了探究温度对水解平衡的影响,用手持技术测定一定浓度 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是
 溶液的pH随温度变化的关系如图所示,下列说法不正确的是
溶液的pH随温度变化的关系如图所示,下列说法不正确的是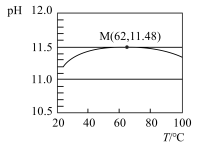
| A.该实验能证明升温促进水解 | B.点M之后 水解放热 水解放热 |
C.点M处溶液中 略大于 略大于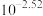 mol/L mol/L | D.点M后pH下降是因为升温对 的影响更大 的影响更大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】电位滴定法是通过测量滴定过程中电位变化来确定滴定终点的方法。已知:某二元酸H2A电离常数Ka1=1.0×10-2、Ka2=1.0×10-8。常温下,采用电位滴定法,用盐酸滴定Na2A溶液,滴定过程中,溶液电位U、pH随盐酸体积V的变化曲线如图所示。下列说法中正确的是
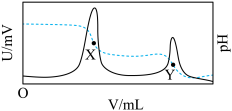

| A.X点溶液显酸性 |
| B.X、Y点水的电离程度相同 |
| C.Y点溶液中: c(A2- )+c(HA- )+c(OH- )=c(H+) |
| D.X、Y点溶液中均存在: c(HA- )·c(OH- )>c(A2-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】已知:pKa=-lgKa。25℃时,H2A的pKa1=1.85,pKa2=7.19。常温下,用0.1 mol·L-1 NaOH溶液滴定20mL0.1mol·L-1H2A溶液的滴定曲线如图所示。下列说法不正确的是
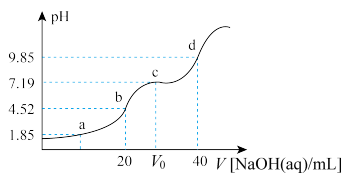

| A.a点溶液中:c(HA-)=c(H2A) |
| B.b点溶液中:A2-水解平衡常数Kh1=10-6.81 |
| C.c点溶液中:V0=30 |
| D.a、b、c、d四点中,d点溶液中水的电离程度最大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】25℃时,在c(Na2CO3)+c(NaHCO3)=0.100mol·L-1的混合溶液中,c(HCO3-)、c(CO32-)与pH的关系如下图所示。下列说法正确的是


| A.pH=10的溶液中:c(HCO3-)<c(CO32-) |
| B.E点溶液中:c(Na+)=3c(CO32-) |
| C.pH=11的溶液中:c(H+)+c(Na+)+c(H2CO3)=c(OH-)+c(CO32-)+0.100mol·L-1 |
| D.在E点溶液中加入等体积0.100mol·L-1的NaOH溶液,c(CO32-)与c(HCO3-)之和保持不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】已知MR为易溶的弱酸弱碱盐,常温下,调节0.1 的MR溶液的pH(忽略温度和溶液体积变化),溶液pH与
的MR溶液的pH(忽略温度和溶液体积变化),溶液pH与 变化情况如图所示。
变化情况如图所示。
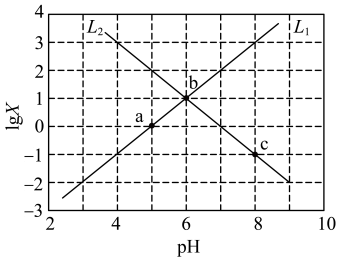
下列说法正确的是
A. 表示 表示 |
B. 的水解平衡常数 的水解平衡常数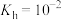 |
C.b点溶液中: |
D.两条直线上任意点均满足: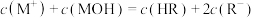 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】下列各溶液中,微粒的物质的量浓度关系正确的是
| A.等浓度的HAc和NaAc混合溶液中:c(H+)-c(OH-)=1/2[c(Ac-)-c(HAc)] |
| B.0.1mol·L-1NH4Cl和0.1mol·L-1HCl溶液等体积混合:c(NH4+)+c(NH3.H2O)=0.1mol·L-1 |
| C.向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
| D.等物质的量浓度的①NH4Cl溶液②(NH4)2SO4溶液 ③NH4HSO4溶液 ④(NH4)2CO3溶液⑤NH4HCO3中NH4+浓度的大小关系是②>④>①>③>⑤ |
您最近一年使用:0次

 溶液(不考虑空气的影响)中缓慢通入0.05 mol
溶液(不考虑空气的影响)中缓慢通入0.05 mol ,充分混合,完全,整个过程中无气体逸出,忽略溶液中体积和温度的变化,测得溶液的pH与通入
,充分混合,完全,整个过程中无气体逸出,忽略溶液中体积和温度的变化,测得溶液的pH与通入 ,
, 。下列说法错误的是
。下列说法错误的是
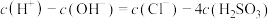
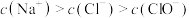
 )的叙述正确的是
)的叙述正确的是
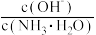 将增大
将增大

 的负对数与NaOH溶液体积之间的关系如图所示,下列说法正确的
的负对数与NaOH溶液体积之间的关系如图所示,下列说法正确的