含硫化合物是实验室和工业上的常用化学品。
回答下列问题:
(1)实验室可用铜与浓硫酸反应制备少量 :
:
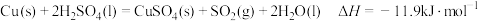 ,判断该反应的自发性,并说明理由
,判断该反应的自发性,并说明理由___________ 。
(2)在一个固定容积为 的密闭容器中,充入
的密闭容器中,充入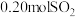 和
和 ,半分钟后达到平衡,测得容器中含
,半分钟后达到平衡,测得容器中含 ,则
,则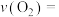
___________  。若继续通入
。若继续通入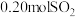 和
和 ,则平衡
,则平衡___________ 移动(填“向正反应方向”、“向逆反应方向”或“不”),再次达到平衡时,___________ 
___________  。
。
(3)接触法制硫酸工艺中,其主反应在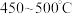 并有催化剂存在条件下进行:
并有催化剂存在条件下进行:

①该热化学反应方程式的含义是___________ 。
②为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如图所示。下列说法正确的是___________ (填标号)。
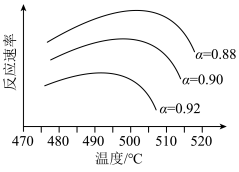
a.温度越高,反应速率越大
b.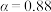 的曲线代表平衡转化率
的曲线代表平衡转化率
c. 越大,反应速率最大值对应温度越低
越大,反应速率最大值对应温度越低
d.可根据不同 对应的最大反应速率,选择最佳生产温度
对应的最大反应速率,选择最佳生产温度
③设 的平衡分压为
的平衡分压为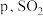 的平衡转化率为
的平衡转化率为 ,用含
,用含 和
和 的代数式表示上述催化氧化反应的
的代数式表示上述催化氧化反应的
___________ (用平衡分压代替平衡浓度)。
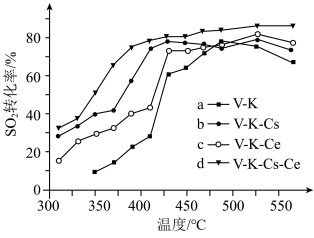
④为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如下图所示,催化性能最佳的是___________ (填标号)。
回答下列问题:
(1)实验室可用铜与浓硫酸反应制备少量
 :
: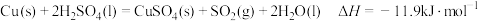 ,判断该反应的自发性,并说明理由
,判断该反应的自发性,并说明理由(2)在一个固定容积为
 的密闭容器中,充入
的密闭容器中,充入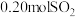 和
和 ,半分钟后达到平衡,测得容器中含
,半分钟后达到平衡,测得容器中含 ,则
,则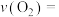
 。若继续通入
。若继续通入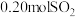 和
和 ,则平衡
,则平衡
 。
。(3)接触法制硫酸工艺中,其主反应在
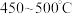 并有催化剂存在条件下进行:
并有催化剂存在条件下进行:
①该热化学反应方程式的含义是
②为寻求固定投料比下不同反应阶段的最佳生产温度,绘制相应转化率(α)下反应速率(数值已略去)与温度的关系如图所示。下列说法正确的是

a.温度越高,反应速率越大
b.
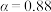 的曲线代表平衡转化率
的曲线代表平衡转化率c.
 越大,反应速率最大值对应温度越低
越大,反应速率最大值对应温度越低d.可根据不同
 对应的最大反应速率,选择最佳生产温度
对应的最大反应速率,选择最佳生产温度③设
 的平衡分压为
的平衡分压为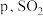 的平衡转化率为
的平衡转化率为 ,用含
,用含 和
和 的代数式表示上述催化氧化反应的
的代数式表示上述催化氧化反应的
④为提高钒催化剂的综合性能,我国科学家对其进行了改良。不同催化剂下,温度和转化率关系如下图所示,催化性能最佳的是

更新时间:2024-04-26 09:41:34
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】I.在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强 ②混合气体的密度③混合气体的总物质的量 ④混合气体的平均相对分子质量 ⑤混合气体的颜色。
(1)一定能证明2SO2(g)+O2(g) 2SO3(g)达到平衡状态的是
2SO3(g)达到平衡状态的是______ (填序号,下同)。
(2)一定能证明 A(s)+2B(g) C(g)+D(g)达到平衡状态的是
C(g)+D(g)达到平衡状态的是_______ 。(注:B、C、D均为无色物质)
II.某温度时,在一个1L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
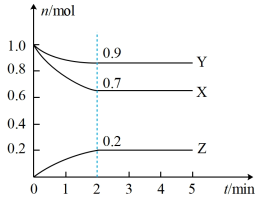
(1)反应开始至2min,以气体Y表示的平均反应速率为________ ;
(2)该反应的化学方程式为___________ ;
(3)X的转化率___________ ,生成的Z的百分含量___________
(4)amolX与bmolY的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=___________ 。
(1)一定能证明2SO2(g)+O2(g)
 2SO3(g)达到平衡状态的是
2SO3(g)达到平衡状态的是(2)一定能证明 A(s)+2B(g)
 C(g)+D(g)达到平衡状态的是
C(g)+D(g)达到平衡状态的是II.某温度时,在一个1L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:

(1)反应开始至2min,以气体Y表示的平均反应速率为
(2)该反应的化学方程式为
(3)X的转化率
(4)amolX与bmolY的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中a:b=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】(1)已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
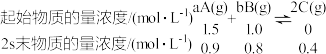
请回答下列问题。
①该可逆反应的化学方程式可表示为___ 。
②用物质B来表示0~2s的平均反应速率为___ 。
③从反应开始到2s末,A的转化率为___ 。
④下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是__ (填序号)。
A.vB(消耗)=vC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.容器内气体C的物质的量分数保持不变
(2)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是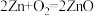 。则该电池的负极材料是
。则该电池的负极材料是__ 。
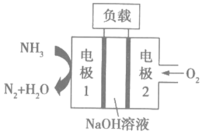
②瑞典ASES公司设计的曾用于驱动潜艇的液氨—液氧燃料电池的示意图如图所示,该燃料电池工作时,电池的总反应方程式为__ ;负极的电极反应式为___ 。
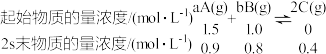
请回答下列问题。
①该可逆反应的化学方程式可表示为
②用物质B来表示0~2s的平均反应速率为
③从反应开始到2s末,A的转化率为
④下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
A.vB(消耗)=vC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.容器内气体C的物质的量分数保持不变
(2)①锌电池有望代替铅蓄电池,它的构成材料是锌、空气、某种电解质溶液,发生的总反应方程式是
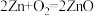 。则该电池的负极材料是
。则该电池的负极材料是②瑞典ASES公司设计的曾用于驱动潜艇的液氨—液氧燃料电池的示意图如图所示,该燃料电池工作时,电池的总反应方程式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器内,进行反应:CO(g)+H2O(g) CO2(g)+H2(g)。
CO2(g)+H2(g)。
得到如下两组数据:
①实验1中以v(CO2)表示的反应速率为___ 。
②该反应的逆反应为___ (填“吸”或“放”)热反应。
(2)在一容积为2L的密闭容器内加入2mol的CO和6mol的H2,在一定条件下发生如下反应:CO(g)+2H2(g) CH3OH(g) △H<0该反应的逆反应速率与时间的关系如图所示:
CH3OH(g) △H<0该反应的逆反应速率与时间的关系如图所示:
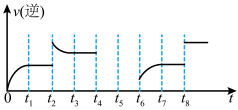
①由图可知反应在t1、t3、t7时都达到平衡,而在t2、t8时都改变了条件,试从以下措施中选出适宜的改变条件:t2___ 、t8___ 。(此处两空均填下列选项字母序号)
a.增加CO的物质的量 b.加催化剂 c.升高温度 d.压缩容器体积 e.将CH3OH气体液化 f.充入氦气
②若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线___ 。
(3)已知反应2NO(g)+2CO(g) N2(g)+2CO2(g)在100kPa下△H=-113.0kJ/mol,△S=-145.3J·mol-1·K-1。理论上,该反应在温度
N2(g)+2CO2(g)在100kPa下△H=-113.0kJ/mol,△S=-145.3J·mol-1·K-1。理论上,该反应在温度___ (填“高于”或“低于”)___ 时均可自发进行。
 CO2(g)+H2(g)。
CO2(g)+H2(g)。得到如下两组数据:
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需要的时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
①实验1中以v(CO2)表示的反应速率为
②该反应的逆反应为
(2)在一容积为2L的密闭容器内加入2mol的CO和6mol的H2,在一定条件下发生如下反应:CO(g)+2H2(g)
 CH3OH(g) △H<0该反应的逆反应速率与时间的关系如图所示:
CH3OH(g) △H<0该反应的逆反应速率与时间的关系如图所示:
①由图可知反应在t1、t3、t7时都达到平衡,而在t2、t8时都改变了条件,试从以下措施中选出适宜的改变条件:t2
a.增加CO的物质的量 b.加催化剂 c.升高温度 d.压缩容器体积 e.将CH3OH气体液化 f.充入氦气
②若t4时降压,t5时达到平衡,t6时增大反应物的浓度,请在图中画出t4~t6时逆反应速率与时间的关系曲线
(3)已知反应2NO(g)+2CO(g)
 N2(g)+2CO2(g)在100kPa下△H=-113.0kJ/mol,△S=-145.3J·mol-1·K-1。理论上,该反应在温度
N2(g)+2CO2(g)在100kPa下△H=-113.0kJ/mol,△S=-145.3J·mol-1·K-1。理论上,该反应在温度
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】(1) ① 25℃时,NH4Cl溶液呈酸性,原因是______ 水解引起的(填“NH4+”或“Cl-”);
② 常温下,0.0100mol/L NaOH溶液的pH=___________ ;
③ 用0.0100mol/L 盐酸滴定未知浓度的NaOH溶液,酚酞作指示剂,滴定终点时,溶液的颜色由浅红色变为_______ (填“蓝色”或“无色”),且半分钟内颜色保持不变。
④ 已知在25℃:AgCl(s) Ag+(aq)+Cl-(aq) Ksp=1.8×10-10
Ag+(aq)+Cl-(aq) Ksp=1.8×10-10
Ag2S(s) 2Ag+(aq)+S2-(aq) Ksp=6.3×10-50
2Ag+(aq)+S2-(aq) Ksp=6.3×10-50
向浓度均为0.001 mol/L的NaCl和Na2S的混合溶液中,逐滴加入AgNO3溶液,最先产生的沉淀是_________ (填“AgCl”或“Ag2S”)。
(2)已知25℃合成氨反应中,1mol N2完全转化为NH3时释放的能量为92.4 kJ。现将1mol N2和3mol H2混合置于2L密闭容器中,反应进行到2s末测得NH3为0.4mol。
回答下列:
① 该反应的热化学方程式是______________ ;
② 该反应达到平衡后,升高温度平衡向_______ (填“正”、“逆”)反应方向移动;加入催化剂平衡________ (填“正”、“逆”、 “不”)移动;
③ 前2s内v(H2)是___________ 。
(3)燃料电池能量转化率高,具有广阔的发展前景。天然气燃料电池中,在负极发生反应的物质是________ (填化学式);如果该电池中的电解质溶液是KOH溶液,电极B电极上发生的电极反应式是:______________ 。
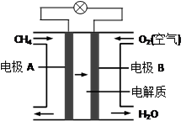 。
。
② 常温下,0.0100mol/L NaOH溶液的pH=
③ 用0.0100mol/L 盐酸滴定未知浓度的NaOH溶液,酚酞作指示剂,滴定终点时,溶液的颜色由浅红色变为
④ 已知在25℃:AgCl(s)
 Ag+(aq)+Cl-(aq) Ksp=1.8×10-10
Ag+(aq)+Cl-(aq) Ksp=1.8×10-10Ag2S(s)
 2Ag+(aq)+S2-(aq) Ksp=6.3×10-50
2Ag+(aq)+S2-(aq) Ksp=6.3×10-50向浓度均为0.001 mol/L的NaCl和Na2S的混合溶液中,逐滴加入AgNO3溶液,最先产生的沉淀是
(2)已知25℃合成氨反应中,1mol N2完全转化为NH3时释放的能量为92.4 kJ。现将1mol N2和3mol H2混合置于2L密闭容器中,反应进行到2s末测得NH3为0.4mol。
回答下列:
① 该反应的热化学方程式是
② 该反应达到平衡后,升高温度平衡向
③ 前2s内v(H2)是
(3)燃料电池能量转化率高,具有广阔的发展前景。天然气燃料电池中,在负极发生反应的物质是
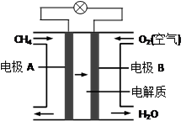 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
真题
【推荐2】以废旧铅酸电池中的含铅废料(Pb、PbO、PbO2、PbSO4及炭黑等)和H2SO4为原料,制备高纯PbO,实现铅的再生利用。其工作流程如下:

(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是__________ 。
(2)过程Ⅰ中,Fe2+催化过程可表示为:
i:2Fe2++ PbO2+4H++SO42− 2Fe3++PbSO4+2H2O
2Fe3++PbSO4+2H2O
ii: ……
①写出ii的离子方程式:________________ 。
②下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b.______________ 。
(3)PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq) NaHPbO2(aq),其溶解度曲线如图所示。
NaHPbO2(aq),其溶解度曲线如图所示。
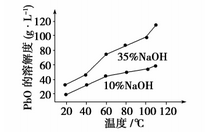
①过程Ⅱ的目的是脱硫。滤液1经处理后可在过程Ⅱ中重复使用,其目的是_____ (选填序号)。
②过程Ⅲ的目的是提纯。结合上述溶解度曲线,简述过程Ⅲ的操作:____ 。

(1)过程Ⅰ中,在Fe2+催化下,Pb和PbO2反应生成PbSO4的化学方程式是
(2)过程Ⅰ中,Fe2+催化过程可表示为:
i:2Fe2++ PbO2+4H++SO42−
 2Fe3++PbSO4+2H2O
2Fe3++PbSO4+2H2Oii: ……
①写出ii的离子方程式:
②下列实验方案可证实上述催化过程。将实验方案补充完整。
a.向酸化的FeSO4溶液中加入KSCN溶液,溶液几乎无色,再加入少量PbO2,溶液变红。
b.
(3)PbO溶解在NaOH溶液中,存在平衡:PbO(s)+NaOH(aq)
 NaHPbO2(aq),其溶解度曲线如图所示。
NaHPbO2(aq),其溶解度曲线如图所示。
①过程Ⅱ的目的是脱硫。滤液1经处理后可在过程Ⅱ中重复使用,其目的是
A.减少PbO的损失,提高产品的产率 B.重复利用NaOH,提高原料的利用率
C.增加Na₂SO4浓度,提高脱硫效率
②过程Ⅲ的目的是提纯。结合上述溶解度曲线,简述过程Ⅲ的操作:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】以下是一些物质的熔沸点数据(常压):
中国科学家用金属钠和CO2在一定条件下制得了金刚石: 4 Na + 3CO2 2 Na2CO3 + C(s,金刚石)
2 Na2CO3 + C(s,金刚石)
(1)若反应在常压、890℃下进行,写出该反应的平衡常数表达式_________ 。若3v正(Na)=4v逆(CO2),则_____ (选填序号)。
a 反应肯定达到平衡 b 反应可能达到平衡 c 反应肯定未达平衡
(2)反应中还有石墨生成,已知:C(s,石墨) C(s,金刚石)- 1.9KJ,则升高温度,生成的碳单质中,金刚石的含量将
C(s,金刚石)- 1.9KJ,则升高温度,生成的碳单质中,金刚石的含量将________ (选填“增大”“减小”“不变”)。在高压下有利于金刚石的制备,理由是_______ ;
(3)石墨的熔点比金刚石高,理由是__________ (选填序号)。
a 石墨中碳碳键键能更大 b 石墨有自由电子 c 石墨层与层之间有范德华力
(4)把副产物Na2CO3溶解,其溶液中存在的平衡体系请分别用化学用语表示出来__________ .若反应在10L密闭容器、常压下进行,温度由890℃升高到1860℃,则_______ 。
(5)容器内气体的平均相对分子质量将________ (选填“增大”“减小”“不变”);
(6)若反应时间为10min, 金属钠的物质的量减少了0.2mol,则10min里CO2的平均反应速率为_______ 。
| 钠 | Na2CO3 | 金刚石 | 石墨 | |
| 熔点(℃) | 97.8 | 851 | 3550 | 3850 |
| 沸点(℃) | 882.9 | 1850(分解产生CO2) | ---- | 4250 |
中国科学家用金属钠和CO2在一定条件下制得了金刚石: 4 Na + 3CO2
 2 Na2CO3 + C(s,金刚石)
2 Na2CO3 + C(s,金刚石)(1)若反应在常压、890℃下进行,写出该反应的平衡常数表达式
a 反应肯定达到平衡 b 反应可能达到平衡 c 反应肯定未达平衡
(2)反应中还有石墨生成,已知:C(s,石墨)
 C(s,金刚石)- 1.9KJ,则升高温度,生成的碳单质中,金刚石的含量将
C(s,金刚石)- 1.9KJ,则升高温度,生成的碳单质中,金刚石的含量将(3)石墨的熔点比金刚石高,理由是
a 石墨中碳碳键键能更大 b 石墨有自由电子 c 石墨层与层之间有范德华力
(4)把副产物Na2CO3溶解,其溶液中存在的平衡体系请分别用化学用语表示出来
(5)容器内气体的平均相对分子质量将
(6)若反应时间为10min, 金属钠的物质的量减少了0.2mol,则10min里CO2的平均反应速率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】I.一定条件下,在容积为5L的密闭容器中,A、B、C三种气体的物质的量n随时间t的变化如图甲所示。已知达到平衡后,降低温度,A的体积分数减小。
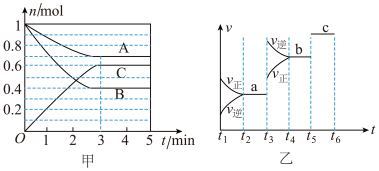
(1)该反应的化学方程式为_______ 。
(2)该反应的反应速率v随时间t的关系如图乙所示。
①根据图乙判断,在t3时刻改变的外界条件是_______ 。
②a、b、c对应的平衡状态中,C的体积分数最大的是状态_______ 。
II.在密闭容器中充入一定量的 ,发生反应:
,发生反应: ,如图丙所示为
,如图丙所示为 气体分解生成
气体分解生成 和
和 的平衡转化率与温度、压强的关系。
的平衡转化率与温度、压强的关系。
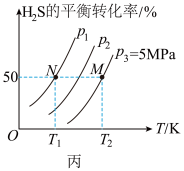
(3)
____ 0(填“>”“<”或“=”)。比较M点和N点对应的平衡常数的大小:KM_____ KN。
(4)图丙中压强( 、
、 、
、 )由大到小的顺序为
)由大到小的顺序为_______ 。
(5)图丙中M点对应的平衡常数
_______  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(6)如果想进一步提高 的转化率,除改变温度、压强外,还可以采取的措施
的转化率,除改变温度、压强外,还可以采取的措施_______ 。

(1)该反应的化学方程式为
(2)该反应的反应速率v随时间t的关系如图乙所示。
①根据图乙判断,在t3时刻改变的外界条件是
②a、b、c对应的平衡状态中,C的体积分数最大的是状态
II.在密闭容器中充入一定量的
 ,发生反应:
,发生反应: ,如图丙所示为
,如图丙所示为 气体分解生成
气体分解生成 和
和 的平衡转化率与温度、压强的关系。
的平衡转化率与温度、压强的关系。
(3)

(4)图丙中压强(
 、
、 、
、 )由大到小的顺序为
)由大到小的顺序为(5)图丙中M点对应的平衡常数

 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(6)如果想进一步提高
 的转化率,除改变温度、压强外,还可以采取的措施
的转化率,除改变温度、压强外,还可以采取的措施
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】工业合成氨是人类科学技术的一项重大突破,其原理为N2(g)+3H2(g) 2NH3(g) △H<0生产示意图如图:
2NH3(g) △H<0生产示意图如图:
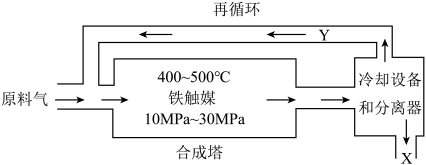
(1)下列有关合成氨工业的说法正确的是________ 。
(2)循环利用的Y是________ ,目的是________ 。
(3)合成氨反应中,某时刻改变条件速率变化如图:

图I中t0时刻改变的条件是________ ,图II中t0时刻改变的条件是________ 。
(4)在合成氨工业中,既能加快反应速率,又能增大氢气转化率采取的措施是________ 。
A.增加N2
B.移走NH3
C.升高温度
D.恒温恒容,充入惰性气体Ar使压强增大
E.压缩体积
(5)氮的固定和氮的循环是几百年来科学家一直研究的课题。如表列举了不同温度下大气固氮和工业固氮的部分K值。
①分析数据可知:①在400℃下模拟工业固氮,某时刻c(N2)=c(H2)=c(NH3)=1mol•L-1,此时v正________ v逆(填“>”“<”或“=”)。
②人类不适合大规模模拟大气固氮的原因是________ 。
 2NH3(g) △H<0生产示意图如图:
2NH3(g) △H<0生产示意图如图:
(1)下列有关合成氨工业的说法正确的是
| A.工业合成氨的反应是熵减小的放热反应,在低温时可自发进行 |
| B.合成氨反应中,反应物的总键能小于产物的总键能 |
| C.合成氨厂一般采用的压强为10MPa~30MPa,因为该压强下铁触媒的活性最高 |
| D.N2的量越多,H2的转化率越大,因此,充入的N2越多越有利于NH3的合成 |
(2)循环利用的Y是
(3)合成氨反应中,某时刻改变条件速率变化如图:

图I中t0时刻改变的条件是
(4)在合成氨工业中,既能加快反应速率,又能增大氢气转化率采取的措施是
A.增加N2
B.移走NH3
C.升高温度
D.恒温恒容,充入惰性气体Ar使压强增大
E.压缩体积
(5)氮的固定和氮的循环是几百年来科学家一直研究的课题。如表列举了不同温度下大气固氮和工业固氮的部分K值。
| 反应 | 大气固氮N2(g)+O2(g) 2NO(g) 2NO(g) | 工业固氮N2(g)+3H2(g) 2NH3(g) 2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
②人类不适合大规模模拟大气固氮的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】丙烯等不饱和烃在有机化工领域有重要的用途,工业上常采用“丙烷脱氢法”制取丙烯,反应的原理为:C3H8(g) C3H6(g)+H2(g) ΔH=+123kJ/mol
C3H6(g)+H2(g) ΔH=+123kJ/mol
回答下列问题:
(1)在石油工业中可通过___ 工艺获得丙烯等不饱和烃(填一种工艺的名称)。
(2)已知:
表中的a=___ 。
(3)工业上进行该反应时,常在丙烷中掺入稀有气体作为稀释剂,在体积可变的反应容器中,维持恒温,并使总压强恒定为0.1MPa,掺入稀有气体作为稀释剂的优点是___ ,试从平衡角度加以解释___ 。
(4)在某密闭容器中充入适量的丙烷,测得丙烷的转化率随温度和压强变化如图所示:
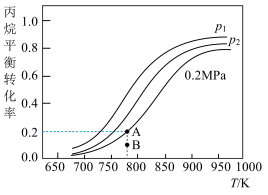
①压强p1___ p2(填“>”、“<”或“=”)。
②图中A点平衡常数Kp=___ (用平衡分压代替平衡浓度,分压=总压×物质的量分数,结果保留三位有效数字)。
③B点若达到A点所示的平衡状态则在建立平衡过程中v正___ v逆(填“>”、“<”或“=”)。
④写出一条提高丙烷平衡转化率的措施___ 。
 C3H6(g)+H2(g) ΔH=+123kJ/mol
C3H6(g)+H2(g) ΔH=+123kJ/mol回答下列问题:
(1)在石油工业中可通过
(2)已知:
| 化学键 | C-H | C-C | C=C | H-H |
| 键能(kJ/mol) | 412 | 348 | a | 436 |
(3)工业上进行该反应时,常在丙烷中掺入稀有气体作为稀释剂,在体积可变的反应容器中,维持恒温,并使总压强恒定为0.1MPa,掺入稀有气体作为稀释剂的优点是
(4)在某密闭容器中充入适量的丙烷,测得丙烷的转化率随温度和压强变化如图所示:

①压强p1
②图中A点平衡常数Kp=
③B点若达到A点所示的平衡状态则在建立平衡过程中v正
④写出一条提高丙烷平衡转化率的措施
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】研究化学反应速率与平衡原理有助于学科思维的提升。
(1)已知焓变与熵变有如下关系:△G=ΔH-TΔS,某反应当△G<0时自发,△G>0不自发。今有A、B、C、D四个反应的焓变、熵变数据如下:
①在任何温度下都能自发进行的反应是_______ (选填ABCD序号,下同);
②任何温度下都不能自发进行的反应是_______ 。
(2)利用图所示装置,可测定盐酸与碳酸钙反应生成CO2的反应速率。请根据要求填空:
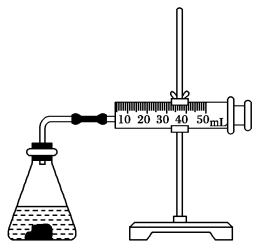
①连接仪器、检查装置气密后,在锥形瓶中加入5 g碳酸钙,迅速加入20 mL 1 mol·L-1盐酸,塞紧瓶塞。
②每隔10 s观测注射器中气体的体积,并以mL·s-1为反应速率的单位,计算每10 s内的反应速率。数据处理的结果见下表:
表格中的“?”处应填的数据是_______ ;从反应速率随时间变化的数据可知,本实验中反应速率与_______ 和_______ 有关。
(3)反应速率(v)和反应物浓度(c)的关系可以用实验方法测定。如化学反应 的正反应速率可表示为
的正反应速率可表示为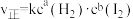 ,式中k为常数,a、b的值可用下表数据确定。据表中数据可推出a=
,式中k为常数,a、b的值可用下表数据确定。据表中数据可推出a=_______ 、b=_______ 。
(4)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),K为化学平衡常数,K和温度的关系如下表:
CO(g)+H2O(g),K为化学平衡常数,K和温度的关系如下表:
根据以上信息推断:
①该反应为_______ 热反应;
②达到平衡后,在其他条件不变情况下加入干燥剂无水氯化钙,氢气的转化率将_______ ;
③1000℃,某时刻CO2、H2、CO、H2O的物质的量分别为0.2mol、0.8mol、0.4mol、0.4mol,此时V正_______ V逆(填“>”、“<”或“=”)。
(5)在3种不同条件下,分别向容积为2 L的恒容密闭容器中充入2 mol A和1 mol B,发生反应:2A(g)+B(g) 2D(g) ΔH=Q kJ·mol-1。相关条件和数据见下表。回答:
2D(g) ΔH=Q kJ·mol-1。相关条件和数据见下表。回答:
①K1、K2和K3三者的关系为_______ ;
②实验Ⅱ改变的条件可能是:_______ ;
③分别达平衡后,实验Ⅰ与实验Ⅲ容器内的压强大小关系是:Ⅰ_______ Ⅲ(选填“大于”、“小于”、“等于”);
④实验Ⅲ达平衡后,恒温下再向容器中通入1 mol A和1 mol D,平衡将_______ (选填“朝正向移动”、“朝逆向移动”、“不移动”)。
(1)已知焓变与熵变有如下关系:△G=ΔH-TΔS,某反应当△G<0时自发,△G>0不自发。今有A、B、C、D四个反应的焓变、熵变数据如下:
| 反应 | A | B | C | D |
| ΔH/(kJ·mol-1) | 10.5 | 1.80 | -126 | -11.7 |
| ΔS/(J·mol-1·K-1) | 30.0 | -113.0 | 84.0 | -105.0 |
②任何温度下都不能自发进行的反应是
(2)利用图所示装置,可测定盐酸与碳酸钙反应生成CO2的反应速率。请根据要求填空:

①连接仪器、检查装置气密后,在锥形瓶中加入5 g碳酸钙,迅速加入20 mL 1 mol·L-1盐酸,塞紧瓶塞。
②每隔10 s观测注射器中气体的体积,并以mL·s-1为反应速率的单位,计算每10 s内的反应速率。数据处理的结果见下表:
| 时间/s | 10 | 20 | 30 | 40 | 50 | 60 |
| 气体体积/mL | 4 | 14 | 25 | 38 | 47 | 55 |
| 反应速率/(mL·s-1) | 0.4 | 1.0 | 1.1 | ? | 0.9 | 0.8 |
(3)反应速率(v)和反应物浓度(c)的关系可以用实验方法测定。如化学反应
 的正反应速率可表示为
的正反应速率可表示为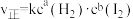 ,式中k为常数,a、b的值可用下表数据确定。据表中数据可推出a=
,式中k为常数,a、b的值可用下表数据确定。据表中数据可推出a=| c(H2)/(mol·L-1) | c(I2)/(mol·L-1) | v/(mol·L-1·s-1) |
| 0.5 | 4.0 | 1.0k |
| 1.0 | 4.0 | 2.0k |
 CO(g)+H2O(g),K为化学平衡常数,K和温度的关系如下表:
CO(g)+H2O(g),K为化学平衡常数,K和温度的关系如下表:| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
①该反应为
②达到平衡后,在其他条件不变情况下加入干燥剂无水氯化钙,氢气的转化率将
③1000℃,某时刻CO2、H2、CO、H2O的物质的量分别为0.2mol、0.8mol、0.4mol、0.4mol,此时V正
(5)在3种不同条件下,分别向容积为2 L的恒容密闭容器中充入2 mol A和1 mol B,发生反应:2A(g)+B(g)
 2D(g) ΔH=Q kJ·mol-1。相关条件和数据见下表。回答:
2D(g) ΔH=Q kJ·mol-1。相关条件和数据见下表。回答:| 实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应温度/℃ | 700 | 700 | 750 |
| 达平衡时间/min | 40 | 5 | 30 |
| n(D)平衡/mol | 1.5 | 1.5 | 1 |
| 化学平衡常数 | K1 | K2 | K3 |
②实验Ⅱ改变的条件可能是:
③分别达平衡后,实验Ⅰ与实验Ⅲ容器内的压强大小关系是:Ⅰ
④实验Ⅲ达平衡后,恒温下再向容器中通入1 mol A和1 mol D,平衡将
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】“低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用.试回答下列问题:
(1)高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g) Fe(s)+CO2(g) △H>0。已知在1100°C时,该反应的化学平衡常数K=0.263。
Fe(s)+CO2(g) △H>0。已知在1100°C时,该反应的化学平衡常数K=0.263。
①温度升高,平衡移动后达到新平衡,此时平衡常数值____ (填“增大”“减小”“不变”);
②1100°C时测得高炉中,c(CO2)=0.025mol·L﹣1,c(CO)=0.1mol·L﹣1,则在这种情况下,该反应这一时刻向_______ 进行(填“左”或“右”)。
(2)目前工业上也可用CO2来生产燃料甲醇CH3OH,有关反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g),△H=﹣49.0KJmol﹣1,某温度下,向体积为1L恒容密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示.
CH3OH(g)+H2O(g),△H=﹣49.0KJmol﹣1,某温度下,向体积为1L恒容密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示.

①反应开始至平衡,氢气的平均反应速率v(H2)=______ ,CO2的转化率为_____ ;该温度下上述反应的平衡常数K=_____ (分数表示);
②反应达到平衡后,下列能使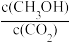 的值增大的措施是
的值增大的措施是______ (填符号)。
a.升高温度 b.再充入H2 c.再充入CO2 d.将H2O(g)从体系中分离 e.充入He(g)
③有人提出,可以设计反应2CO(g)=2C(s)+O2(g) (△H>0)来消除CO的污染,请你判断上述反应是否能自发进行并说明理由________ 。
(1)高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g)
 Fe(s)+CO2(g) △H>0。已知在1100°C时,该反应的化学平衡常数K=0.263。
Fe(s)+CO2(g) △H>0。已知在1100°C时,该反应的化学平衡常数K=0.263。①温度升高,平衡移动后达到新平衡,此时平衡常数值
②1100°C时测得高炉中,c(CO2)=0.025mol·L﹣1,c(CO)=0.1mol·L﹣1,则在这种情况下,该反应这一时刻向
(2)目前工业上也可用CO2来生产燃料甲醇CH3OH,有关反应为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),△H=﹣49.0KJmol﹣1,某温度下,向体积为1L恒容密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示.
CH3OH(g)+H2O(g),△H=﹣49.0KJmol﹣1,某温度下,向体积为1L恒容密闭容器中,充入1molCO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示.
①反应开始至平衡,氢气的平均反应速率v(H2)=
②反应达到平衡后,下列能使
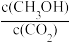 的值增大的措施是
的值增大的措施是a.升高温度 b.再充入H2 c.再充入CO2 d.将H2O(g)从体系中分离 e.充入He(g)
③有人提出,可以设计反应2CO(g)=2C(s)+O2(g) (△H>0)来消除CO的污染,请你判断上述反应是否能自发进行并说明理由
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】氨是化肥工业和基本有机化工的主要原料,合成氨的反应如下: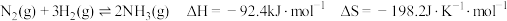
(1)判断合成氨的反应在_________ (选填“高温、低温”)能自发进行,推动反应在该条件下自发进行的主要因素是反应的_________ (选填“焓变、熵变”)。
(2)不同条件下,分别测得上述反应的反应速率,其中表示该反应进行得最快的是_______ 。
a.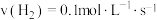 b.
b.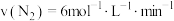
c.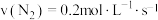 d.
d.
(3)一定温度下,向 密闭容器中加入
密闭容器中加入 和
和 ,发生上述反应,
,发生上述反应, 物质的量随时间的变化如下图所示。
物质的量随时间的变化如下图所示。
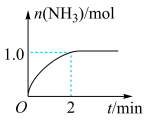
 内的平均反应速率
内的平均反应速率
________________ 。
根据反应条件,判断 内
内 变化趋势为
变化趋势为______ ,运用有效碰撞理论来解释该变化趋势:_______ 。
(4)在合成氨的实际生产过程中,常常加入含铁催化剂.请结合过渡态理论解释使用催化剂使反应速率加快的原因_______ 。
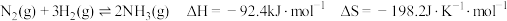
(1)判断合成氨的反应在
(2)不同条件下,分别测得上述反应的反应速率,其中表示该反应进行得最快的是
a.
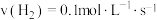 b.
b.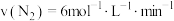
c.
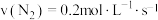 d.
d.
(3)一定温度下,向
 密闭容器中加入
密闭容器中加入 和
和 ,发生上述反应,
,发生上述反应, 物质的量随时间的变化如下图所示。
物质的量随时间的变化如下图所示。
 内的平均反应速率
内的平均反应速率
根据反应条件,判断
 内
内 变化趋势为
变化趋势为(4)在合成氨的实际生产过程中,常常加入含铁催化剂.请结合过渡态理论解释使用催化剂使反应速率加快的原因
您最近一年使用:0次



