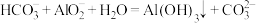常温下,Ka(HCOOH)=1.77xlO-4, Ka(CH3COOH)= Kb(NH3•H20)=1.75x 10-5,下列说法不正确的是
| A.浓度均为0.1 mol•L-1的HCOOH和NH3•H20溶液中:c(HCOO-)>c(NH4+) |
| B.用相同浓度的NaOH溶液分别滴定等体积pH均为3的HCOOH和CH3COOH溶液至终点,HCOOH消耗NaOH溶液的体积比CH3COOH小 |
| C.0.1 mol• L-1CH3COOH溶液与0.1 mol• L-1NaOH溶液等体积混合后,溶液的pH=7 |
| D.pH=7的HCOOH和NH3•H20的混合溶液中,c(HCOO—)=c(NH4+) |
更新时间:2018-10-31 16:05:03
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列电离方程式正确的是
A.H2SO3 2H++SO 2H++SO |
B.NaHCO3 Na++HCO Na++HCO |
C.NH3•H2O NH NH +OH- +OH- |
D.NaHSO4 Na++HSO Na++HSO |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,某碳酸溶液中的 、
、 、
、 的物质的量分数δ随pH的变化如下图所示。下列叙述错误的是
的物质的量分数δ随pH的变化如下图所示。下列叙述错误的是

 、
、 、
、 的物质的量分数δ随pH的变化如下图所示。下列叙述错误的是
的物质的量分数δ随pH的变化如下图所示。下列叙述错误的是
A.当溶液中δ( )达到最大时:c( )达到最大时:c( )>c( )>c( ) ) |
B.Ka2( )的数量级为10-11 )的数量级为10-11 |
C.调节溶液的pH由8~10的过程中 减小 减小 |
D.加入NaOH使溶液pH=9时,主要反应为 + + = = + + |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列图示与对应的叙述不正确的是
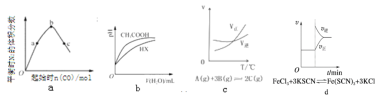

A.a表示反应4CO(g)+2NO2(g) N2(g)+4CO2(g),保持其他条件不变,改变CO的物质的量,平衡时N2的体积分数变化情况。由图可知,NO2的转化率:c>b>a N2(g)+4CO2(g),保持其他条件不变,改变CO的物质的量,平衡时N2的体积分数变化情况。由图可知,NO2的转化率:c>b>a |
| B.b表示25℃时,分别加水稀释体积均为100mL、pH=2的CH3COOH溶液和HX溶液,则25℃时HX的电离平衡常数小于CH3COOH的电离平衡常数 |
| C.c是其他条件一定时,反应速率随温度变化的图像,正反应△H>0 |
| D.d是在平衡体系的溶液中溶入少量KCl固体后化学反应速率随时间变化的图像 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关图象说法不正确 的是
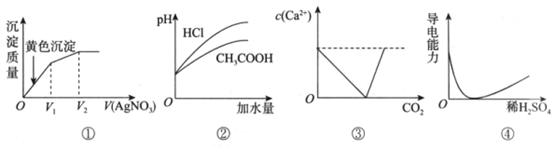

| A.图①:向等浓度的碘化钠和氯化钠的混合溶液中加入硝酸银溶液 |
| B.图②:向pH和体积均相同的盐酸和醋酸两种溶液中分别加水稀释 |
| C.图③:向饱和Ca(OH)2溶液中通入CO2 |
| D.图④:向Ba(OH)2溶液中加入稀H2SO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】已知25℃时,电离常数Ka(HF)=3.6×10-4,溶度积常数Ksp(CaF2)=1.46×10-10。现向1 L 0.1mol·L-1HF溶液中加入0.1 mol CaCl2固体(不考虑溶液体积变化),则下列说法中错误的是
| A.原HF溶液c(H+)约为6×10-3mol·L-1 |
| B.加入 CaCl2后溶液中有CaF2沉淀产生 |
| C.加入CaCl2后溶液中的c(H+)浓度不变 |
| D.2HF(aq)+Ca2+(aq)=CaF2(s)+2H+(aq)的平衡常数为K=8.88×102 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,往某酸的钠盐Na2A溶液中通入HCl,溶液中-lg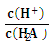 和-lgc(HA-)或-lg
和-lgc(HA-)或-lg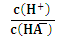 和-1gc(A2-)的关系如图所示。下列说法正确的是
和-1gc(A2-)的关系如图所示。下列说法正确的是
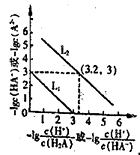
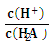 和-lgc(HA-)或-lg
和-lgc(HA-)或-lg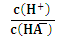 和-1gc(A2-)的关系如图所示。下列说法正确的是
和-1gc(A2-)的关系如图所示。下列说法正确的是
A.直线L2表示-lg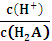 和-lgc(HA-)的关系 和-lgc(HA-)的关系 |
| B.通入HCl过程中,水电离的c(OH-)与水电离的c(H+)的乘积不断增大 |
| C.c(H2A)的数量级为10-7 |
| D.在NaHA溶液中c(Na+)>(HA-)>c(H2A)>c(A2-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法错误的有几句
①NaHCO3溶液加水稀释, 的比值保持增大
的比值保持增大
②浓度均为0.1mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO )+c(HCO
)+c(HCO )]
)]
③在0.1mol·L-1氨水中滴加0.lmol·L-1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=l0-amol·L-1
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO )均增大
)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH-)+c(H2S)+c(HS-)
①NaHCO3溶液加水稀释,
 的比值保持增大
的比值保持增大②浓度均为0.1mol·L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO
 )+c(HCO
)+c(HCO )]
)]③在0.1mol·L-1氨水中滴加0.lmol·L-1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=l0-amol·L-1
④向0.1mol/LNa2SO3溶液中加入少量NaOH固体,c(Na+)、c(SO
 )均增大
)均增大⑤在Na2S稀溶液中,c(H+)=c(OH-)+c(H2S)+c(HS-)
| A.4 | B.3 | C.2 | D.1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】现有HA、HB两种酸。25℃时,用0.1000mol/LNaOH溶液分别滴定20.00mL浓度均为0.1000mol/L的HA、HB两种酸的溶液,滴定过程中溶液的pH随滴入的NaOH溶液体积的变化如图。下列说法正确的是


| A.b 点对应的溶液中c(B-)> c(HB) |
| B.用NaOH溶液滴定HB溶液时适宜用甲基橙指示剂 |
| C.曲线Ⅰ上的c点溶液中:c(B-) > c(Na+) >c(OH-)>c(H+) |
| D.中和等体积、等浓度的HB和HA,所需NaOH:HA>HB |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知X为 的
的 溶液,Y为
溶液,Y为 的
的 溶液。常温下,下列各溶液中,微粒的物质的量浓度关系错误的是
溶液。常温下,下列各溶液中,微粒的物质的量浓度关系错误的是
 的
的 溶液,Y为
溶液,Y为 的
的 溶液。常温下,下列各溶液中,微粒的物质的量浓度关系错误的是
溶液。常温下,下列各溶液中,微粒的物质的量浓度关系错误的是A.X中存在: |
B.Y中存在: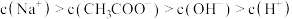 |
C.X和Y等体积混合的溶液中: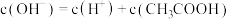 |
D.X和Y等体积混合的溶液中: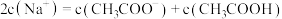 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是( )
| A.pH=6.8的溶液一定显酸性 |
B.相同物质的量浓度的下列溶液中:①NH4Al(SO4)2、②NH4Cl、③CH3COONH4,则c(NH )由大到小的顺序是:①>②>③ )由大到小的顺序是:①>②>③ |
| C.电离平衡常数(K)只与弱电解质本身有关,与其它外部因素无关 |
| D.0.1 mol•L-1的硫化钠溶液中:c(H+)+c(Na+)=c(OH-)+c(HS-)+c(S2-) |
您最近一年使用:0次

 >1
>1 含
含 、
、 ,过滤后得到滤液用
,过滤后得到滤液用 溶液处理,测得溶液pH和
溶液处理,测得溶液pH和 生成的量随加入
生成的量随加入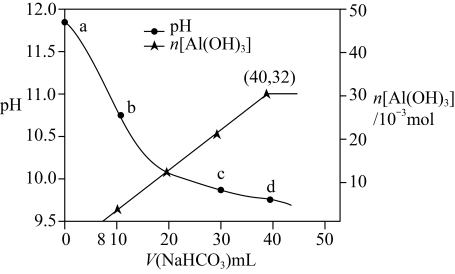


 、
、 、
、 、
、