关于醋酸(CH3COOH)的下列性质中,不能证明它是弱电解质的是
| A.把pH=2的醋酸溶液稀释100倍后pH=3.8 |
| B.100mL l mol·L-1的醋酸溶液恰好与100mL l mol·L-1的NaOH溶液完全反应 |
| C.醋酸钠CH3COONa溶液能使酚酞试液变红 |
| D.0.1 mol·L-1的醋酸溶液的pH约为2 |
更新时间:2019-01-24 16:13:19
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】下列事实不能证明HNO2是弱电解质的是
| A.滴入酚酞试液,NaNO2溶液显红色 |
| B.用HNO2溶液做导电实验,灯泡很暗 |
C.HNO2溶液中的微粒中有:HNO2、H+、NO 、OH-、H2O 、OH-、H2O |
| D.0.10 mol/L HNO2溶液的pH=2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】取 的NaA和NaB两种盐溶液各1L,分别通入
的NaA和NaB两种盐溶液各1L,分别通入 ,发生反应:
,发生反应: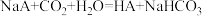 、
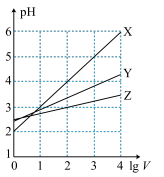
、 ,则1LHA溶液和HB溶液分别加水稀释至溶液体积为VL时,可能对应的图中的线是( )
,则1LHA溶液和HB溶液分别加水稀释至溶液体积为VL时,可能对应的图中的线是( )
 的NaA和NaB两种盐溶液各1L,分别通入
的NaA和NaB两种盐溶液各1L,分别通入 ,发生反应:
,发生反应: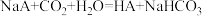 、
、 ,则1LHA溶液和HB溶液分别加水稀释至溶液体积为VL时,可能对应的图中的线是( )
,则1LHA溶液和HB溶液分别加水稀释至溶液体积为VL时,可能对应的图中的线是( )
| A.X对应的是HA、Z对应的是HB | B.Y对应的是HA、Z对应的是HB |
| C.Z对应的是HA、X对应的是HB | D.Z对应的是HA、Y对应的是HB |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列说法不正确的是
| A.0.1mol•L-1CH3COOH溶液加水稀释,CH3COO-数目增多,c(OH-)增大 |
B.室温下,NaHSO3溶液的pH<7,说明 的电离程度大于其水解程度 的电离程度大于其水解程度 |
| C.酸碱质子理论认为,凡能给出质子(H+)的物质都是酸,凡能接受质子的物质都是碱。由该理论可知:NaHCO3、H2O、Al(OH)3均可称为酸碱两性物质 |
| D.25℃时0.1mol•L-1的H2S水溶液中,加入一定量的NaOH溶液,当溶液中存在:c(Na+)=c(S2-)+c(HS-)+c(H2S)时,溶液的主要溶质为Na2S |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下向 的醋酸溶液中加水稀释后,下列说法正确的是
的醋酸溶液中加水稀释后,下列说法正确的是
 的醋酸溶液中加水稀释后,下列说法正确的是
的醋酸溶液中加水稀释后,下列说法正确的是| A.溶液中带电粒子的数目不变 |
B.溶液中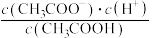 不变 不变 |
C.醋酸的电离程度增大, 亦增大 亦增大 |
| D.醋酸的电离常数Ka随醋酸浓度减小而减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列各项比较中,一定相等的是
A.相同物质的量浓度的氨水和NH4Cl溶液中的 的物质的量浓度 的物质的量浓度 |
| B.相同物质的量的Na分别完全转化为Na2O和Na2O2时转移电子的数目 |
| C.相同物质的量的正丁烷和2-甲基丁烷中含有的C―H键的数目 |
| D.标准状况下,相同体积的乙炔和水中含有的H原子的数目 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,用0.1 mol·L-1的NaOH溶液滴定0.1 mol·L-1某二元弱酸H2R溶液的滴定曲线如图所示。下列说法正确的是

已知:滴定分数为滴定过程中加入的NaOH溶液中NaOH的物质的量与待测溶液中H2R的物质的量之比。

已知:滴定分数为滴定过程中加入的NaOH溶液中NaOH的物质的量与待测溶液中H2R的物质的量之比。
A.a点溶液中存在: |
B.b点溶液中存在: |
C.c点溶液中, |
D.a点至d点的过程中,混合溶液中 始终减小 始终减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】根据反应中质子(H+)的转移,可以重新定义酸和碱:酸=质子+(共轭)碱。因此酸碱之间存在彼此的共轭关系:HA+B⇌A-+BH+。关于反应:HC2O4-+H3O+ H2C2O4+H2O、HC2O4-+OH-
H2C2O4+H2O、HC2O4-+OH- C2O42-+H2O,下列判断正确的是
C2O42-+H2O,下列判断正确的是
 H2C2O4+H2O、HC2O4-+OH-
H2C2O4+H2O、HC2O4-+OH- C2O42-+H2O,下列判断正确的是
C2O42-+H2O,下列判断正确的是| A. HC2O4-的共轭碱为H2C2O4 |
| B. HC2O4-的共轭酸为C2O42- |
| C. HC2O4-既有酸性又有碱性 |
| D.H3O+是水的共轭碱,H2O是OH-的共轭酸 |
您最近一年使用:0次



