一定温度下,某密闭容器里发生如下反应:CO(g)+H2O(g)  CO2(g)+H2(g)(正反应为放热反应),当反应达到平衡时,测得容器中各物质的物质的量均为n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变时,下列措施中可以采用的是 ( )
CO2(g)+H2(g)(正反应为放热反应),当反应达到平衡时,测得容器中各物质的物质的量均为n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变时,下列措施中可以采用的是 ( )
①升高温度 ②增大压强 ③再通入n mol CO2和n mol H2 ④再加入2n mol CO2和2n mol H2(g)
 CO2(g)+H2(g)(正反应为放热反应),当反应达到平衡时,测得容器中各物质的物质的量均为n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变时,下列措施中可以采用的是 ( )
CO2(g)+H2(g)(正反应为放热反应),当反应达到平衡时,测得容器中各物质的物质的量均为n mol。欲使H2的物质的量浓度增大1倍,在其他条件不变时,下列措施中可以采用的是 ( )①升高温度 ②增大压强 ③再通入n mol CO2和n mol H2 ④再加入2n mol CO2和2n mol H2(g)
| A.①②④ | B.②④ |
| C.③④ | D.①②③ |
更新时间:2019-06-11 16:44:51
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】某温度下,分别在下列容积为2L的恒容绝热密闭容器中,发生如下反应: 2CO(g)+SO2(g)=S(g)+2CO2(g) △H>0。测得相关数据如下表所示。
下列说法正确的是
| 容器 | 起始时物质的量 | 平衡时CO(g)的浓度/mol·L | |||
| CO(g) | SO2(g) | S(g) | CO2(g) | ||
| 甲 | 1 | 0.5 | 0.5 | 1 | a |
| 乙 | 1 | 0.5 | 0 | 0 | 0.2 |
| 丙 | 0 | 0 | 1 | 2 | b |
下列说法正确的是
| A.平衡常数:K甲>K乙 |
| B.a=0.4 |
| C.若乙容器l0min达到平衡.则用S(g)表示的反应速率为0.005mol•L-1•min-1 |
| D.若将丙容器改为恒压绝热容器,则达到平衡时b=0.2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】在一定条件下,CO可以去除烟气中的SO2,其反应原理为2CO(g)+SO2(g)  2CO2(g)+S(l)。以疏松多孔的γAl2O3作为催化剂(其他条件相同),反应相同的时间,SO2的去除率随反应温度的变化如图所示(图中虚线表示相同条件下SO2的平衡去除率随温度的变化)。下列说法正确的是
2CO2(g)+S(l)。以疏松多孔的γAl2O3作为催化剂(其他条件相同),反应相同的时间,SO2的去除率随反应温度的变化如图所示(图中虚线表示相同条件下SO2的平衡去除率随温度的变化)。下列说法正确的是

 2CO2(g)+S(l)。以疏松多孔的γAl2O3作为催化剂(其他条件相同),反应相同的时间,SO2的去除率随反应温度的变化如图所示(图中虚线表示相同条件下SO2的平衡去除率随温度的变化)。下列说法正确的是
2CO2(g)+S(l)。以疏松多孔的γAl2O3作为催化剂(其他条件相同),反应相同的时间,SO2的去除率随反应温度的变化如图所示(图中虚线表示相同条件下SO2的平衡去除率随温度的变化)。下列说法正确的是
| A.该反应的ΔH>0 |
| B.180℃,SO2去除率较高的主要原因是SO2被γAl2O3吸附 |
| C.500℃时,其他条件不变,采用高效的催化剂可以提高SO2去除率 |
| D.X点恒容下再通入CO、CO2各0.1 mol,达到平衡前v(正)>v(逆) |
您最近一年使用:0次
【推荐1】恒温恒容下向2L密闭容器中加入SO3发生反应:2SO3(g) 2SO2(g)+O2(g),反应过程中测定的部分数据如下表:下列说法正确的是( )
2SO2(g)+O2(g),反应过程中测定的部分数据如下表:下列说法正确的是( )
 2SO2(g)+O2(g),反应过程中测定的部分数据如下表:下列说法正确的是( )
2SO2(g)+O2(g),反应过程中测定的部分数据如下表:下列说法正确的是( )反应时间/min | n(SO3)/mol | n(O2)/mol |
0 | 2.0 | 0 |
2 | 0.8 | |
4 | 0.6 | |
6 | 1.8 | 1.1 |
| A.0~2 min平均速率v(SO2)=0.6 mol·L﹣1·min﹣1 |
| B.4 min后,平衡移动的原因可能是减压 |
| C.若升高温度后的平衡常数的值为1.0,则该正反应为吸热反应 |
| D.若起始时容器中SO3的物质的量改为1.0 mol,则平衡时n(SO2)=0.6 mol |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】已知2SO2(g) + O2(g) 2SO3(g);ΔH=-197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3(g);ΔH=-197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是
 2SO3(g);ΔH=-197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是
2SO3(g);ΔH=-197 kJ·mol-1。向同温、同体积的三个密闭容器中分别充入气体:(甲) 2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2;(丙) 2 mol SO3。恒温、恒容下反应达平衡时,下列关系一定正确的是| A.容器内压强P:P甲=P丙> 2P乙 |
| B.SO3的质量m:m甲=m丙> 2m乙 |
| C.c(SO2)与c(O2)之比k:k甲=k丙> k乙 |
| D.反应放出或吸收热量的数值Q:Q甲=Q丙> 2Q乙 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列有关实验现象和解释或结论都正确的组合是
| 选项 | 实验操作 | 现象 | 解释或结论 |
A | 相同条件下,分别测量0.1molL1和0.01molL1醋酸溶液的导电性 | 前者的导电性强 | 醋酸浓度越大,电离程度越大 |
B | 向FeCl3和KSCN的混合溶液中加入KCl固体 | 血红色溶液变浅 | 增大KCl的浓度,使得平衡逆向移动 |
C | 两支试管各盛4mL0.1mol/L酸性高锰酸钾溶液,分别加入2mL0.1mol/L草酸溶液和2mL0.2mol/L草酸溶液 | 加入0.2mol/L草酸溶液的试管中,高锰酸钾溶液褪色更快 | 反应物浓度越大,反应速率越快 |
D | 把充有NO2和N2O4的平衡球装置分别放入热水和冷水中 | 热水中颜色更深 | 其他条件不变时,温度升高,平衡向吸热反应方向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】化学平衡状态Ⅰ、Ⅱ、III的相关数据如下表:
根据以上信息判断,下列结论正确的是
| 编号 | 化学方程式 | 平衡常数 | 温度 | |
| 979K | 1173K | |||
| Ⅰ | Fe(s)+CO2(g) ⇌ FeO(s)+ CO(g) | K1 | 1.47 | 2.15 |
| Ⅱ | CO(g)+H2O(g) ⇌ CO2(g)+H2(g) | K2 | 1.62 | b |
| Ⅲ | Fe(s)+ H2O(g) ⇌ FeO(s) +H2(g) | K3 | a | 1.68 |
| A.a<b |
| B.反应Ⅱ、III均为放热反应 |
| C.升高温度平衡状态III向正反应方向移动 |
| D.增大压强,状态Ⅱ正反应速率增大,逆反应速率减小,平衡不移动 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在一可变密闭容器中发生反应:2A(g) + B(g) xC(g),达到平衡时测得 A 的浓度为 0.5 mol/L,在温度不变的条件下,将容器的容积扩大到原来的 2 倍,再次达平衡时,测得 A 的浓度为 0.2 mol/L。下列有关的判断正确的是
xC(g),达到平衡时测得 A 的浓度为 0.5 mol/L,在温度不变的条件下,将容器的容积扩大到原来的 2 倍,再次达平衡时,测得 A 的浓度为 0.2 mol/L。下列有关的判断正确的是
 xC(g),达到平衡时测得 A 的浓度为 0.5 mol/L,在温度不变的条件下,将容器的容积扩大到原来的 2 倍,再次达平衡时,测得 A 的浓度为 0.2 mol/L。下列有关的判断正确的是
xC(g),达到平衡时测得 A 的浓度为 0.5 mol/L,在温度不变的条件下,将容器的容积扩大到原来的 2 倍,再次达平衡时,测得 A 的浓度为 0.2 mol/L。下列有关的判断正确的是| A.x = 3 | B.物质 C 的体积分数减小 |
| C.平衡向正反应方向移动 | D.物质 B 的转化率降低 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】利用催化技术可将汽车尾气中的 NO和 CO转变成CO2和N2,化学方程式:2NO(g)+2CO(g)  2CO2(g)+N2(g)。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
2CO2(g)+N2(g)。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
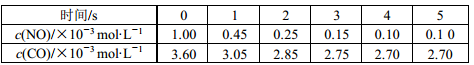
下列说法中不正确的是
 2CO2(g)+N2(g)。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
2CO2(g)+N2(g)。某温度下,在容积不变的密闭容器中通入NO和CO,测得不同时间的NO和CO的浓度如下表:
下列说法中不正确的是
| A.2 s内的平均反应速率 v(N2)=1.875×10-4 mol·L-1·s-1 |
| B.在该温度下,反应的平衡常数 K=5 |
| C.若将容积缩小为原来的一半, NO 转化率大于 90% |
| D.使用催化剂可以提高整个过程中 CO 和 NO 的处理量 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】在一体积可变的密闭容器中,加入一定量的X、Y、Z,发生反应mX(g)+nY(g) pZ(g)ΔH=QkJ·mol-1。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。
pZ(g)ΔH=QkJ·mol-1。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。
下列说法不正确的是
 pZ(g)ΔH=QkJ·mol-1。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。
pZ(g)ΔH=QkJ·mol-1。反应达到平衡后,Y的物质的量浓度与温度、容器体积的关系如下表所示。容器体积/L c(Y)/(mol·L-1) 温度/℃ | 1 | 2 | 3 |
100 | 1.00 | 0.75 | 0.53 |
200 | 1.20 | 0.90 | 0.63 |
300 | 1.30 | 1.00 | 0.70 |
| A.m+n>p |
| B.Q<0 |
| C.体积不变,温度升高,平衡向逆反应方向移动 |
| D.温度不变,压强增大,Y的质量分数增大 |
您最近一年使用:0次

 的恒容密闭容器中发生反应
的恒容密闭容器中发生反应 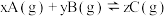 ,图Ⅰ表示
,图Ⅰ表示  时容器中
时容器中  、
、 、
、 物质的量随时间的变化,图Ⅱ表示不同温度下平衡时
物质的量随时间的变化,图Ⅱ表示不同温度下平衡时 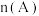 :
: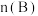 的变化关系.则下列结论正确的是
的变化关系.则下列结论正确的是
 和
和 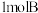 ,达到平衡时
,达到平衡时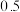
 ,且
,且 
 ,重新达到平衡前
,重新达到平衡前 
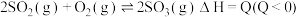 ,向同温、同体积的三个真空密闭容器中分别充入气体:
,向同温、同体积的三个真空密闭容器中分别充入气体: 甲
甲 和
和 ;
;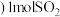 和
和 ;
;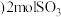 ;恒温、恒容下反应达平衡时,下列关系一定正确的是
;恒温、恒容下反应达平衡时,下列关系一定正确的是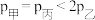
 的质量m:
的质量m:
 与
与 之比k:
之比k: