C、N、S 的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
(1)CO2的重整用 CO2和 H2为原料可得到 CH4燃料。
已知: ①CH4 (g)+CO2(g)=2CO(g)+2H2(g) △H1=+247kJ/mol
②CH4 (g)+H2O(g)=CO(g)+3H2(g) △H2=+205kJ/mol
写出 CO2重整的热化学方程式:_____ 。
(2) “亚硫酸盐法”吸收烟中的 SO2
①将烟气通入 1.0mol/L 的 Na2SO3溶液,若此过程中溶液体积不变,则溶液的 pH 不断_____ (填“减小”“不变” 或“增大)。当溶液 pH 约为 6 时,吸收 SO2的能力显著下降,应更换吸收剂,此时溶液中 c(SO32-) =0.2mol/L, 则溶液中 c(HSO3-) =_____ 。
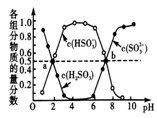
②室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液 pH 与各组分物质的量分数的变化关系如图: b 点时溶液 pH=7,则 n(NH4+):n(HSO3—)=______________ 。
(3)催化氧化法去除 NO。一定条件下,用 NH3 消除 NO 污染,其反应原理4NH3+6NO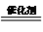 5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为 4:1、3:1、1:3 时,得到 NO 脱除率曲线如图所示:
5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为 4:1、3:1、1:3 时,得到 NO 脱除率曲线如图所示:
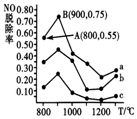
①曲线 a 中,NO 的起始浓度为6×10-4mg·m-3,从 A 点到 B 点经过0.8s,该时间段内 NO 的脱除速率为_____ mg·m-3·s-1。
②曲线 b 对应 NH3与 NO 的物质的量之比是_____ 。
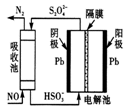
(4)间接电化学法除 NO。其原理如图所示:写出阴极的电极反应式(阴极室溶液呈酸性)_____ 。吸收池中除去 NO 的原理_____ (用离子方程式表示)。
(1)CO2的重整用 CO2和 H2为原料可得到 CH4燃料。
已知: ①CH4 (g)+CO2(g)=2CO(g)+2H2(g) △H1=+247kJ/mol
②CH4 (g)+H2O(g)=CO(g)+3H2(g) △H2=+205kJ/mol
写出 CO2重整的热化学方程式:
(2) “亚硫酸盐法”吸收烟中的 SO2
①将烟气通入 1.0mol/L 的 Na2SO3溶液,若此过程中溶液体积不变,则溶液的 pH 不断
②室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液 pH 与各组分物质的量分数的变化关系如图: b 点时溶液 pH=7,则 n(NH4+):n(HSO3—)=

(3)催化氧化法去除 NO。一定条件下,用 NH3 消除 NO 污染,其反应原理4NH3+6NO
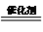 5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为 4:1、3:1、1:3 时,得到 NO 脱除率曲线如图所示:
5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为 4:1、3:1、1:3 时,得到 NO 脱除率曲线如图所示:
①曲线 a 中,NO 的起始浓度为6×10-4mg·m-3,从 A 点到 B 点经过0.8s,该时间段内 NO 的脱除速率为
②曲线 b 对应 NH3与 NO 的物质的量之比是
(4)间接电化学法除 NO。其原理如图所示:写出阴极的电极反应式(阴极室溶液呈酸性)

更新时间:2020-02-17 16:19:49
|
相似题推荐
【推荐1】六氟锑酸钠( NaSbF6)广泛用于有机合成、光化学反应中的催化剂、蚀刻剂等。一种由锑矿粉(主要含Sb2O3、Fe2O3和少量Sb2O5、Sb2S3、CuS等)合成六氟锑酸钠的工艺流程如图所示:

请回答下列问题:
(1)“碱浸、还原”时,若Sb2O5与Na2S2O3反应计量关系为2:1,则氧化产物为_______ ,Sb2S3发生反应的离子方程式为_______
(2)“除杂”时,当溶液中出现蓝色沉淀,停止加入CuSO4溶液,若此时溶液中-lgc(S2- )与pH的关系如图。

已知Ksp[Cu(OH)2]=2.0×10-20,则Ksp(CuS) =_______
(3)“转化”时控温约50°C的原因_______ ;“转化”后,检验NaSbO3·3H2O是否洗涤干净应选用的试剂为_______ 。
(4)“氟化”反应的离子方程式为_______ 。
(5)“系列操作”为蒸发浓缩、冷却结晶、过滤、洗涤、干燥,则下列仪器中需使用的有_______ (填字母标号) ,不需使用的为_______ (填名称)。
A. B.
B. C.
C. D.
D.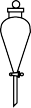 E.
E.

请回答下列问题:
(1)“碱浸、还原”时,若Sb2O5与Na2S2O3反应计量关系为2:1,则氧化产物为
(2)“除杂”时,当溶液中出现蓝色沉淀,停止加入CuSO4溶液,若此时溶液中-lgc(S2- )与pH的关系如图。

已知Ksp[Cu(OH)2]=2.0×10-20,则Ksp(CuS) =
(3)“转化”时控温约50°C的原因
(4)“氟化”反应的离子方程式为
(5)“系列操作”为蒸发浓缩、冷却结晶、过滤、洗涤、干燥,则下列仪器中需使用的有
A.
 B.
B. C.
C. D.
D.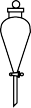 E.
E.
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】工业废水中含+6价的铬会损害环境,必须进行处理。某工厂的处理工艺流程如下:

(1)N2H4的电子式为_____ 。
(2)下列溶液中,可替代N2H4的是_____ 。(填选项序号字母)
a.FeSO4溶液 b.浓HNO3溶液 c.酸性KMnO4溶液 d.Na2SO3溶液
(3)已知加入N2H4后,N2H4转化为无污染的物质,则该反应中氧化剂与还原剂的物质的量之比为_____ 。
(4)在实际工业生产中,处理含铬废水还可采用直接沉淀的方法,其成本较低。
①已知酸性废水中存在Cr2O72-和CrO42-的转化平衡,请用离子方程式表示它们之间的转化反应_____ ;
②加入沉淀剂BaCl2溶液之前需加入一定量的NaOH溶液,以利于沉淀的生成,则生成的沉淀为_____ (写化学式)。
(5)工业上还可用电解法来处理含Cr2O72-的酸性废水,通过电解制得还原剂。右图为电解装置示意图(电极材料分别为铁和石墨)。
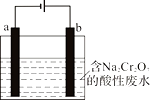
①装置中b电极的材料是_____ (填“铁”或“石墨”)。
②该处理过程中,Cr2O72-被还原成Cr3+的离子方程式为_____ 。

(1)N2H4的电子式为
(2)下列溶液中,可替代N2H4的是
a.FeSO4溶液 b.浓HNO3溶液 c.酸性KMnO4溶液 d.Na2SO3溶液
(3)已知加入N2H4后,N2H4转化为无污染的物质,则该反应中氧化剂与还原剂的物质的量之比为
(4)在实际工业生产中,处理含铬废水还可采用直接沉淀的方法,其成本较低。
①已知酸性废水中存在Cr2O72-和CrO42-的转化平衡,请用离子方程式表示它们之间的转化反应
②加入沉淀剂BaCl2溶液之前需加入一定量的NaOH溶液,以利于沉淀的生成,则生成的沉淀为
(5)工业上还可用电解法来处理含Cr2O72-的酸性废水,通过电解制得还原剂。右图为电解装置示意图(电极材料分别为铁和石墨)。

①装置中b电极的材料是
②该处理过程中,Cr2O72-被还原成Cr3+的离子方程式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】实验室制取A并进一步制取无水FeCl3的实验装置如图所示。
已知:无水FeCl3在空气中易与水发生作用,加热易升华。
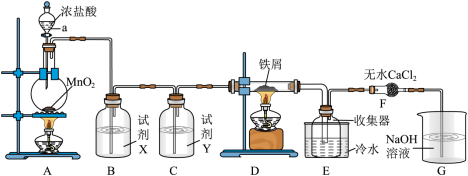
回答下列问题:
(1)仪器a的名称是_______ ,装置A所发生的氧化还原反应中,氧化剂与还原剂的物质的量之比为_______ 。
(2)试剂X是_______ 。
(3)装置F中无水CaCl2的作用是_______
(4)某温度下,将氯气通入G装置中,反应得到NaCl,NaClO和NaClO3的混合溶液,经测定ClO-与ClO 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:_______ 。
已知:无水FeCl3在空气中易与水发生作用,加热易升华。

回答下列问题:
(1)仪器a的名称是
(2)试剂X是
(3)装置F中无水CaCl2的作用是
(4)某温度下,将氯气通入G装置中,反应得到NaCl,NaClO和NaClO3的混合溶液,经测定ClO-与ClO
 的物质的量之比为4∶1,写出该反应总的离子方程式:
的物质的量之比为4∶1,写出该反应总的离子方程式:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】氨是重要的基础化工原料,可以制备亚硝酸(HNO2)、连二次硝酸(H2N2O2)、尿素[CO(NH2)2]等多种含氮的化工产品。
(1)水能发生自偶电离2H2O H3O++OH-,液氨比水更难电离,试写出液氨的自偶电离方程
H3O++OH-,液氨比水更难电离,试写出液氨的自偶电离方程___________ 。
(2)25℃时,亚硝酸和连二次硝酸的电离常数如下表所示:
①物质的量浓度相同的NaNO2和NaHN2O2溶液的pH(NaNO2)___________ pH(NaHN2O2)(填“>”、“<”或“=”)。
②25℃时NaHN2O2溶液中存在水解平衡,其水解常数Kh=___________ (保留三位有效数字)。
(3)以NH3与CO2为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
反应I:2NH3(g)+CO2(g) NH2CO2NH4(s) △H1=-159.5kJ•mol-1;
NH2CO2NH4(s) △H1=-159.5kJ•mol-1;
反应II:NH2CO2NH4(s) CO(NH2)2(s)+H2O(g) △H2=+116.5kJ•mol-1;
CO(NH2)2(s)+H2O(g) △H2=+116.5kJ•mol-1;
反应III:H2O(l)═H2O(g) △H3=+44.0kJ•mol-1。
(4)T1℃时,向容积为2L的恒容密闭容器中充入n(NH3):n(CO2)=2:l的原料气,使之发生反应Ⅳ,反应结束后得到尿素的质量为30g,容器内的压强p随时间t的变化如图1所示。
①T1℃时,该反应的平衡常数K的值为___________ 。
②图2中能正确反应平衡常数K随温度变化关系的曲线为___________ (填字母标号)。

(5)据文献报道,二氧化碳可以在酸性水溶液中用惰性电极电解制得乙烯,其原理如图3所示。则b电极上的电极反应式为___________ 。
(1)水能发生自偶电离2H2O
 H3O++OH-,液氨比水更难电离,试写出液氨的自偶电离方程
H3O++OH-,液氨比水更难电离,试写出液氨的自偶电离方程(2)25℃时,亚硝酸和连二次硝酸的电离常数如下表所示:
| 化学式 | HNO2 | H2N2O2 |
| 电离常数 | Ka=5.1×10-4 | Ka1=6.17×10-8、Ka2=2.88×10-12 |
②25℃时NaHN2O2溶液中存在水解平衡,其水解常数Kh=
(3)以NH3与CO2为原料可以合成尿素[CO(NH2)2],涉及的化学反应如下:
反应I:2NH3(g)+CO2(g)
 NH2CO2NH4(s) △H1=-159.5kJ•mol-1;
NH2CO2NH4(s) △H1=-159.5kJ•mol-1;反应II:NH2CO2NH4(s)
 CO(NH2)2(s)+H2O(g) △H2=+116.5kJ•mol-1;
CO(NH2)2(s)+H2O(g) △H2=+116.5kJ•mol-1;反应III:H2O(l)═H2O(g) △H3=+44.0kJ•mol-1。
(4)T1℃时,向容积为2L的恒容密闭容器中充入n(NH3):n(CO2)=2:l的原料气,使之发生反应Ⅳ,反应结束后得到尿素的质量为30g,容器内的压强p随时间t的变化如图1所示。
①T1℃时,该反应的平衡常数K的值为
②图2中能正确反应平衡常数K随温度变化关系的曲线为

(5)据文献报道,二氧化碳可以在酸性水溶液中用惰性电极电解制得乙烯,其原理如图3所示。则b电极上的电极反应式为
您最近一年使用:0次
【推荐2】2020年9月,习近平主席在第75届联合国大会提出我国要实现2030年前碳达峰、2060年前碳中和的目标。因此CO2的捕集、利用与封存成为科学家研究的重要课题。
I.研究表明CO2与CH4在催化剂存在下可发生反应制得合成气:CO2(g)+CH4(g)⇌2CO(g)+2H2(g) △H
(1)已知:①2CO2(g)=2CO(g)+O2(g) △H1=+566kJ·mol-l
②2H2(g)+O2(g)=2H2O(g) △H2=-484kJ·mol-l
③CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3=-802kJ·mol-l
则△H=______ kJ·mol-l。分析反应①利于该反应自发进行的条件是_______ (填“高温”或“低温”)。
(2)一定温度下,向一恒容密闭容器中充入CO2和CH4发生上述反应,初始时CO2和CH4的物质的量均为1mol,体系压强为1MPa,段时间达到平衡后,测得体系压强是起始时的1.2倍,则该反应的平衡常数Kp=___________ (MPa)2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
II.CO2和H2合成甲烷也是CO2资源化利用的重要方法。对于反应CO2(g)+4H2(g)⇌CH4+2H2O(g) △H=-165kJ·mol-l,催化剂的选择是CO2甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如下图所示:
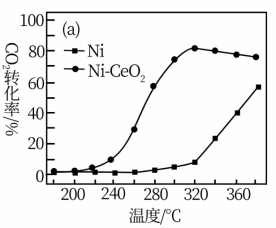

(3)高于320℃后,以Ni为催化剂,CO2转化率仍在上升,其原因是_______ 。
(4)对比上述两种催化剂的催化性能,工业上应选择的催化剂是___ ,使用的合适温度为____ 。
III.
(5)通过电化学方法可有效实现以CO2和水为原料合成甲酸,其原理示意图如下:

则A极的电极反应式为___________ 。以铅蓄电池为电源进行电解,理论上当有1molHCOOH生成时,铅蓄电池中消耗H2SO4___________ mol
I.研究表明CO2与CH4在催化剂存在下可发生反应制得合成气:CO2(g)+CH4(g)⇌2CO(g)+2H2(g) △H
(1)已知:①2CO2(g)=2CO(g)+O2(g) △H1=+566kJ·mol-l
②2H2(g)+O2(g)=2H2O(g) △H2=-484kJ·mol-l
③CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H3=-802kJ·mol-l
则△H=
(2)一定温度下,向一恒容密闭容器中充入CO2和CH4发生上述反应,初始时CO2和CH4的物质的量均为1mol,体系压强为1MPa,段时间达到平衡后,测得体系压强是起始时的1.2倍,则该反应的平衡常数Kp=
II.CO2和H2合成甲烷也是CO2资源化利用的重要方法。对于反应CO2(g)+4H2(g)⇌CH4+2H2O(g) △H=-165kJ·mol-l,催化剂的选择是CO2甲烷化技术的核心。在两种不同催化剂条件下反应相同时间,测得CO2转化率和生成CH4选择性随温度变化的影响如下图所示:


(3)高于320℃后,以Ni为催化剂,CO2转化率仍在上升,其原因是
(4)对比上述两种催化剂的催化性能,工业上应选择的催化剂是
III.
(5)通过电化学方法可有效实现以CO2和水为原料合成甲酸,其原理示意图如下:

则A极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】合成氨反应是重要的化工反应,请回答下列问题:
(1)①NH3(g)+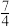 O2(g)
O2(g) NO2(g)+
NO2(g)+ H2O(g) △H=-299.6kJ·mol-1
H2O(g) △H=-299.6kJ·mol-1
②H2(g)+ O2(g)=H2O(g) △H=-241.8kJ·mol-1
O2(g)=H2O(g) △H=-241.8kJ·mol-1
③N2(g)+2O2(g)=2NO2(g) △H=+33.9kJ·mol-1
由上述反应,可求出N2(g)+3H2(g) 2NH3(g)的△H=
2NH3(g)的△H=___ 。
(2)对于反应①,在恒温恒容(H2O为气态)的容器中,下列选项表明反应已达到平衡的是___ 。
A.混合气体的平均摩尔质量不变
B.混合气体的密度不变
C.气体的颜色不再变化
D.体系内压强不再变化
E.每消耗1molNH3的同时生成1molNO2
(3)已知:N2(g)+3H2(g) 2NH3(g)反应的熵变△S=-0.081kJ·mol-1·K-1,则298K时,该反应
2NH3(g)反应的熵变△S=-0.081kJ·mol-1·K-1,则298K时,该反应___ (填“能”或“不能”)自发进行。
(4)如图为673K温度下,某合成氨塔里各气体组分压强变化图。
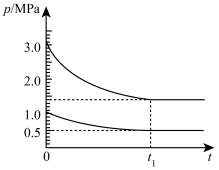
①t1平衡时,氨气的体积分数为___ %(保留位小数)。
②在图中画出氨气组分压强变化图___ 。
③该温度下N2(g)+3H2(g) 2NH3(g)反应的压力平衡常数Kp=
2NH3(g)反应的压力平衡常数Kp=___ (MPa)-2(保留1位小数,Kp为以气体分压表示反应的平衡常数)
(1)①NH3(g)+
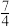 O2(g)
O2(g) NO2(g)+
NO2(g)+ H2O(g) △H=-299.6kJ·mol-1
H2O(g) △H=-299.6kJ·mol-1②H2(g)+
 O2(g)=H2O(g) △H=-241.8kJ·mol-1
O2(g)=H2O(g) △H=-241.8kJ·mol-1③N2(g)+2O2(g)=2NO2(g) △H=+33.9kJ·mol-1
由上述反应,可求出N2(g)+3H2(g)
 2NH3(g)的△H=
2NH3(g)的△H=(2)对于反应①,在恒温恒容(H2O为气态)的容器中,下列选项表明反应已达到平衡的是
A.混合气体的平均摩尔质量不变
B.混合气体的密度不变
C.气体的颜色不再变化
D.体系内压强不再变化
E.每消耗1molNH3的同时生成1molNO2
(3)已知:N2(g)+3H2(g)
 2NH3(g)反应的熵变△S=-0.081kJ·mol-1·K-1,则298K时,该反应
2NH3(g)反应的熵变△S=-0.081kJ·mol-1·K-1,则298K时,该反应(4)如图为673K温度下,某合成氨塔里各气体组分压强变化图。

①t1平衡时,氨气的体积分数为
②在图中画出氨气组分压强变化图
③该温度下N2(g)+3H2(g)
 2NH3(g)反应的压力平衡常数Kp=
2NH3(g)反应的压力平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】根据要求,回答下列问题:
Ⅰ. 是温室气体,可用
是温室气体,可用 溶液吸收得到
溶液吸收得到 或
或 。
。
(1) 水解的离子方程式为(忽略第二步水解)
水解的离子方程式为(忽略第二步水解)___________ ,其水解常数的表达式为 =
=___________ 。
(2)已知25℃时, 的
的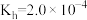 ,则当溶液中
,则当溶液中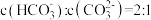 时,溶液的pH=
时,溶液的pH=___________ 。
(3)
 溶液中,
溶液中,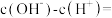
___________ [用含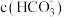 、
、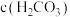 的关系式表示]。
的关系式表示]。
(4)向 溶液中加入明矾溶液,有沉淀和气体产生,反应的离子方程式为
溶液中加入明矾溶液,有沉淀和气体产生,反应的离子方程式为___________ 。
Ⅱ.工业上制取 的生产流程如下:
的生产流程如下:

25℃时, 、
、 、
、 的溶度积
的溶度积 和
和 、
、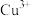 、
、 完全沉淀时的pH范围如下表所示:
完全沉淀时的pH范围如下表所示:
(5)在溶液A中加入 的目的是
的目的是___________ 。
(6)在溶液B中加入 的作用是
的作用是___________ 。
(7)操作a的目的是___________ 。
(8)在 中加入盐酸使
中加入盐酸使 转化为
转化为 ,采用稍过量盐酸和低温蒸干的目的是
,采用稍过量盐酸和低温蒸干的目的是___________ 。
Ⅰ.
 是温室气体,可用
是温室气体,可用 溶液吸收得到
溶液吸收得到 或
或 。
。(1)
 水解的离子方程式为(忽略第二步水解)
水解的离子方程式为(忽略第二步水解) =
=(2)已知25℃时,
 的
的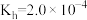 ,则当溶液中
,则当溶液中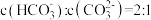 时,溶液的pH=
时,溶液的pH=(3)

 溶液中,
溶液中,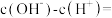
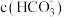 、
、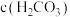 的关系式表示]。
的关系式表示]。(4)向
 溶液中加入明矾溶液,有沉淀和气体产生,反应的离子方程式为
溶液中加入明矾溶液,有沉淀和气体产生,反应的离子方程式为Ⅱ.工业上制取
 的生产流程如下:
的生产流程如下:
25℃时,
 、
、 、
、 的溶度积
的溶度积 和
和 、
、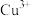 、
、 完全沉淀时的pH范围如下表所示:
完全沉淀时的pH范围如下表所示:| 物质 |  |  |  |
25℃时, |  | 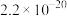 |  |
| 金属离子完全沉淀时的pH范围 | 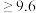 | 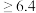 | 3~4 |
 的目的是
的目的是(6)在溶液B中加入
 的作用是
的作用是(7)操作a的目的是
(8)在
 中加入盐酸使
中加入盐酸使 转化为
转化为 ,采用稍过量盐酸和低温蒸干的目的是
,采用稍过量盐酸和低温蒸干的目的是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】磷的含氧酸有次磷酸(H3PO2)、亚磷酸(H3PO3)、磷酸(H3PO4)等多种,都是重要的化工原料。
(1)已知次磷酸(H3PO2)的水溶液中存在H3PO2分子,H3PO2与足量NaOH溶液充分反应,消耗的酸和碱的物质的量相等,反应的离子方程式为____ ,生成的盐属于____ (填“正盐”或“酸式盐”)。
(2)查阅资料知25℃时,亚磷酸(H3PO3)的Ka1=5×10-2,Ka2=2.5×10-7。25℃时,Na2HPO3水解反应的Kh=____ (填数值)。
(3)若用甲基橙做指示剂,用NaOH溶液滴定某浓度的H3PO3溶液,达到滴定终点时所得溶液中c(Na+)____ c(H2PO )+2c(HPO
)+2c(HPO )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。
(4)磷酸(H3PO4)在水溶液中各种微粒的物质的量分数δ随pH的变化曲线如图所示:
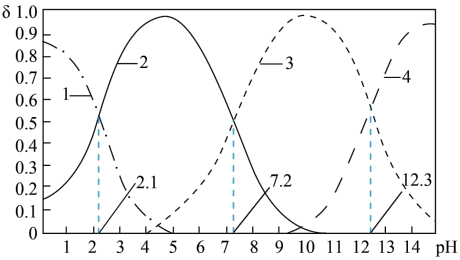
①向某浓度的磷酸溶液中滴加NaOH溶液,以酚酞为指示剂,当溶液由无色变为浅红色时,发生的主要反应的离子方程式是____ 。
②从图中推断下列说法正确的是___ 。
A.25℃时,H3PO4的第三步电离常数为10-12.3
B.Na2HPO4溶液中:c(Na+)>c(H2PO )>c(H3PO4)>c(HPO
)>c(H3PO4)>c(HPO )
)
C.Na2HPO4溶液中:c(Na+)>c(H2PO )>c(PO
)>c(PO )>c(HPO
)>c(HPO )
)
D.pH=7.2时,溶液中c(Na+)+c(H+)=3c(H2PO )+3c(PO
)+3c(PO )+c(OH-)
)+c(OH-)
(1)已知次磷酸(H3PO2)的水溶液中存在H3PO2分子,H3PO2与足量NaOH溶液充分反应,消耗的酸和碱的物质的量相等,反应的离子方程式为
(2)查阅资料知25℃时,亚磷酸(H3PO3)的Ka1=5×10-2,Ka2=2.5×10-7。25℃时,Na2HPO3水解反应的Kh=
(3)若用甲基橙做指示剂,用NaOH溶液滴定某浓度的H3PO3溶液,达到滴定终点时所得溶液中c(Na+)
 )+2c(HPO
)+2c(HPO )(填“>”、“<”或“=”)。
)(填“>”、“<”或“=”)。(4)磷酸(H3PO4)在水溶液中各种微粒的物质的量分数δ随pH的变化曲线如图所示:

①向某浓度的磷酸溶液中滴加NaOH溶液,以酚酞为指示剂,当溶液由无色变为浅红色时,发生的主要反应的离子方程式是
②从图中推断下列说法正确的是
A.25℃时,H3PO4的第三步电离常数为10-12.3
B.Na2HPO4溶液中:c(Na+)>c(H2PO
 )>c(H3PO4)>c(HPO
)>c(H3PO4)>c(HPO )
)C.Na2HPO4溶液中:c(Na+)>c(H2PO
 )>c(PO
)>c(PO )>c(HPO
)>c(HPO )
)D.pH=7.2时,溶液中c(Na+)+c(H+)=3c(H2PO
 )+3c(PO
)+3c(PO )+c(OH-)
)+c(OH-)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】 为高效漂白剂和氧化剂,可用于纸浆、纸张和各种纤维的漂白,也在环境治理中有所应用。
为高效漂白剂和氧化剂,可用于纸浆、纸张和各种纤维的漂白,也在环境治理中有所应用。
(1)已知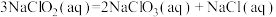
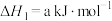
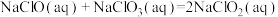
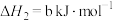
则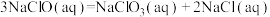

___________  (用含a、b式子表示)。
(用含a、b式子表示)。
(2)浓度均为0.1
 和
和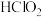 混合溶液呈酸性,则溶液中微粒浓度大小关系:
混合溶液呈酸性,则溶液中微粒浓度大小关系: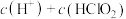
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)工业上可用电解法制备 ,其工作原理如图所示(NaCl足量),电解一段时间后,将Pt(A)电极区的溶液除去微量二氧化氯后,喷雾干燥即得
,其工作原理如图所示(NaCl足量),电解一段时间后,将Pt(A)电极区的溶液除去微量二氧化氯后,喷雾干燥即得 粗品。
粗品。

M处是外接直流电源的___________ 极(填“正”或“负”);离子交换膜应选择___________ (填“阴”或“阳”)离子交换膜;当外电路转移0.1mol电子时,理论上Pt(B)电极区电解质溶液质量减少___________ g。
(4)以 为氧化剂是一种新型脱除NO方法,其原理为:
为氧化剂是一种新型脱除NO方法,其原理为:
第一步:NO在碱性环境中被氧化为 ,反应为:
,反应为: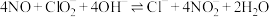 ;
;
第二步: 继续被氧化为
继续被氧化为 ,反应为:
,反应为: 。
。
① 溶液吸收NO的过程中,适当增加压强,对NO的脱除率的影响是
溶液吸收NO的过程中,适当增加压强,对NO的脱除率的影响是___________ (填“提高”“无影响”或“降低”)。
②在50℃时,将NO匀速通过足量浓度为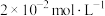
 碱性溶液,3min后,测得溶液中
碱性溶液,3min后,测得溶液中 浓度为
浓度为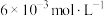 。则该时间段内平均反应速率
。则该时间段内平均反应速率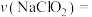
___________ (反应前后溶液的体积变化忽略不计)。
 为高效漂白剂和氧化剂,可用于纸浆、纸张和各种纤维的漂白,也在环境治理中有所应用。
为高效漂白剂和氧化剂,可用于纸浆、纸张和各种纤维的漂白,也在环境治理中有所应用。(1)已知
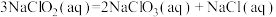
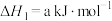
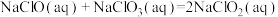
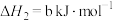
则
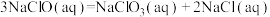

 (用含a、b式子表示)。
(用含a、b式子表示)。(2)浓度均为0.1

 和
和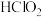 混合溶液呈酸性,则溶液中微粒浓度大小关系:
混合溶液呈酸性,则溶液中微粒浓度大小关系: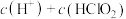
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)工业上可用电解法制备
 ,其工作原理如图所示(NaCl足量),电解一段时间后,将Pt(A)电极区的溶液除去微量二氧化氯后,喷雾干燥即得
,其工作原理如图所示(NaCl足量),电解一段时间后,将Pt(A)电极区的溶液除去微量二氧化氯后,喷雾干燥即得 粗品。
粗品。
M处是外接直流电源的
(4)以
 为氧化剂是一种新型脱除NO方法,其原理为:
为氧化剂是一种新型脱除NO方法,其原理为:第一步:NO在碱性环境中被氧化为
 ,反应为:
,反应为: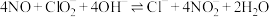 ;
;第二步:
 继续被氧化为
继续被氧化为 ,反应为:
,反应为: 。
。①
 溶液吸收NO的过程中,适当增加压强,对NO的脱除率的影响是
溶液吸收NO的过程中,适当增加压强,对NO的脱除率的影响是②在50℃时,将NO匀速通过足量浓度为
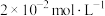
 碱性溶液,3min后,测得溶液中
碱性溶液,3min后,测得溶液中 浓度为
浓度为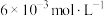 。则该时间段内平均反应速率
。则该时间段内平均反应速率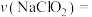
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】“碳中和“理念中碳捕获、碳利用、碳封存技术能实现二氧化碳资源化,产生经济效益。
I.图1是利用太阳能将CO2分解制取炭黑的示意图。
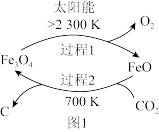
已知①C(s)+O2(g)=CO2(g) ΔH=a kJ·mol-1;
②6FeO(s) +CO2(g)=2Fe3O4(s)+C(s) ΔH=bkJ·mol-1
(1)则过程1的热化学方程式为_______ 。
Ⅱ.二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域。
(2)在体系压强为0.1MPa,初始原料按组成n(CO2):n(H2)=1:3投料,发生反应2CO2(g) + 6H2(g) C2H4(g)+4H2O(g)。达到平衡时,四种组分的物质的量分数x随温度T的变化如图2所示。
C2H4(g)+4H2O(g)。达到平衡时,四种组分的物质的量分数x随温度T的变化如图2所示。

①图2中表示C2H4变化的曲线是_______ 。CO2催化加氢合成C2H4反应的反应热△H_______ 0(填“>”或“<”)。其他条件相同,在不同催化剂(A、B)作用下,它们正、逆反应活化能的差值分别用EA、EB表示,则EA_______ EB(填“大于”“小于”或“等于”)。
②A点氢气的转化率是_______ 。B点的化学平衡常数_______ (填“>”“<”或“=”)C点。
(3)如图3所示是反应2CO2(g) +6H2(g) C2H4(g)+4H2O(g)的平衡移动图象,影响平衡移动的原因是_______(填字母)。
C2H4(g)+4H2O(g)的平衡移动图象,影响平衡移动的原因是_______(填字母)。

(4)一定温度下,反应2CO2(g) +6H2(g)  C2H4(g)+4H2O(g)在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在t1时刻达到平衡状态的是
C2H4(g)+4H2O(g)在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在t1时刻达到平衡状态的是_______ (填字母)。

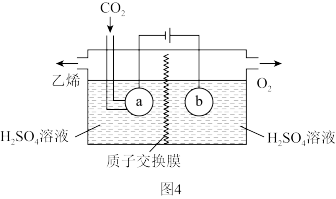
(5)如图4所示,电解法可制取乙烯,阴极的电极反应式为_______ 。当外电路通过1.2mole- 时,电解池右侧电解质溶液减少_______ g。
I.图1是利用太阳能将CO2分解制取炭黑的示意图。

已知①C(s)+O2(g)=CO2(g) ΔH=a kJ·mol-1;
②6FeO(s) +CO2(g)=2Fe3O4(s)+C(s) ΔH=bkJ·mol-1
(1)则过程1的热化学方程式为
Ⅱ.二氧化碳催化加氢合成乙烯是综合利用CO2的热点研究领域。
(2)在体系压强为0.1MPa,初始原料按组成n(CO2):n(H2)=1:3投料,发生反应2CO2(g) + 6H2(g)
 C2H4(g)+4H2O(g)。达到平衡时,四种组分的物质的量分数x随温度T的变化如图2所示。
C2H4(g)+4H2O(g)。达到平衡时,四种组分的物质的量分数x随温度T的变化如图2所示。
①图2中表示C2H4变化的曲线是
②A点氢气的转化率是
(3)如图3所示是反应2CO2(g) +6H2(g)
 C2H4(g)+4H2O(g)的平衡移动图象,影响平衡移动的原因是_______(填字母)。
C2H4(g)+4H2O(g)的平衡移动图象,影响平衡移动的原因是_______(填字母)。
| A.升高温度,同时加压 |
| B.降低温度,同时减压 |
| C.增大反应物浓度,同时减小生成物浓度 |
| D.增大反应物浓度,同时使用催化剂 |
 C2H4(g)+4H2O(g)在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在t1时刻达到平衡状态的是
C2H4(g)+4H2O(g)在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在t1时刻达到平衡状态的是
(5)如图4所示,电解法可制取乙烯,阴极的电极反应式为

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】某工厂以粗硅藻土 主要成分是
主要成分是 和有机质,并含有少量的
和有机质,并含有少量的 、
、 等杂质
等杂质 ,生产精制硅藻土并获得
,生产精制硅藻土并获得 及高铁酸钾
及高铁酸钾 的工艺流程如下:
的工艺流程如下:
(1)粗硅藻土在煅烧过程中,为了加快反应速率可以采取的措施有___________  写两条
写两条 。
。
(2)查阅资料得知:常温下 、
、 在浓度为
在浓度为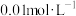 时,氢氧化物沉淀的
时,氢氧化物沉淀的 如下表:
如下表:
要使 与
与 分离,应调节溶液的
分离,应调节溶液的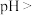
___________ ;根据表中数据,该温度下
___________ 。
(3)滤液 中通入过量
中通入过量 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)滤渣 与
与 溶液、
溶液、 反应的化学方程式为
反应的化学方程式为___________ ;在该反应中每生成 ,转移的电子数为
,转移的电子数为___________ 。
(5)工业可利用电解法制取高铁酸钾 ,装置示意图如下:
,装置示意图如下: 在电解时,镍电极接电源的
在电解时,镍电极接电源的___________ 极 填“正”或“负”
填“正”或“负” 。
。
 在电解过程中,阳极的电极反应式为
在电解过程中,阳极的电极反应式为___________ ;阴极区溶液的
___________ (填“增大”“减少”或“不变” 。
。
 主要成分是
主要成分是 和有机质,并含有少量的
和有机质,并含有少量的 、
、 等杂质
等杂质 ,生产精制硅藻土并获得
,生产精制硅藻土并获得 及高铁酸钾
及高铁酸钾 的工艺流程如下:
的工艺流程如下: 
(1)粗硅藻土在煅烧过程中,为了加快反应速率可以采取的措施有
 写两条
写两条 。
。(2)查阅资料得知:常温下
 、
、 在浓度为
在浓度为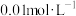 时,氢氧化物沉淀的
时,氢氧化物沉淀的 如下表:
如下表:| 氢氧化物 |  |  |  在 在 时开始溶解, 时开始溶解, 完全溶解 完全溶解 |
开始沉淀的 |  | 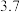 | |
完全沉淀的 |  | 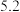 |
 与
与 分离,应调节溶液的
分离,应调节溶液的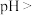

(3)滤液
 中通入过量
中通入过量 发生反应的离子方程式为
发生反应的离子方程式为(4)滤渣
 与
与 溶液、
溶液、 反应的化学方程式为
反应的化学方程式为 ,转移的电子数为
,转移的电子数为(5)工业可利用电解法制取高铁酸钾
 ,装置示意图如下:
,装置示意图如下:
 在电解时,镍电极接电源的
在电解时,镍电极接电源的 填“正”或“负”
填“正”或“负” 。
。 在电解过程中,阳极的电极反应式为
在电解过程中,阳极的电极反应式为
 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】从砷化镓废料(主要成分为 ,含
,含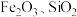 和
和 等杂质)中回收镓和砷的工艺流程如下:
等杂质)中回收镓和砷的工艺流程如下:

已知:① 是两性氢氧化物。
是两性氢氧化物。
②25℃时, 的溶度积
的溶度积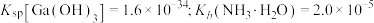 。
。
回答下列问题:
(1)“浆化”是将砷化镓废料转变成悬浊液的过程,其目的是_______ 。
(2)砷化镓(GaAs)在“碱浸”时,砷化镓转化为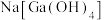 和
和 进入溶液,该反应的化学方程式为
进入溶液,该反应的化学方程式为_______ 。
(3)“碱浸”的温度控制在70℃左右,温度不宜过高或过低的原因是_______ ;“滤渣2”的成分为_______ (填化学式)。
(4)向“中和”后得到的滤液中加入足量的 溶液,使
溶液,使 大于12,经
大于12,经_______ ,降温结晶、过滤、洗涤、低温干燥后得到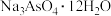 。
。
(5)“旋流电解”时用惰性电极,则所得“尾液”的主要溶质是_______ (填化学式),可进行循环利用,提高经济效益。
(6)为了探究 在氨水中能否溶解,计算反应
在氨水中能否溶解,计算反应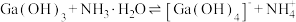 的平衡常数
的平衡常数
_______ (已知: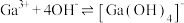
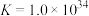 )
)
 ,含
,含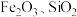 和
和 等杂质)中回收镓和砷的工艺流程如下:
等杂质)中回收镓和砷的工艺流程如下:
已知:①
 是两性氢氧化物。
是两性氢氧化物。②25℃时,
 的溶度积
的溶度积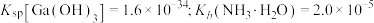 。
。回答下列问题:
(1)“浆化”是将砷化镓废料转变成悬浊液的过程,其目的是
(2)砷化镓(GaAs)在“碱浸”时,砷化镓转化为
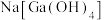 和
和 进入溶液,该反应的化学方程式为
进入溶液,该反应的化学方程式为(3)“碱浸”的温度控制在70℃左右,温度不宜过高或过低的原因是
(4)向“中和”后得到的滤液中加入足量的
 溶液,使
溶液,使 大于12,经
大于12,经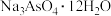 。
。(5)“旋流电解”时用惰性电极,则所得“尾液”的主要溶质是
(6)为了探究
 在氨水中能否溶解,计算反应
在氨水中能否溶解,计算反应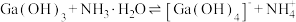 的平衡常数
的平衡常数
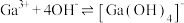
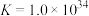 )
)
您最近一年使用:0次



