1 . 两个容积均为2L的密闭容器I和II中充入NO和CO气体,发生反应: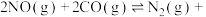
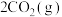 △H,各物质的起始物质的量见下表。实验测得两容器在不同温度下达到平衡时
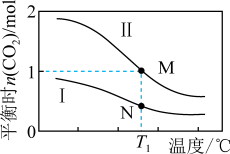
△H,各物质的起始物质的量见下表。实验测得两容器在不同温度下达到平衡时 的物质的量如图所示。下列说法正确的是
的物质的量如图所示。下列说法正确的是
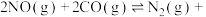
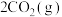 △H,各物质的起始物质的量见下表。实验测得两容器在不同温度下达到平衡时
△H,各物质的起始物质的量见下表。实验测得两容器在不同温度下达到平衡时 的物质的量如图所示。下列说法正确的是
的物质的量如图所示。下列说法正确的是
| 容器 | 起始物质的量 | |
| NO | CO | |
| I | 1mol | 3mol |
| II | 6mol | 2mol |
| A.M、N两点容器内的压强:P(M)<2P(N) |
| B.N点的平衡常数为0.08 |
C.若将容器I的容积改为1L, 温度下达到平衡时NO的转化率为25% 温度下达到平衡时NO的转化率为25% |
D.图中M点所示条件下,再通入CO、 各2mol,此时v(正)>v(逆) 各2mol,此时v(正)>v(逆) |
您最近半年使用:0次
2022-11-06更新
|
354次组卷
|
2卷引用:湖南省长沙市雅礼中学2022-2023学年高二上学期期中考试化学试题
2 . 某温度下2 L密闭容器中,3种气体起始状态和平衡状态时的物质的量(n)如下表所示。下列说法正确的是
| X | Y | W | |
| n(起始状态)/mol | 2 | 1 | 0 |
| n(平衡状态)/mol | 1 | 0.5 | 1.5 |
| A.该温度下,此反应的平衡常数K=6.75 |
| B.升高温度,若W的体积分数减小,则此反应ΔH<0 |
| C.增大压强,正、逆反应速率均增大,平衡向正反应方向移动 |
D.该温度下,此反应的平衡常数表达式是K= 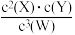 |
您最近半年使用:0次
名校
解题方法
3 . 温度为T1时,在三个容积均为1L的恒容密闭容器中发生反应:2NO2(g) 2NO(g)+O2(g)(正反应吸热)。验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)c(O2),k正、k逆为速率常数。下列说法正确的是
2NO(g)+O2(g)(正反应吸热)。验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)c(O2),k正、k逆为速率常数。下列说法正确的是
 2NO(g)+O2(g)(正反应吸热)。验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)c(O2),k正、k逆为速率常数。下列说法正确的是
2NO(g)+O2(g)(正反应吸热)。验测得:v正=v(NO2)消耗=k正c2(NO2),v逆=v(NO)消耗=2v(O2)消耗=k逆c2(NO)c(O2),k正、k逆为速率常数。下列说法正确的是| 容器编号 | 物质的起始浓度(mol•L-1) | 物质的平衡浓度(mol•L-1) | ||
| c(NO2) | c(NO) | c(O2) | ||
| I | 0.6 | 0 | 0 | 0.2 |
| II | 0.2 | 0.5 | 0.2 | |
| III | 0 | 0.5 | 0.35 | |
| A.达平衡时,容器I与容器II中的总压强之比为8:9 |
B.达平衡时,容器II中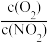 比容器I中的大 比容器I中的大 |
| C.达平衡时,容器III中NO的体积分数大于50% |
| D.当温度改变为T2时,若k正>k逆,则T2>T1 |
您最近半年使用:0次
名校
解题方法
4 . 丙烯是一种重要的有机化工原料,工业上以丁烯、乙烯为原料制取丙烯的反应如下: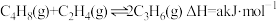 ,一定温度下,向体积为
,一定温度下,向体积为 密闭容器中充入
密闭容器中充入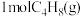 和
和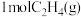 ,测得
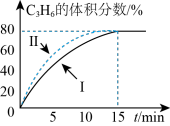
,测得 的体积分数随时间的变化如图中线Ⅰ所示。
的体积分数随时间的变化如图中线Ⅰ所示。
已知几种气体的燃烧热如下表所示
下列说法正确的是
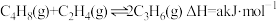 ,一定温度下,向体积为
,一定温度下,向体积为 密闭容器中充入
密闭容器中充入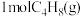 和
和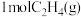 ,测得
,测得 的体积分数随时间的变化如图中线Ⅰ所示。
的体积分数随时间的变化如图中线Ⅰ所示。
已知几种气体的燃烧热如下表所示
| 气体 |  | 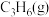 |  |
燃烧热/ / / | 1411 | 2049 | 2539 |
A. 燃烧的热化学方程式可表示为 燃烧的热化学方程式可表示为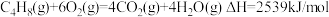 |
B.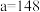 |
| C.该温度下反应的平衡常数为64 |
| D.图中线II可能是其他条件一定,反应在更高温度时进行 |
您最近半年使用:0次
22-23高二上·全国·课时练习
解题方法
5 . 将2molA和1molB充入某密闭容器中发生反应:2A(g)+B(g) xC(g),达到化学平衡后,C的体积分数为a(假设该反应的条件分别和下列各选项的条件相同),下列判断正确的是
xC(g),达到化学平衡后,C的体积分数为a(假设该反应的条件分别和下列各选项的条件相同),下列判断正确的是
 xC(g),达到化学平衡后,C的体积分数为a(假设该反应的条件分别和下列各选项的条件相同),下列判断正确的是
xC(g),达到化学平衡后,C的体积分数为a(假设该反应的条件分别和下列各选项的条件相同),下列判断正确的是A.若在恒温恒压下,当x=1时,按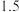 molA、1molC作为起始物质,达到平衡后,C的体积分数仍为a molA、1molC作为起始物质,达到平衡后,C的体积分数仍为a |
| B.若在恒温恒容下,当x=2时,将2molC作起始物质,达到平衡后,C的体积分数仍为a |
| C.若在恒温恒压下,当x=3时,1mol A、1molB、6molC作起始物质,达到平衡后,C的体积分数仍为a |
| D.若在恒温恒容下,按0.6molA、0.3molB、1.4molC作起始物质,达到平衡后,C的体积分数仍为a,则x一定为2或3 |
您最近半年使用:0次
名校
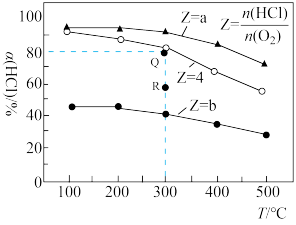
6 . 有Ⅰ~Ⅳ四个体积均为1L的恒容密闭容器,在Ⅰ、Ⅱ、Ⅲ中按不同投料比(Z)充入HCl和 (如表),加入催化剂发生反应:4HCl(g)+O2(g)
(如表),加入催化剂发生反应:4HCl(g)+O2(g)  2Cl2(g)+2H2O(g)ΔH,HCl的平衡转化率(
2Cl2(g)+2H2O(g)ΔH,HCl的平衡转化率( )与Z和温度(T)的关系如图所示。下列说法正确的是
)与Z和温度(T)的关系如图所示。下列说法正确的是
 (如表),加入催化剂发生反应:4HCl(g)+O2(g)
(如表),加入催化剂发生反应:4HCl(g)+O2(g)  2Cl2(g)+2H2O(g)ΔH,HCl的平衡转化率(
2Cl2(g)+2H2O(g)ΔH,HCl的平衡转化率( )与Z和温度(T)的关系如图所示。下列说法正确的是
)与Z和温度(T)的关系如图所示。下列说法正确的是| 容器 | 起始时 | ||
| T/℃ | n(HCl)/mol | Z | |
| Ⅰ | 300 | 0.5 |  |
| Ⅱ | 300 | 0.5 | 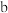 |
| Ⅲ | 300 | 0.5 | 4 |

| A.ΔH<0,b>4>a |
B.容器Ⅲ某时刻处在R点,则R点的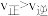 ,压强:p(R)>p(Q) ,压强:p(R)>p(Q) |
| C.300℃该反应的平衡常数的值为160 |
D.起始时,在容器Ⅳ中充入0.5mol 和0.5mol 和0.5mol (g),300℃达平衡时容器中 (g),300℃达平衡时容器中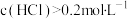 |
您最近半年使用:0次
7 . 一定条件下,分别向体积为1L的密闭容器中充入气体,发生反应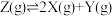 ,测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
,测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
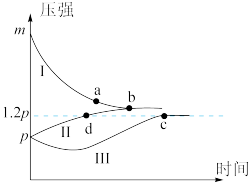
 ,测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
,测得实验①、②、③反应过程中体系压强随时间的变化曲线如图所示。下列说法正确的是
| 实验 | 充入气体量 | 反应过程条件 |
| ① | 2mol X+1mol Y | 恒温 |
| ② | 1molZ | 恒温 |
| ③ | 1molZ | 绝热 |
A.曲线Ⅰ对应实验①,且 | B.Z的转化率:b<c |
C.气体的总物质的量: | D.b点平衡常数: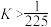 |
您最近半年使用:0次
2022-10-11更新
|
543次组卷
|
3卷引用:山东德州市普通高中2022-2023学年高三上学期10月过程性检测化学试题
名校
解题方法
8 . 甲烷重整制合成气,体系中主要反应如下:
I.CH4(g)+H2O(g) CO(g)+3H2(g) ΔH1
CO(g)+3H2(g) ΔH1
Ⅱ.CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH2
2CO(g)+2H2(g) ΔH2
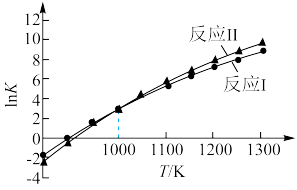
各反应平衡常数与温度的关系如图所示,下列说法正确的是
I.CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH1
CO(g)+3H2(g) ΔH1Ⅱ.CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH2
2CO(g)+2H2(g) ΔH2各反应平衡常数与温度的关系如图所示,下列说法正确的是

| A.体系温度高于1000K时,升温对反应I的平衡影响更大 |
| B.理论上,反应Ⅱ在低温下可自发进行 |
C.1000K时,反应CO2(g)+H2(g)  CO(g)+H2O(g)的平衡常数K=1 CO(g)+H2O(g)的平衡常数K=1 |
D.1000K时,若平衡时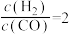 ,则 ,则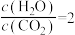 ,应控制起始投料比 ,应控制起始投料比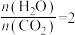 |
您最近半年使用:0次
2022-09-27更新
|
1118次组卷
|
7卷引用:湖南省永州市2023届高考第一次适应性考试化学试题
湖南省永州市2023届高考第一次适应性考试化学试题湖南省宁远县第一中学2022-2023学年高二上学期第一次适应性考试化学试题(已下线)热点情景汇编-专题七 化学反应速率与平衡(已下线)专题17 化学平衡图表分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题15 化学平衡图像-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)河南省周口恒大中学2022-2023学年高二上学期1月期末考试化学试题河南省周口市2022-2023学年恒大中学高二(上)期末化学试卷
名校
解题方法
9 . 由合成气(CO和H2)通过如下反应可制得甲醇:2H2(g)+CO(g) CH3OH(g) ΔH<0。400K时,向体积为0.1L的密闭容器中充入0.02molH2和0.01molCO,在催化剂作用下充分反应,tmin时反应达到平衡,CO的物质的量为0.002mol。下列说法正确的是
CH3OH(g) ΔH<0。400K时,向体积为0.1L的密闭容器中充入0.02molH2和0.01molCO,在催化剂作用下充分反应,tmin时反应达到平衡,CO的物质的量为0.002mol。下列说法正确的是
 CH3OH(g) ΔH<0。400K时,向体积为0.1L的密闭容器中充入0.02molH2和0.01molCO,在催化剂作用下充分反应,tmin时反应达到平衡,CO的物质的量为0.002mol。下列说法正确的是
CH3OH(g) ΔH<0。400K时,向体积为0.1L的密闭容器中充入0.02molH2和0.01molCO,在催化剂作用下充分反应,tmin时反应达到平衡,CO的物质的量为0.002mol。下列说法正确的是| A.反应的ΔS>0 |
| B.当容器中气体密度不再发生变化时,反应达到平衡 |
| C.温度为400K时,反应的平衡常数K=2500 |
| D.其他条件不变,若起始时向容器中充入0.008molH2、0.004molCO和0.016molCH3OH,此时v(正)>v(逆) |
您最近半年使用:0次
2022-09-23更新
|
295次组卷
|
2卷引用:江苏省如皋中学2022-2023学年高三上学期8月综合测试化学试题
解题方法
10 . 
在催化剂作用下主要发生反应: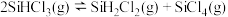 △H=+48kJ•mol-1。已知:反应速率
△H=+48kJ•mol-1。已知:反应速率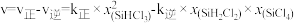 ,
, 、
、 分别为正、逆反应速率常数,x为物质的量分数,向两个容积相等的恒容密闭容器中分别充入等量
分别为正、逆反应速率常数,x为物质的量分数,向两个容积相等的恒容密闭容器中分别充入等量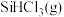 ,在323K和343K时
,在323K和343K时 的转化率随时间变化的结果如图所示。
的转化率随时间变化的结果如图所示。
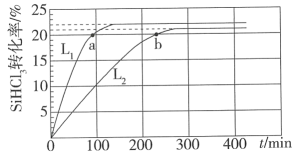
下列说法正确的是

在催化剂作用下主要发生反应:
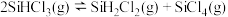 △H=+48kJ•mol-1。已知:反应速率
△H=+48kJ•mol-1。已知:反应速率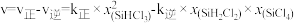 ,
, 、
、 分别为正、逆反应速率常数,x为物质的量分数,向两个容积相等的恒容密闭容器中分别充入等量
分别为正、逆反应速率常数,x为物质的量分数,向两个容积相等的恒容密闭容器中分别充入等量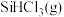 ,在323K和343K时
,在323K和343K时 的转化率随时间变化的结果如图所示。
的转化率随时间变化的结果如图所示。
下列说法正确的是
| A.a点的反应速率大于b点的反应速率 |
| B.343K时反应物的平衡转化率为21% |
C.343K时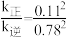 |
D.由323K时 的平衡转化率数据,不能计算323K的平衡常数K 的平衡转化率数据,不能计算323K的平衡常数K |
您最近半年使用:0次



