名校
解题方法
1 . 农药波尔多液的主要成份是 ,下列两个反应都有
,下列两个反应都有 生成。
生成。
①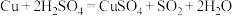 ②
②
请回答下列问题:
(1)从分类角度来看 属于
属于_______ , 属于
属于_______ 。(填序号)
A.氧化物 B.盐 C.碱 D.酸
(2)上述两个反应属于氧化还原反应的是_______ ,其中氧化剂是_______ ,氧化产物是_______ 。
(3)反应①的副产物 是大气污染物,可用
是大气污染物,可用 溶液吸收,该反应的化学方程式是
溶液吸收,该反应的化学方程式是_______ 。
 ,下列两个反应都有
,下列两个反应都有 生成。
生成。①
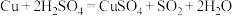 ②
②
请回答下列问题:
(1)从分类角度来看
 属于
属于 属于
属于A.氧化物 B.盐 C.碱 D.酸
(2)上述两个反应属于氧化还原反应的是
(3)反应①的副产物
 是大气污染物,可用
是大气污染物,可用 溶液吸收,该反应的化学方程式是
溶液吸收,该反应的化学方程式是
您最近一年使用:0次
名校
2 . “7•20特大洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效措施之一。“84”消毒液、漂白粉和 等都是有效的消杀试剂。
等都是有效的消杀试剂。
(1)用化学方程式表示氯气与烧碱溶液制备“84”消毒液的原理______ ,标况下56L氯气完全被吸收,需要______ L 1mol/L的NaOH溶液。
(2)使用漂白粉漂白,只需取适量漂白粉溶于水即可,漂白原理用化学方程式表示为______ 。
(3)漂白粉的保存要注意密封,为了判断一份儿久置的漂白粉是①没有失效②部分失效③完全失效。某化学兴趣小组设计实验进行验证。
已知: 溶液呈碱性;
溶液呈碱性; ;
;
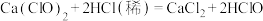
a.甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此,判断结论为①,乙同学不同意这一观点,你认为的结论是______ 。
A.② B.③ C.①或② D.①②③均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。据此你得出的结论是______ (从①②③中选填)。
(4)目前普遍使用 代替
代替 及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。
及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。 还可以将剧毒的NaCN转化为无毒物质除去,产物是氯化钠和两种常见气体。试写出该反应的化学方程式
还可以将剧毒的NaCN转化为无毒物质除去,产物是氯化钠和两种常见气体。试写出该反应的化学方程式______ 。
 等都是有效的消杀试剂。
等都是有效的消杀试剂。(1)用化学方程式表示氯气与烧碱溶液制备“84”消毒液的原理
(2)使用漂白粉漂白,只需取适量漂白粉溶于水即可,漂白原理用化学方程式表示为
(3)漂白粉的保存要注意密封,为了判断一份儿久置的漂白粉是①没有失效②部分失效③完全失效。某化学兴趣小组设计实验进行验证。
已知:
 溶液呈碱性;
溶液呈碱性; ;
;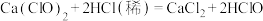
a.甲同学取适量漂白粉样品,滴加浓盐酸,将产生的气体直接通入澄清石灰水中,没有发现石灰水变浑浊。由此,判断结论为①,乙同学不同意这一观点,你认为的结论是
A.② B.③ C.①或② D.①②③均有可能
b.乙同学改用滴加稀盐酸,发现产生大量气泡,将气体通入澄清石灰水中,石灰水变浑浊;他又取少量漂白粉样品配成溶液,滴在pH试纸上,最终试纸变白。据此你得出的结论是
(4)目前普遍使用
 代替
代替 及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。
及次氯酸盐作为广谱抗菌消毒剂,因为它安全、低毒,高效。 还可以将剧毒的NaCN转化为无毒物质除去,产物是氯化钠和两种常见气体。试写出该反应的化学方程式
还可以将剧毒的NaCN转化为无毒物质除去,产物是氯化钠和两种常见气体。试写出该反应的化学方程式
您最近一年使用:0次
2023-01-07更新
|
138次组卷
|
2卷引用:吉林省长春市第五中学2022-2023学年高一上学期期末考试化学试题
3 . 根据①~④四个反应,回答下列问题:
①Cl2+2KI=2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2FeCl3+2HI=2FeCl2+2HCl+I2
④H2S+I2=S+2HI
(1)反应①的反应类型为___ (填序号)。
A.置换反应 B.复分解反应 C.化合反应 D.氧化还原反应
(2)根据上述四个反应可判断出Cl2、I2、Fe3+、H2S四种物质的氧化性强弱顺序为____ 。
(3)亚硝酸钠(NaNO2)有毒,一次摄入量超过3g可导致死亡。
Ⅰ.实验室中,亚硝酸钠也被用于处理过量的叠氮化钠,有关反应方程式如下:
NaNO2+H2SO4=HNO2+NaHSO4 a
2NaN3+2HNO2=3N2↑+2NO↑+2NaOH b
①上述两个反应中属于非氧化还原反应的是___ (选填字母“a”或“b")。
②其中的氧化还原反应的氧化剂是___ (写化学式),该反应的还原产物与氧化产物的质量之比为___ 。
Ⅱ.亚硝酸钠外观与食盐相似,均有咸味。某学校实验探究小组欲对亚硝酸钠与氯化钠进行鉴别,下列是他们的鉴别方法:
将样品盐放入稀硫酸与另外一种溶液(溶质为X)的混合液中,振荡,再加淀粉。如果溶液显蓝色则可以证明该样品盐是亚硝酸钠,如果溶液无变化,则可以证明该样品盐为氯化钠。X与亚硝酸钠发生的反应可以用下列化学方程式表示:2NaNO2+2X+2H2SO4=2NO↑+I2+K2SO4+Na2SO4+2H2O
写出X的化学式并用双线桥法标出电子转移的方向和数目___ ,___ 。
①Cl2+2KI=2KCl+I2
②2FeCl2+Cl2=2FeCl3
③2FeCl3+2HI=2FeCl2+2HCl+I2
④H2S+I2=S+2HI
(1)反应①的反应类型为
A.置换反应 B.复分解反应 C.化合反应 D.氧化还原反应
(2)根据上述四个反应可判断出Cl2、I2、Fe3+、H2S四种物质的氧化性强弱顺序为
(3)亚硝酸钠(NaNO2)有毒,一次摄入量超过3g可导致死亡。
Ⅰ.实验室中,亚硝酸钠也被用于处理过量的叠氮化钠,有关反应方程式如下:
NaNO2+H2SO4=HNO2+NaHSO4 a
2NaN3+2HNO2=3N2↑+2NO↑+2NaOH b
①上述两个反应中属于非氧化还原反应的是
②其中的氧化还原反应的氧化剂是
Ⅱ.亚硝酸钠外观与食盐相似,均有咸味。某学校实验探究小组欲对亚硝酸钠与氯化钠进行鉴别,下列是他们的鉴别方法:
将样品盐放入稀硫酸与另外一种溶液(溶质为X)的混合液中,振荡,再加淀粉。如果溶液显蓝色则可以证明该样品盐是亚硝酸钠,如果溶液无变化,则可以证明该样品盐为氯化钠。X与亚硝酸钠发生的反应可以用下列化学方程式表示:2NaNO2+2X+2H2SO4=2NO↑+I2+K2SO4+Na2SO4+2H2O
写出X的化学式并用双线桥法标出电子转移的方向和数目
您最近一年使用:0次
2014高三·全国·专题练习
名校
4 . 2013年中国水周的主题是:“节约保护水资源,大力建设生态文明”.
(1)ClO2和Cl2(还原产物都为Cl﹣)是生活中常用的净水消毒剂.当消耗等物质的量的两种物质时,ClO2的消毒效率是Cl2的_________ 倍.
(2)某无色废水中可能含有Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作流程和有关现象如图所示:操作③的相关图象如图
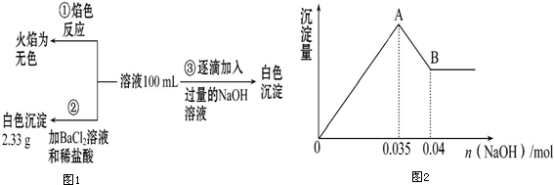
请根据上图回答下列问题:
①实验中需配制1.0mol•L﹣1的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为_______________ .
②实验③中沉淀量由A→B过程中所发生反应的离子方程式为___________ .
③试确定NO3-是否存在?________ (填“存在”“不存在”或“不确定”),若存在,试计算c(NO3-)=_____ (若不存在,此问不必作答).
(1)ClO2和Cl2(还原产物都为Cl﹣)是生活中常用的净水消毒剂.当消耗等物质的量的两种物质时,ClO2的消毒效率是Cl2的
(2)某无色废水中可能含有Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作流程和有关现象如图所示:操作③的相关图象如图

请根据上图回答下列问题:
①实验中需配制1.0mol•L﹣1的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为
②实验③中沉淀量由A→B过程中所发生反应的离子方程式为
③试确定NO3-是否存在?
您最近一年使用:0次
2016-12-09更新
|
267次组卷
|
5卷引用:吉林省长春市第五中学2021届高三上学期期中考试化学试题
吉林省长春市第五中学2021届高三上学期期中考试化学试题(已下线)2014届高考化学二轮专题冲刺第3讲 离子反应氧化还原反应练习卷2016届山东省枣庄市滕州五中高三上学期期末化学试卷新疆乌什县阿克托海乡中学2019届高三年级四月调研考试理综化学试题湖北省石首市第一中学2019-2020学年高三上学期8月月考化学试题



