1 . 中国高铁被誉为中国新“四大发明”之一,它对实现“一带一路”的构想有重要的作用。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是黏土和___________ 。
(2)高铁车厢的大部分材料是铝合金,是利用了铝合金材料___________ (填2种)等优点。
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式为___________ 。
(4)高铁洗手间中有一瓶“84”消毒液。
①在“84”消毒液中滴加几滴酚酞试液,可观察到的现象是___________ 。
②“84”消毒液必须避光密封保存,目的是防止与空气中的二氧化碳反应而变质,用化学方程式解释其原因:a.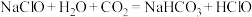 ;b.
;b.___________ 。
③“84”消毒液还可作为水处理剂除去水中的杂质离子。例如过量次氯酸钠可使酸性废水中的 完全转化为
完全转化为 ,该反应中氧化剂与氧化产物的物质的量之比为
,该反应中氧化剂与氧化产物的物质的量之比为___________ 。
(1)建设高铁轨道需要大量的水泥,生产水泥的主要原材料是黏土和
(2)高铁车厢的大部分材料是铝合金,是利用了铝合金材料
(3)高铁上安装有许多玻璃,氢氟酸可以处理玻璃表面的微裂纹,氢氟酸与玻璃中的二氧化硅反应的化学方程式为
(4)高铁洗手间中有一瓶“84”消毒液。
①在“84”消毒液中滴加几滴酚酞试液,可观察到的现象是
②“84”消毒液必须避光密封保存,目的是防止与空气中的二氧化碳反应而变质,用化学方程式解释其原因:a.
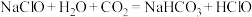 ;b.
;b.③“84”消毒液还可作为水处理剂除去水中的杂质离子。例如过量次氯酸钠可使酸性废水中的
 完全转化为
完全转化为 ,该反应中氧化剂与氧化产物的物质的量之比为
,该反应中氧化剂与氧化产物的物质的量之比为
您最近一年使用:0次
2023-09-17更新
|
170次组卷
|
2卷引用:新疆生产建设兵团第二师八一中学2022-2023学年高三上学期11月月考化学试题
名校
2 . 对下列内容进行填空。
(1)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是___________ 。
(2)两个相同容积的密闭容器X、Y,在25℃下,X中充入ag A气体,Y中充入ag CH4气体,X与Y内的压强之比是4:11,则A的摩尔质量为___________ 。
(3)某固体A在一定条件下加热分解,产物都是气体。分解的方程式为2A =B↑ + 2C↑ + 2D↑。测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为___________ 。
(4)现有24 mL 浓度为0.1 mol/L Na2SO3溶液恰好与20 mL 浓度为0.04 mol/L KRO4 溶液完全转化为Na2SO4,则R元素在产物中的化合价是___________ 。
(5)碳酸钠样品中可能含有氢氧化钠、碳酸钙、生石灰、氯化钠、硫酸铜五种杂质中的三种。现进行下列实验:①称取4.7g样品,加入足量水,样品部分溶解;②向①中所得悬浊液中加入100 mL 1 mol / L HCl ,最终得到无色澄清溶液,此过程中共产生0.04 mol气体;③向②中反应后的溶液中加入足量的硝酸银与稀硝酸,得到15.8 g白色沉淀。由此可知杂质中一定含有___________ (填写化学式)。
(1)在一定的温度和压强下,1体积气体X2跟3体积气体Y2化合生成2体积化合物,则该化合物的化学式是
(2)两个相同容积的密闭容器X、Y,在25℃下,X中充入ag A气体,Y中充入ag CH4气体,X与Y内的压强之比是4:11,则A的摩尔质量为
(3)某固体A在一定条件下加热分解,产物都是气体。分解的方程式为2A =B↑ + 2C↑ + 2D↑。测得生成的混合气体对氢气的相对密度为d,则A的相对分子质量为
(4)现有24 mL 浓度为0.1 mol/L Na2SO3溶液恰好与20 mL 浓度为0.04 mol/L KRO4 溶液完全转化为Na2SO4,则R元素在产物中的化合价是
(5)碳酸钠样品中可能含有氢氧化钠、碳酸钙、生石灰、氯化钠、硫酸铜五种杂质中的三种。现进行下列实验:①称取4.7g样品,加入足量水,样品部分溶解;②向①中所得悬浊液中加入100 mL 1 mol / L HCl ,最终得到无色澄清溶液,此过程中共产生0.04 mol气体;③向②中反应后的溶液中加入足量的硝酸银与稀硝酸,得到15.8 g白色沉淀。由此可知杂质中一定含有
您最近一年使用:0次
名校
解题方法
3 . 实验室可用如下方法制取Cl2:
①MnO2 +4HCl(浓) Cl2↑+ MnCl2+ 2H2O
Cl2↑+ MnCl2+ 2H2O
②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
根据相关信息,回答下列问题:
(1)在反应①中,HCl表现的性质有______ 、________ 。
(2)若反应①中有0.1mol的氧化剂被还原,则被氧化的物质的物质的量为____ 。
(3)将(2)生成的氯气与0.2mol H2完全反应,将产物溶于水配成100mL溶液,此溶液的物质的量浓度为_______ 。
(4)若要制得相同质量的氯气,①②③三个反应中电子转移的数目之比为____ 。
(5)已知反应4HCl(g)+O2 2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为_______ 。
(6)将不纯的NaOH样品2.50 g(样品含少量Na2CO3和水),放入50.0 mL 2.00mol/L盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40.0 mL 1.00 mol/L的NaOH溶液。蒸发中和后的溶液,最终得到固体的质量为_______ 。
①MnO2 +4HCl(浓)
 Cl2↑+ MnCl2+ 2H2O
Cl2↑+ MnCl2+ 2H2O ②KClO3+6HCl(浓)=3Cl2↑+KCl+3H2O
③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
根据相关信息,回答下列问题:
(1)在反应①中,HCl表现的性质有
(2)若反应①中有0.1mol的氧化剂被还原,则被氧化的物质的物质的量为
(3)将(2)生成的氯气与0.2mol H2完全反应,将产物溶于水配成100mL溶液,此溶液的物质的量浓度为
(4)若要制得相同质量的氯气,①②③三个反应中电子转移的数目之比为
(5)已知反应4HCl(g)+O2
 2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为
2Cl2+2H2O(g),该反应也能制得氯气,则MnO2、O2、KMnO4三种物质氧化性由强到弱的顺序为(6)将不纯的NaOH样品2.50 g(样品含少量Na2CO3和水),放入50.0 mL 2.00mol/L盐酸中,充分反应后,溶液呈酸性,中和多余的酸又用去40.0 mL 1.00 mol/L的NaOH溶液。蒸发中和后的溶液,最终得到固体的质量为
您最近一年使用:0次
2014高三·全国·专题练习
名校
4 . 2013年中国水周的主题是:“节约保护水资源,大力建设生态文明”.
(1)ClO2和Cl2(还原产物都为Cl﹣)是生活中常用的净水消毒剂.当消耗等物质的量的两种物质时,ClO2的消毒效率是Cl2的_________ 倍.
(2)某无色废水中可能含有Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作流程和有关现象如图所示:操作③的相关图象如图
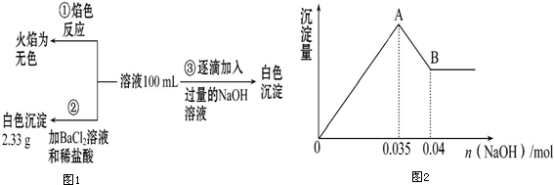
请根据上图回答下列问题:
①实验中需配制1.0mol•L﹣1的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为_______________ .
②实验③中沉淀量由A→B过程中所发生反应的离子方程式为___________ .
③试确定NO3-是否存在?________ (填“存在”“不存在”或“不确定”),若存在,试计算c(NO3-)=_____ (若不存在,此问不必作答).
(1)ClO2和Cl2(还原产物都为Cl﹣)是生活中常用的净水消毒剂.当消耗等物质的量的两种物质时,ClO2的消毒效率是Cl2的
(2)某无色废水中可能含有Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100mL,进行了三组实验,其操作流程和有关现象如图所示:操作③的相关图象如图

请根据上图回答下列问题:
①实验中需配制1.0mol•L﹣1的NaOH溶液100mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管,还缺少的仪器为
②实验③中沉淀量由A→B过程中所发生反应的离子方程式为
③试确定NO3-是否存在?
您最近一年使用:0次
2016-12-09更新
|
267次组卷
|
5卷引用:新疆乌什县阿克托海乡中学2019届高三年级四月调研考试理综化学试题
新疆乌什县阿克托海乡中学2019届高三年级四月调研考试理综化学试题(已下线)2014届高考化学二轮专题冲刺第3讲 离子反应氧化还原反应练习卷2016届山东省枣庄市滕州五中高三上学期期末化学试卷吉林省长春市第五中学2021届高三上学期期中考试化学试题湖北省石首市第一中学2019-2020学年高三上学期8月月考化学试题



