1 . 下列有关物质结构与性质的说法错误的是
A. 比 比 稳定,是由于 稳定,是由于 分子间存在氢键,而 分子间存在氢键,而 分子间不存在氢键 分子间不存在氢键 |
| B.Zn的第一电离能大于Ga,是由于Zn的价层电子排布是全充满的,比较稳定 |
C. 溶于氨水,是由于 溶于氨水,是由于 与 与 反应生成了可溶性配合物 反应生成了可溶性配合物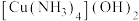 |
| D.金刚石可用作地质钻探钻头,是由于金刚石具有很高的硬度 |
您最近半年使用:0次
2 . 磷化氢(PH3)具有能量密度高、可再生优势,常用作新能源材料。一种工业上利用副产法制备PH3的流程如图所示:
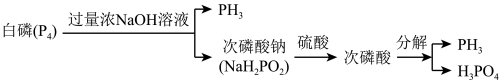
| A.白磷(P4)属于共价晶体 |
| B.次磷酸钠是酸式盐 |
| C.白磷与浓NaOH溶液反应,氧化剂与还原剂的物质的量之比为1:3 |
| D.流程中的每一步反应均属于氧化还原反应 |
您最近半年使用:0次
名校
3 .  是原子序数依次增大的短周期主族元素。基态
是原子序数依次增大的短周期主族元素。基态 原子核外电子有3种空间运动状态;
原子核外电子有3种空间运动状态; 是自然界中形成化合物最多的元素;
是自然界中形成化合物最多的元素; 的简单氢化物与其最高价氧化物对应水化物可发生反应;与
的简单氢化物与其最高价氧化物对应水化物可发生反应;与 同周期的元素中,第一电离能大于
同周期的元素中,第一电离能大于 的有三种;
的有三种; 与
与 同主族。下列说法正确的是
同主族。下列说法正确的是
 是原子序数依次增大的短周期主族元素。基态
是原子序数依次增大的短周期主族元素。基态 原子核外电子有3种空间运动状态;
原子核外电子有3种空间运动状态; 是自然界中形成化合物最多的元素;
是自然界中形成化合物最多的元素; 的简单氢化物与其最高价氧化物对应水化物可发生反应;与
的简单氢化物与其最高价氧化物对应水化物可发生反应;与 同周期的元素中,第一电离能大于
同周期的元素中,第一电离能大于 的有三种;
的有三种; 与
与 同主族。下列说法正确的是
同主族。下列说法正确的是| A.P元素形成的单质在常温下为固态,属于分子晶体 |
B.化合物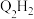 中, 中, 键与 键与 键的数目之比为 键的数目之比为 |
C. 最高价氧化物对应的水化物可与氨水发生复分解反应 最高价氧化物对应的水化物可与氨水发生复分解反应 |
D.简单离子半径: |
您最近半年使用:0次
4 . 氮化硼是一种重要的无机非金属材料,在工业生产中有着重要的作用。常见的三种氮化硼晶体结构如下图:
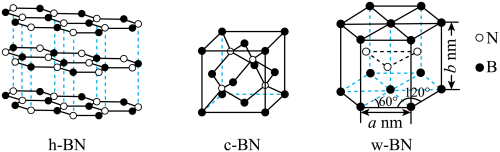
A.h-BN晶体中存在大 键 键 |
| B.c-BN晶体中由B、N构成最小的环为6元环 |
| C.w-BN晶体中B的配位数为12 |
D.w-BN晶体的密度可表示为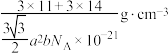 |
您最近半年使用:0次
7日内更新
|
155次组卷
|
2卷引用:河北省张家口市尚义县第一中学等校2023-2024学年高三下学期4月模拟测试化学试题
名校
解题方法
5 . X、Y、Z、M和Q是五种前四周期元素,原子序数依次增大,基态X原子核外电子有3种空间运动状态,基态Z原子的价电子排布式为 ,M与Y同族,基态Q原子有4个未成对电子,下列说法正确的是
,M与Y同族,基态Q原子有4个未成对电子,下列说法正确的是
 ,M与Y同族,基态Q原子有4个未成对电子,下列说法正确的是
,M与Y同族,基态Q原子有4个未成对电子,下列说法正确的是A.Z分别和X、M都能形成 稳定结构的共价晶体 稳定结构的共价晶体 |
B.X、Z形成简单氢化物时,中心原子均为 杂化 杂化 |
| C.同周期元素中,第一电离能介于X和Z之间的元素有2种 |
| D.金属材料中常掺杂Q元素来增强耐磨性和抗腐蚀能力 |
您最近半年使用:0次
6 . 金刚石有重要的应用,科学家不断研究制备金刚石的方法。
方法Ⅰ:C(石墨) C(金刚石)
C(金刚石) 
方法Ⅱ: (金刚石)
(金刚石)
下列说法正确的是
方法Ⅰ:C(石墨)
 C(金刚石)
C(金刚石) 
方法Ⅱ:
 (金刚石)
(金刚石)下列说法正确的是
| A.金刚石和石墨互称为同位素 |
| B.金刚石和石墨中粒子间的作用力类型相同 |
| C.键长:Si-C键<C-C键(金刚石) |
| D.熔点:SiC<C(金刚石) |
您最近半年使用:0次
名校
7 . 下列各组数据比较中,前者等于后者两倍的是
选项 | 比较的数据 |
A | 键能: 键与 键与 键 键 |
B |  晶体: 晶体: 的配位数与 的配位数与 的配位数 的配位数 |
C | 未成对电子数:基态氧原子与基态碳原子 |
D |
|
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
8 . 下列类比或推理结果正确的是
A.已知 和浓硫酸可发生归中反应,则 和浓硫酸可发生归中反应,则 和硝酸也可发生归中反应 和硝酸也可发生归中反应 |
B.已知加热时Cu与 反应生成 反应生成 ,则加热时Cu与S反应生成 ,则加热时Cu与S反应生成 |
C.已知C、Si形成的氧化物晶体类型不同,可推知等物质的量的 和 和 中σ键数目不相同 中σ键数目不相同 |
D.已知氧化性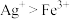 ,根据溶液中 ,根据溶液中 和 和 易发生氧化还原反应,推断溶液中 易发生氧化还原反应,推断溶液中 和 和 也易发生氧化还原反应 也易发生氧化还原反应 |
您最近半年使用:0次
名校
9 . 下列说法中正确的有
①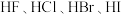 的熔沸点依次升高
的熔沸点依次升高
② 的热稳定性依次减弱
的热稳定性依次减弱
③硬度由大到小:金刚石>碳化硅>晶体硅
④分子晶体的熔点一定比金属晶体的低
⑤水结成冰,密度减小,与水分子之间能形成氢键有关
⑥金属晶体的导电性、导热性,均与自由电子有关
①
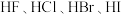 的熔沸点依次升高
的熔沸点依次升高②
 的热稳定性依次减弱
的热稳定性依次减弱③硬度由大到小:金刚石>碳化硅>晶体硅
④分子晶体的熔点一定比金属晶体的低
⑤水结成冰,密度减小,与水分子之间能形成氢键有关
⑥金属晶体的导电性、导热性,均与自由电子有关
| A.②③⑤⑥ | B.①②③⑥ | C.②③④⑤ | D.①②⑤⑥ |
您最近半年使用:0次
解题方法
10 . 化合物 有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:
有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:
(1)Ca2+的焰色试验呈砖红色,金属元素能产生焰色试验的微观原因为____________ 。
(2)与Ni同周期且基态原子最外层电子数相同的Zn元素位于元素周期表的________ 区。
(3)Fe能与CO、 等形成配合物,如
等形成配合物,如 (结构如图1)、
(结构如图1)、 (结构如图2),其中1mol
(结构如图2),其中1mol  中含有
中含有________ mol配位原子, 中含有
中含有 键与
键与 键的数目之比为
键的数目之比为_________ 。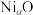 晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为
晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为 、
、 ,则晶体中
,则晶体中 与
与 的最简整数比为
的最简整数比为________ 。
(5)P与As同主族,磷化硼(BP,结构如图3)是一种超硬耐磨涂层材料,磷化硼晶体属于_________ (填“共价”“离子”或“分子”)晶体,_________ (填“是”或“否”)含有配位键,晶体中P原子的配位数为__________ 。 ,配位数为6的晶体有两种:X和Y。化学式为
,配位数为6的晶体有两种:X和Y。化学式为 的X呈绿色,定量实验表明,1mol X恰好与2mol
的X呈绿色,定量实验表明,1mol X恰好与2mol  反应生成沉淀。Y呈紫色,且1molY恰好与3mol
反应生成沉淀。Y呈紫色,且1molY恰好与3mol  反应生成沉淀,则Y的化学式为
反应生成沉淀,则Y的化学式为___________ 。
 有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:
有助于更好地理解磁性与非常规超导性之间的联系。回答下列问题:(1)Ca2+的焰色试验呈砖红色,金属元素能产生焰色试验的微观原因为
(2)与Ni同周期且基态原子最外层电子数相同的Zn元素位于元素周期表的
(3)Fe能与CO、
 等形成配合物,如
等形成配合物,如 (结构如图1)、
(结构如图1)、 (结构如图2),其中1mol
(结构如图2),其中1mol  中含有
中含有 中含有
中含有 键与
键与 键的数目之比为
键的数目之比为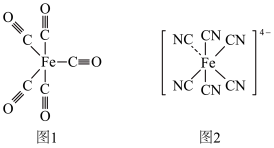
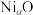 晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为
晶体结构为NaCl型,由于晶体存在缺陷,a的值为0.88,且晶体中的Ni分别为 、
、 ,则晶体中
,则晶体中 与
与 的最简整数比为
的最简整数比为(5)P与As同主族,磷化硼(BP,结构如图3)是一种超硬耐磨涂层材料,磷化硼晶体属于

 ,配位数为6的晶体有两种:X和Y。化学式为
,配位数为6的晶体有两种:X和Y。化学式为 的X呈绿色,定量实验表明,1mol X恰好与2mol
的X呈绿色,定量实验表明,1mol X恰好与2mol  反应生成沉淀。Y呈紫色,且1molY恰好与3mol
反应生成沉淀。Y呈紫色,且1molY恰好与3mol  反应生成沉淀,则Y的化学式为
反应生成沉淀,则Y的化学式为
您最近半年使用:0次

 :
: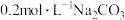 溶液与
溶液与 溶液
溶液

