解题方法
1 . 钠在氯气中燃烧生成氯化钠。下列说法不正确的是

| A.金属钠中含有Na+和自由电子 |
| B.Cl2分子中的共价键是p﹣pσ键 |
| C.氯化钠晶胞中含有14个Cl﹣和13个Na+ |
| D.熔点:NaCl>Na>Cl2 |
您最近一年使用:0次
解题方法
2 . 分子的结构与物质性质之间存在紧密的联系。
(1)如图是部分主族元素氢化物的沸点变化趋势_______ ,其汽化过程中克服的作用力是 _______ 。
②氢化物b、c、d的沸点均高于同族其它元素氢化物的沸点,原因是_______ 。
③H2O的沸点高于HF,预测可能的原因是_______ 。
(2)如图是冰(H2O)和干冰(CO2)的结构模型。_______ (填字母序号)。
a.冰中氢键存在方向性,晶体有较大空隙,空间利用率低
b.水分子极性强,分子间作用力大
c.二氧化碳分子的质量大于水分子
d.干冰晶胞中二氧化碳分子堆积得更密集
(3)苯胺(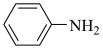 )与甲苯(
)与甲苯(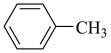 )的相对分子质量接近,但苯胺的熔点(﹣6.2℃)和沸点(184.4℃)高于甲苯的熔点(﹣95.0℃)和沸点(110.6℃),原因是
)的相对分子质量接近,但苯胺的熔点(﹣6.2℃)和沸点(184.4℃)高于甲苯的熔点(﹣95.0℃)和沸点(110.6℃),原因是 _______ 。
(1)如图是部分主族元素氢化物的沸点变化趋势
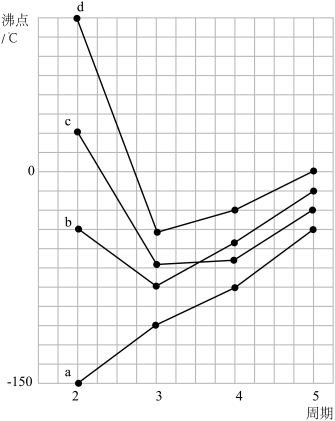
②氢化物b、c、d的沸点均高于同族其它元素氢化物的沸点,原因是
③H2O的沸点高于HF,预测可能的原因是
(2)如图是冰(H2O)和干冰(CO2)的结构模型。
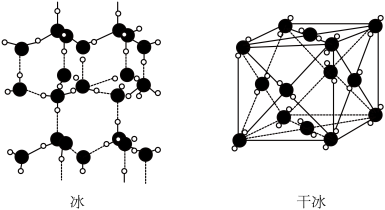
a.冰中氢键存在方向性,晶体有较大空隙,空间利用率低
b.水分子极性强,分子间作用力大
c.二氧化碳分子的质量大于水分子
d.干冰晶胞中二氧化碳分子堆积得更密集
(3)苯胺(
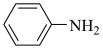 )与甲苯(
)与甲苯( )的相对分子质量接近,但苯胺的熔点(﹣6.2℃)和沸点(184.4℃)高于甲苯的熔点(﹣95.0℃)和沸点(110.6℃),原因是
)的相对分子质量接近,但苯胺的熔点(﹣6.2℃)和沸点(184.4℃)高于甲苯的熔点(﹣95.0℃)和沸点(110.6℃),原因是
您最近一年使用:0次
解题方法
3 . 将钴酞菁和三氯化铝复合嵌接在碳纳米管上,可制得一种高效催化剂。
(1)碳的几种单质如图所示。___________ 。
②下列说法正确的是_____ 。
a.金刚石中碳碳原子间是σ键
b.C60熔化时破坏的作用力是共价键
c.以上四种单质均能导电
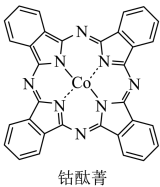
(2)钴酞菁是配位化合物,其分子结构如图所示。____________ 。
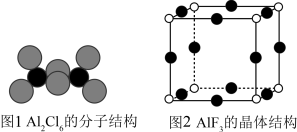
(3)气态AlCl3通常以二聚体Al2Cl6的形式存在,其空间结构如图1所示。AlF3结构属立方晶系,晶胞如图2所示。________ 。
②AlCl3的熔点为192℃,远低于AlF3的熔点1090℃的原因是_____________ 。
③AlF3晶体距离F最近的阳离子有_____ 个。
④AlF3的晶胞形状为正方体,边长为anm,该晶体密度为_____________ g•cm﹣3。(列出计算式,阿伏加德罗常数用NA表示,1nm=10﹣7cm)
(1)碳的几种单质如图所示。
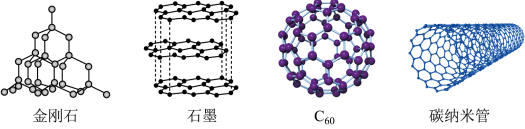
②下列说法正确的是
a.金刚石中碳碳原子间是σ键
b.C60熔化时破坏的作用力是共价键
c.以上四种单质均能导电
(2)钴酞菁是配位化合物,其分子结构如图所示。
(3)气态AlCl3通常以二聚体Al2Cl6的形式存在,其空间结构如图1所示。AlF3结构属立方晶系,晶胞如图2所示。
②AlCl3的熔点为192℃,远低于AlF3的熔点1090℃的原因是
③AlF3晶体距离F最近的阳离子有
④AlF3的晶胞形状为正方体,边长为anm,该晶体密度为
您最近一年使用:0次
4 . 下列物质中,存在手性碳原子的是
| A.CH4 |
| B.CH3﹣CH2﹣OH |
C.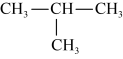 |
D.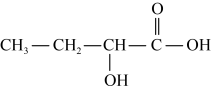 |
您最近一年使用:0次
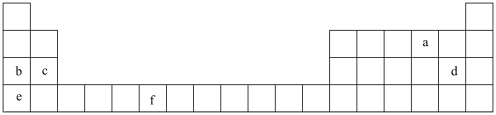
5 . 原子结构、元素性质、元素在周期表中的位置之间存在密切的相互关系。如图是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
(1)a的原子结构示意图为___________ 。
(2)基态b原子核外电子占据的最高能级符号为_______ ,该能级的电子云轮廓图形状为 _______ 形。
(3)元素c位于周期表的_____ 区。
(4)元素b、d、e中电负性最大的是_______ (用元素符号表示)。
(5)基态f原子的价层电子排布式为___________ 。
(6)气态c原子失去核外不同电子所需能量如下:
①元素c的最高化合价为 _______ 。
②c原子的逐级电离能越来越大的原因是__________ 。
(1)a的原子结构示意图为
(2)基态b原子核外电子占据的最高能级符号为
(3)元素c位于周期表的
(4)元素b、d、e中电负性最大的是
(5)基态f原子的价层电子排布式为
(6)气态c原子失去核外不同电子所需能量如下:
| 电离能 | I1(第一电离能) | I2(第二电离能) | I3(第三电离能) |
| 能量/kJ•mol﹣1 | 737.7 | 1450.7 | 7732.7 |
②c原子的逐级电离能越来越大的原因是
您最近一年使用:0次
6 . 现有下列几种常见物质:①N2、②CO2、③NaCl、④H2O、⑤Cu。
(1)含有π键的是_______ (填序号,下同);
(2)含有非极性键的是_____ ;
(3)含有离子键的是_____ ;
(4)含有金属键的是_____ ;
(5)H2O中O原子杂化轨道类型是________ ,分子的空间结构为 _______ ,H﹣O﹣H键角 _____ (填“>”“=”或“<”)109°28',属于 _______ (“极性”或“非极性”)分子。
(1)含有π键的是
(2)含有非极性键的是
(3)含有离子键的是
(4)含有金属键的是
(5)H2O中O原子杂化轨道类型是
您最近一年使用:0次
解题方法
7 . 下列关于物质的结构或性质以及解释均正确的是
| 选项 | 物质的结构或性质 | 解释 |
| A | 键角:NH3>BF3 | NH3中N的孤电子对数比BF3中B的孤电子对数多 |
| B | 酸性:CF3COOH>CCl3COOH | F的电负性大于Cl的电负性,使CF3COOH中羧基上的氢更易电离 |
| C | 熔点:碳化硅>金刚石 | C﹣Si键能大于C﹣C键能 |
| D | 稳定性:H2O>CH4 | H2O分子之间除了范德华力以外还存在氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
8 . 一种可吸附甲醇的材料,其化学式为[C(NH2)3]4[B(OCH3)4]3Cl,部分晶体结构如图所示,其中[C(NH2)3]+为平面结构。

| A.元素的电负性:C<N<O |
| B.该化合物中阴阳离子个数比为1:1 |
| C.该晶体中存在N﹣H…O氢键 |
| D.[C(NH2)3]+中C原子的杂化类型是sp3 |
您最近一年使用:0次
解题方法
9 . 钛酸钙是一种典型的钙钛矿型半导体材料,其晶胞结构如图所示。下列关于钛酸钙说法不正确的是

| A.每个晶胞中含有3个O2﹣ |
| B.化学式为CaTiO3 |
| C.含有离子键 |
| D.晶体具有良好的导电性和延展性 |
您最近一年使用:0次
解题方法
10 . 下列微粒的空间结构是平面三角形的是
| A.CO2 | B.H2S | C.CH2O | D. |
您最近一年使用:0次



