名校
1 . 综合利用废弃物,对资源利用和环境保护具有现实意义。以废铁屑(含少量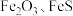 等杂质)为原料,制备硫酸亚铁晶体(
等杂质)为原料,制备硫酸亚铁晶体( ),流程示意图如下。
),流程示意图如下。
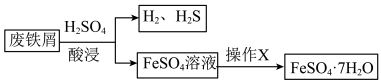
(1)酸浸过程中, 的作用是
的作用是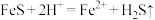 、
、 、
、___________ (用离子方程式表示)。
(2)酸浸时间对所得溶液的成分影响如下表所示。
①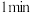 时检验,溶液变红,写出离子方程式
时检验,溶液变红,写出离子方程式___________
② 时检验,用离子方程式表示溶液未变红的原因
时检验,用离子方程式表示溶液未变红的原因___________ 。
③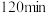 时检验,溶液复又变红,用文字说明原因
时检验,溶液复又变红,用文字说明原因___________ 。
(3)已知: 受热易失水。操作X为:
受热易失水。操作X为: ___________ 。
(4)测定所得硫酸亚铁晶体中 的含量,步骤如下:
的含量,步骤如下:
Ⅰ.称取 硫酸亚铁晶体样品,配制成
硫酸亚铁晶体样品,配制成 溶液。
溶液。
Ⅱ.取出 溶液,加入适量稀硫酸,滴入
溶液,加入适量稀硫酸,滴入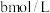 的
的 溶液,至反应完全共消耗
溶液,至反应完全共消耗 溶液
溶液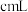 。
。
①依题意完善Ⅱ中 氧化
氧化 的离子方程式
的离子方程式________

 ___________
___________
 ___________
___________
②计算硫酸亚铁晶体样品中 的质量分数
的质量分数___________ 。
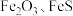 等杂质)为原料,制备硫酸亚铁晶体(
等杂质)为原料,制备硫酸亚铁晶体( ),流程示意图如下。
),流程示意图如下。
(1)酸浸过程中,
 的作用是
的作用是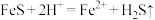 、
、 、
、(2)酸浸时间对所得溶液的成分影响如下表所示。
| 酸浸时间 | 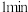 |  |  |
用 溶液检验 溶液检验 | 变红 | 未变红 | 变红 |
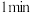 时检验,溶液变红,写出离子方程式
时检验,溶液变红,写出离子方程式②
 时检验,用离子方程式表示溶液未变红的原因
时检验,用离子方程式表示溶液未变红的原因③
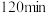 时检验,溶液复又变红,用文字说明原因
时检验,溶液复又变红,用文字说明原因(3)已知:
 受热易失水。操作X为:
受热易失水。操作X为: (4)测定所得硫酸亚铁晶体中
 的含量,步骤如下:
的含量,步骤如下:Ⅰ.称取
 硫酸亚铁晶体样品,配制成
硫酸亚铁晶体样品,配制成 溶液。
溶液。Ⅱ.取出
 溶液,加入适量稀硫酸,滴入
溶液,加入适量稀硫酸,滴入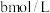 的
的 溶液,至反应完全共消耗
溶液,至反应完全共消耗 溶液
溶液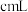 。
。①依题意完善Ⅱ中
 氧化
氧化 的离子方程式
的离子方程式
 ___________
___________
 ___________
___________②计算硫酸亚铁晶体样品中
 的质量分数
的质量分数
您最近一年使用:0次
2024-03-27更新
|
225次组卷
|
4卷引用:河北省沧州市泊头市第一中学2023-2024学年高一下学期3月月考化学试题
名校
2 . 钙元素以多种形式广泛存在于自然界中,鸡蛋壳中钙的存在形式为CaCO3。为测定鸡蛋壳中钙的含量,课外小组做如下实验:
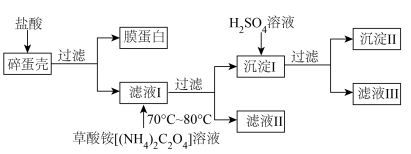
回答下列问题。
(1)滤液I与草酸铵反应采用水浴加热的优点是_______ 。
(2)为保证实验精确度,判断沉淀I是否洗涤干净的方法是_______ 。
(3)向沉淀 中加入
中加入 溶液,反应的离子方程式为
溶液,反应的离子方程式为_______ 。
(4)用 标准溶液滴定滤液III的过程中,
标准溶液滴定滤液III的过程中, (VII)被还原为
(VII)被还原为 (II),C(III)被氧化为
(II),C(III)被氧化为 。现将滤液III稀释至
。现将滤液III稀释至 ,再取其中的
,再取其中的 溶液,用
溶液,用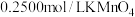 标准溶液滴定。
标准溶液滴定。
①以上操作过程中一定需要下列哪些仪器:_______ (填字母)。
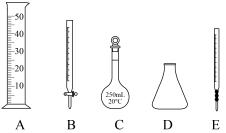
②达到滴定终点时,溶液的颜色变化是_______ 。
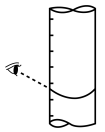
③滴定到终点,静置后如图读取KMnO4标准溶液的体积数值,则测定钙元素含量将_______ (填“偏高”“偏低”或“无影响”)。
④若实验测得数据如下表,蛋壳中含钙的质量分数为_______ (保留两位小数)。
(5)如果采用由碳酸钙直接转化为草酸钙进行测定,25℃时,向20mL碳酸钙的饱和溶液中逐滴加入cmol/L的草酸铵溶液20mL,若有草酸钙沉淀生成,则c的取值范围为_______ (草酸钙的Ksp=4.0×10-8,碳酸钙的Ksp=2.5×10-9)。

回答下列问题。
(1)滤液I与草酸铵反应采用水浴加热的优点是
(2)为保证实验精确度,判断沉淀I是否洗涤干净的方法是
(3)向沉淀
 中加入
中加入 溶液,反应的离子方程式为
溶液,反应的离子方程式为(4)用
 标准溶液滴定滤液III的过程中,
标准溶液滴定滤液III的过程中, (VII)被还原为
(VII)被还原为 (II),C(III)被氧化为
(II),C(III)被氧化为 。现将滤液III稀释至
。现将滤液III稀释至 ,再取其中的
,再取其中的 溶液,用
溶液,用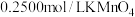 标准溶液滴定。
标准溶液滴定。①以上操作过程中一定需要下列哪些仪器:

②达到滴定终点时,溶液的颜色变化是
③滴定到终点,静置后如图读取KMnO4标准溶液的体积数值,则测定钙元素含量将

④若实验测得数据如下表,蛋壳中含钙的质量分数为
| 编号 | 1 | 2 | 3 |
| 蛋壳质量/g | 10.19 | 11.12 | 11.13 |
| KMnO4溶液/mL | 15.28 | 16.72 | 17.72 |
(5)如果采用由碳酸钙直接转化为草酸钙进行测定,25℃时,向20mL碳酸钙的饱和溶液中逐滴加入cmol/L的草酸铵溶液20mL,若有草酸钙沉淀生成,则c的取值范围为
您最近一年使用:0次
2023-11-26更新
|
213次组卷
|
5卷引用:河北省承德市双滦区实验中学2023-2024学年高三上学期一轮复习联考(三) 化学试题
河北省承德市双滦区实验中学2023-2024学年高三上学期一轮复习联考(三) 化学试题 河北省沧州市泊头市第一中学2023-2024学年高二上学期12月月考化学试题(已下线)T27-实验综合题(已下线)化学(九省联考考后提升卷,甘肃卷)-2024年1月“九省联考”真题完全解读与考后提升(已下线)热点22 定量分析型实验综合题
真题
名校
3 . 碳酸钠俗称纯碱,是一种重要的化工原料。以碳酸氢铵和氯化钠为原料制备碳酸钠,并测定产品中少量碳酸氢钠的含量,过程如下:
步骤I. 的制备
的制备
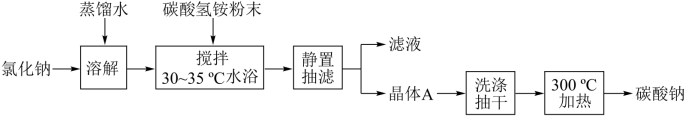
步骤Ⅱ.产品中 含量测定
含量测定
①称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中;
②移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用 盐酸标准溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸
盐酸标准溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸 ;
;
③在上述锥形瓶中再加入2滴指示剂N,继续用 盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸
盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸 ;
;
④平行测定三次, 平均值为22.45,
平均值为22.45, 平均值为23.51。
平均值为23.51。
已知:(i)当温度超过35℃时, 开始分解。
开始分解。
(ii)相关盐在不同温度下的溶解度表
回答下列问题:
(1)步骤I中晶体A的化学式为_______ ,晶体A能够析出的原因是_______ ;
(2)步骤I中“300℃加热”所选用的仪器是_______ (填标号);
A. B.
B.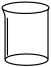 C.
C.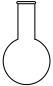 D.
D.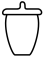
(3)指示剂N为_______ ,描述第二滴定终点前后颜色变化_______ ;
(4)产品中 的质量分数为
的质量分数为_______ (保留三位有效数字);
(5)第一滴定终点时,某同学俯视读数,其他操作均正确,则 质量分数的计算结果
质量分数的计算结果_______ (填“偏大”“偏小”或“无影响”)。
步骤I.
 的制备
的制备
步骤Ⅱ.产品中
 含量测定
含量测定①称取产品2.500g,用蒸馏水溶解,定容于250mL容量瓶中;
②移取25.00mL上述溶液于锥形瓶,加入2滴指示剂M,用
 盐酸标准溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸
盐酸标准溶液滴定,溶液由红色变至近无色(第一滴定终点),消耗盐酸 ;
;③在上述锥形瓶中再加入2滴指示剂N,继续用
 盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸
盐酸标准溶液滴定至终点(第二滴定终点),又消耗盐酸 ;
;④平行测定三次,
 平均值为22.45,
平均值为22.45, 平均值为23.51。
平均值为23.51。已知:(i)当温度超过35℃时,
 开始分解。
开始分解。(ii)相关盐在不同温度下的溶解度表
温度/ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
 | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 |
 | 11.9 | 15.8 | 21.0 | 27.0 | |||
 | 6.9 | 8.2 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 |
 | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
(1)步骤I中晶体A的化学式为
(2)步骤I中“300℃加热”所选用的仪器是
A.
 B.
B. C.
C. D.
D.
(3)指示剂N为
(4)产品中
 的质量分数为
的质量分数为(5)第一滴定终点时,某同学俯视读数,其他操作均正确,则
 质量分数的计算结果
质量分数的计算结果
您最近一年使用:0次
2021-06-09更新
|
9099次组卷
|
31卷引用:河北省邢台市第一中学2022-2023学年高二上学期期末考试化学试题
河北省邢台市第一中学2022-2023学年高二上学期期末考试化学试题2021年新高考湖南化学高考真题(已下线)考向02 物质的量浓度及其相关计算-备战2022年高考化学一轮复习考点微专题(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点31 化学实验与工艺流程-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)第6讲 钠及其化合物(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)江西省新余市第一中学2021-2022学年高三上学期第二次模拟考试化学试题2021年湖南省高考化学试卷变式题11-19(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)专题10 化学实验综合—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)押新高考卷16题 化学实验综合题-备战2022年高考化学临考题号押题(新高考通版)(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)专题17 化学实验综合题-三年(2020-2022)高考真题分项汇编(已下线)考点13 钠及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第06讲 钠及其化合物(讲)-2023年高考化学一轮复习讲练测(新教材新高考)第三章 综合拔高练(已下线)第28讲 定性、定量实验(练)-2023年高考化学一轮复习讲练测(新教材新高考)湖南省常德市汉寿县第一中学2022-2023学年高三上学期第一次月考化学试题(已下线)易错点05 钠及其化合物-备战2023年高考化学考试易错题山东省鄄城县第一中学2022-2023学年高二上学期期末考试化学试题辽宁省葫芦岛市兴城市高级中学等四校2022-2023学年高二上学期12月月考化学试题(已下线)专题六 金属元素及其化合物-实战高考·二轮复习核心突破山东省济南市历城第二中学2022-2023学年高二上学期期末线上测试化学试题(已下线)专题26 定量测定类综合性实验题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第十章 化学综合实验 第64讲 物质的检测综合实验探究热点1滴定法(已下线)第一部分 化学综合实验 综合提能训练(已下线)考点09 钠及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点13 钠及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
4 . 现有由乙酸、丙烯、环己烷组成的混合物,其中氧的质量分数为30%,则氢的质量分数是
| A.5% | B.10% | C.15% | D.20% |
您最近一年使用:0次
2024-04-02更新
|
215次组卷
|
2卷引用:河北省保定市清苑中学等校2023-2024学年高二下学期3月月考化学试题
21-22高一·全国·课后作业
名校
5 . 如图为实验室某浓盐酸试剂瓶标签上的部分数据,试根据标签.上的相关数据回答下列问题:.
(1)该浓盐酸中HCl的物质的量浓度为______ mol/L。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是______(填字母)。
(3)某学生欲用上述浓盐酸和蒸馏水配制480mL物质的量浓度为0.400mol/L的稀盐酸。
①该学生需要量取______ mL上述浓盐酸进行配制。
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏大”“偏小”或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面:______ ;
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水:______ 。
(4)①假设该同学成功配制了0.400mol/L的盐酸,他又用该盐酸中和含0.4g NaOH的NaOH溶液,则该同学需取______ mL盐酸。
②假设该同学用新配制的盐酸中和含0.4g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是______ 。
A.浓盐酸挥发,浓度不足 B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出
| 盐酸 分子式:HCl 相对分子质量:36.5 密度:  HCl的质量分数:36.5% |
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是______(填字母)。
| A.溶液中HCl的物质的量 | B.溶液的浓度 |
C.溶液中 的数目 的数目 | D.溶液的密度 |
①该学生需要量取
②在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(填“偏大”“偏小”或“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面:
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水:
(4)①假设该同学成功配制了0.400mol/L的盐酸,他又用该盐酸中和含0.4g NaOH的NaOH溶液,则该同学需取
②假设该同学用新配制的盐酸中和含0.4g NaOH的NaOH溶液,发现比①中所求体积偏小,则可能的原因是
A.浓盐酸挥发,浓度不足 B.配制溶液时,未洗涤烧杯
C.配制溶液时,俯视容量瓶刻度线 D.加水时超过刻度线,用胶头滴管吸出
您最近一年使用:0次
2024-02-22更新
|
74次组卷
|
6卷引用:河北省隆化存瑞中学2022-2023学年高一上学期第一次月考化学试题
河北省隆化存瑞中学2022-2023学年高一上学期第一次月考化学试题(已下线)第一章 单元检测-2021-2022学年高一化学课后培优练(鲁科版2019必修第一册)山东省威海市文登新一中2021-2022学年高一上学期12月月考化学试题河南省濮阳市第一高级中学2022-2023学年高一上学期期中质量检测化学试题黑龙江省齐齐哈尔市普高联谊校2022-2023学年高三上学期期中考试化学试题河南省周口市鹿邑县2023-2024学年高一上学期1月期末化学试题
名校
解题方法
6 . 某实验小组以含硒废料(主要成分为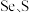 等)提取硒,并测定产品硒的纯度。回答下列问题:
等)提取硒,并测定产品硒的纯度。回答下列问题:
Ⅰ.提取硒的实验步骤如下:
i.含硒废料用 和硫酸混合溶液溶解,得到
和硫酸混合溶液溶解,得到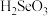 和
和 混合溶液;
混合溶液;
ii.控制反应温度为 ,使
,使 转化为
转化为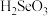 ;
;
iii.调节溶液 ,通入
,通入 ,得到硒单质沉淀。
,得到硒单质沉淀。
(1) 的空间结构名称为
的空间结构名称为___________ 。
(2)用如图所示装置进行实验。
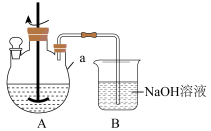
①反应器 的名称为
的名称为___________ ,装置 的加热方法为
的加热方法为___________ 。
②装置 的主要作用为
的主要作用为___________ 。
③步骤ⅲ生成硒单质的化学方程式为___________ 。
Ⅱ.测定产品硒的纯度,实验步骤如下:
i.准确称取 产品并研磨,加适量浓硫酸煮沸生成
产品并研磨,加适量浓硫酸煮沸生成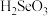 ,再稀释配成
,再稀释配成 的溶液。
的溶液。
ii.准确量取 待测液于锥形瓶中,用
待测液于锥形瓶中,用 酸性
酸性 标准溶液进行滴定,重复三次实验,实验数据见下表:
标准溶液进行滴定,重复三次实验,实验数据见下表:
(已知: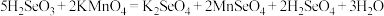 )
)
(3)该产品中硒的质量分数为___________ 。
(4)达到滴定终点时,若读数时仰视刻度线,则会导致测定结果___________ (填“偏大”、“偏小”或“不变”)。
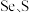 等)提取硒,并测定产品硒的纯度。回答下列问题:
等)提取硒,并测定产品硒的纯度。回答下列问题:Ⅰ.提取硒的实验步骤如下:
i.含硒废料用
 和硫酸混合溶液溶解,得到
和硫酸混合溶液溶解,得到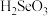 和
和 混合溶液;
混合溶液;ii.控制反应温度为
 ,使
,使 转化为
转化为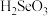 ;
;iii.调节溶液
 ,通入
,通入 ,得到硒单质沉淀。
,得到硒单质沉淀。(1)
 的空间结构名称为
的空间结构名称为(2)用如图所示装置进行实验。

①反应器
 的名称为
的名称为 的加热方法为
的加热方法为②装置
 的主要作用为
的主要作用为③步骤ⅲ生成硒单质的化学方程式为
Ⅱ.测定产品硒的纯度,实验步骤如下:
i.准确称取
 产品并研磨,加适量浓硫酸煮沸生成
产品并研磨,加适量浓硫酸煮沸生成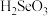 ,再稀释配成
,再稀释配成 的溶液。
的溶液。ii.准确量取
 待测液于锥形瓶中,用
待测液于锥形瓶中,用 酸性
酸性 标准溶液进行滴定,重复三次实验,实验数据见下表:
标准溶液进行滴定,重复三次实验,实验数据见下表:(已知:
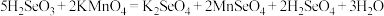 )
)| 实验次数 | 滴定前读数 | 滴定后读数 |
| 1 | 0.10 | 20.20 |
| 2 | 1.85 | 21.75 |
| 3 | 0.00 | 20.00 |
(3)该产品中硒的质量分数为
(4)达到滴定终点时,若读数时仰视刻度线,则会导致测定结果
您最近一年使用:0次
2024-02-29更新
|
40次组卷
|
2卷引用:河北正定中学本部2023-2024学年高二上学期期末考试化学试题
名校
解题方法
7 . 有机物M(只含C、H、O三种元素中的两种或三种)具有令人愉悦的牛奶香气,主要用于配制奶油、乳品、酸奶和草莓等型香精,是我国批准使用的香料产品,其沸点为148℃。某化学兴趣小组从粗品中分离提纯有机物M,然后借助李比希法、现代科学仪器测定有机物M的分子组成和结构,具体实验过程如下:
步骤一:将粗品用蒸馏法进行纯化。
(1)蒸馏装置如图1所示,仪器a的名称是___________ ,图中虚线框内应选用右侧的___________ (填“仪器x”或“仪器y”),该仪器使用时冷水从___________ 进。
(2)利用元素分析仪测得有机物M中碳的质量分数为54.5%,氢的质量分数为9.1%。
①M的实验式为___________ 。
②已知M的密度是同温同压下二氧化碳密度的2倍,则M的相对分子质量为___________ ,分子式为___________ 。
步骤三:确定M的结构简式。
(3)用核磁共振仪测出M的核磁共振氢谱如图2所示,图中峰面积之比为1∶3∶1∶3;利用红外光谱仪测得M的红外光谱如图3所示。___________ ,M的结构简式为___________ (填键线式)。
(4)写出两种含有酯基的M的同分异构体的结构简式:___________ 。
步骤一:将粗品用蒸馏法进行纯化。
(1)蒸馏装置如图1所示,仪器a的名称是

(2)利用元素分析仪测得有机物M中碳的质量分数为54.5%,氢的质量分数为9.1%。
①M的实验式为
②已知M的密度是同温同压下二氧化碳密度的2倍,则M的相对分子质量为
步骤三:确定M的结构简式。
(3)用核磁共振仪测出M的核磁共振氢谱如图2所示,图中峰面积之比为1∶3∶1∶3;利用红外光谱仪测得M的红外光谱如图3所示。

(4)写出两种含有酯基的M的同分异构体的结构简式:
您最近一年使用:0次
2023-09-15更新
|
322次组卷
|
3卷引用:河北省保定市唐县第一中学2022-2023学年高二下学期3月月考化学试题
名校
8 . 大连理工大学课题组通过CuO/ 催化,使NO-CO-
催化,使NO-CO- 反应体系在温和条件下产生
反应体系在温和条件下产生 ,为NO和CO的烟气处理提供了新的途径,其相关的反应为:
,为NO和CO的烟气处理提供了新的途径,其相关的反应为: (未配平),
(未配平), 是阿伏加德罗常数的值,下列有关说法正确的是
是阿伏加德罗常数的值,下列有关说法正确的是
 催化,使NO-CO-
催化,使NO-CO- 反应体系在温和条件下产生
反应体系在温和条件下产生 ,为NO和CO的烟气处理提供了新的途径,其相关的反应为:
,为NO和CO的烟气处理提供了新的途径,其相关的反应为: (未配平),
(未配平), 是阿伏加德罗常数的值,下列有关说法正确的是
是阿伏加德罗常数的值,下列有关说法正确的是A.标准状况下,1.12L NO中含有电子数为1.5 |
B.将 个 个 溶于100mL水中,所得溶液的质量分数约为29.9% 溶于100mL水中,所得溶液的质量分数约为29.9% |
C.生成22g  能消除NO的数目为0.2 能消除NO的数目为0.2 |
D.若NO和CO混合气体的平均相对分子质量为29,则含有CO的数目为0.5 |
您最近一年使用:0次
2024-03-13更新
|
302次组卷
|
4卷引用:河北省沧州市泊头市第一中学2023-2024学年高一下学期4月月考化学试题
解题方法
9 . 实验室需要0.5 mol·L-1硫酸溶液480 mL。回答下列问题:
(1)选取________ mL容量瓶,实验中需要质量分数为98%、密度为1.84 g·cm-3的浓硫酸________ mL,在量取时宜选用规格为________ (填序号)的量筒。
A.10 mL B.20 mL
C.50 mL D.100 mL
(2)如图所示的仪器中配制溶液肯定不需要的是________ (填序号),配制上述溶液还需用到的玻璃仪器是________ 、________ (填仪器名称)。
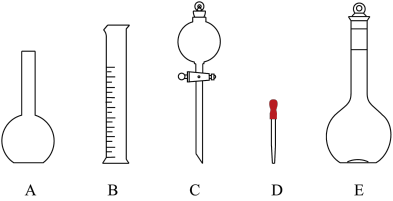
(3)在量取浓硫酸后,进行了下列操作:
①等稀释的浓硫酸的温度与室温一致后,将其沿玻璃棒注入容量瓶中。
②往容量瓶中小心加蒸馏水且边加边振荡摇匀,加蒸馏水至液面距容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的凹液面与瓶颈的刻度线相切。
③在盛有一定体积的蒸馏水的烧杯中沿杯壁注入浓硫酸,并用玻璃棒搅拌,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是________ (填序号)。
(4)若实验过程中遇到下列情况,对硫酸物质的量浓度有何影响(填“偏高”“偏低”或“无影响”)。
①未经冷却将溶液注入容量瓶中:________ ;
②定容时俯视液面:________ 。
(1)选取
A.10 mL B.20 mL
C.50 mL D.100 mL
(2)如图所示的仪器中配制溶液肯定不需要的是

(3)在量取浓硫酸后,进行了下列操作:
①等稀释的浓硫酸的温度与室温一致后,将其沿玻璃棒注入容量瓶中。
②往容量瓶中小心加蒸馏水且边加边振荡摇匀,加蒸馏水至液面距容量瓶刻度线1~2 cm时,改用胶头滴管加蒸馏水,使溶液的凹液面与瓶颈的刻度线相切。
③在盛有一定体积的蒸馏水的烧杯中沿杯壁注入浓硫酸,并用玻璃棒搅拌,使其混合均匀。
④用蒸馏水洗涤烧杯和玻璃棒2至3次,并将洗涤液全部注入容量瓶。
上述操作中,正确的顺序是
(4)若实验过程中遇到下列情况,对硫酸物质的量浓度有何影响(填“偏高”“偏低”或“无影响”)。
①未经冷却将溶液注入容量瓶中:
②定容时俯视液面:
您最近一年使用:0次
2023-08-26更新
|
603次组卷
|
3卷引用:河北省衡水志华实验中学2023-2024学年高一上学期期中考试化学试题
12-13高二上·江西宜春·阶段练习
名校
解题方法
10 . 在一容积可变的密闭容器中加入一定量的X、Y,发生反应mX(g)⇌nY(g) ∆H=QkJ/mol。反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如表所示:
下列说法正确 的是
| 温度(℃) | c(Y)/(mol/L) | ||
| 1L | 2L | 4L | |
| 100 | 1.00 | 0.75 | 0.53 |
| 200 | 1.20 | 0.90 | 0.63 |
| 300 | 1.30 | 1.00 | 0.70 |
| A.m>n |
| B.Q<0 |
| C.体积不变,温度升高,平衡向逆反应方向移动 |
| D.温度不变,压强增大,Y的质量分数减少 |
您最近一年使用:0次
2024-01-18更新
|
43次组卷
|
22卷引用:2012-2013学年河北省邢台一中高一下学期第三次月考化学试卷
(已下线)2012-2013学年河北省邢台一中高一下学期第三次月考化学试卷(已下线)2011-2012学年江西省上高二中高二上学期第三次月考化学试卷(已下线)2011-2012学年湖南省望城县第一中学高二上学期期末质量检测化学试卷(已下线)2013-2014学年黑龙江省哈师大附中高二上学期期中化学试卷(已下线)2013-2014学年安徽省屯溪一中高二上学期期中考试化学试卷(已下线)2014年高二化学人教版选修四 8化学平衡移动练习卷(已下线)2015届黑龙江省双鸭山市第一中学高三9月月考化学试卷(已下线)2014-2015湖南省新化一中高二上学期期中化学试卷2014-2015学年内蒙古包头市第一中学高一下学期期末考试化学试卷2015-2016浙江宁波效实中学高二上期中考试化学试题卷2015-2016学年云南省昆明三中高二下期中化学试卷2016-2017学年四川省成都开发区实验中学高二10月月考化学卷辽宁省大连市第二十四中学2017-2018学年高二上学期期中考试化学试题黑龙江省孙吴县第一中学2017-2018学年高二上学期期中考试化学试题步步为赢 高二化学暑假作业:作业九 化学反应速率和化学平衡吉林省白城市第一中学2018-2019学年高一下学期期末考试化学试题福建省三明市三地三校2020-2021学年高二上学期期中联考化学试题吉林省延边朝鲜族自治州汪清县第四中学2020-2021学年高二上学期期末考试化学试题黑龙江省鹤岗市第一中学2021-2022学年高二上学期期中考试化学试题湖南师范大学附属中学2021-2022学年高一下学期期末考试化学试题湖南省常德市第一中学2023-2024学年高二上学期12月月考化学试题海南省琼海市嘉积中学2023-2024学年高二上学期期末考试化学试题A卷



