1 . 实验小组制备高铁酸钾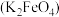 并探究其性质。
并探究其性质。
资料: 为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生
为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生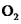 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。
(1)制备 (夹持装置略)
(夹持装置略)
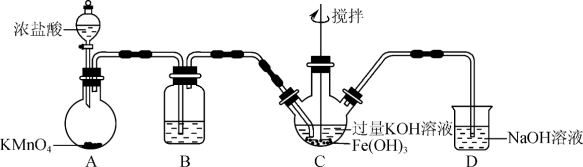
A为氯气发生装置。A中反应化学方程式是________________ (锰被还原为Mn2+)。除杂装置B所用试剂为________ 。C中得到紫色固体和溶液,C中Cl2发生的反应有 ,另外还有(离子方程式表示)
,另外还有(离子方程式表示)_____ 。
(2)探究 的性质
的性质
取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否 氧化了Cl-而产生Cl2,设计下图方案:
氧化了Cl-而产生Cl2,设计下图方案:
①由方案一中溶液变红可知a中含有______ 离子,但该离子的产生不能判断一定是 将Cl-氧化,还可能由
将Cl-氧化,还可能由____________ 产生(用离子方程式表示)。
②根据 的制备实验得出:氧化性Cl2
的制备实验得出:氧化性Cl2______  (填“>”或“<”),而方案二实验表明,Cl2和
(填“>”或“<”),而方案二实验表明,Cl2和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是________ 。
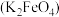 并探究其性质。
并探究其性质。资料:
 为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生
为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生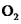 ,在碱性溶液中较稳定。
,在碱性溶液中较稳定。(1)制备
 (夹持装置略)
(夹持装置略)
A为氯气发生装置。A中反应化学方程式是
 ,另外还有(离子方程式表示)
,另外还有(离子方程式表示)(2)探究
 的性质
的性质取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明是否
 氧化了Cl-而产生Cl2,设计下图方案:
氧化了Cl-而产生Cl2,设计下图方案:| 方案一 | 取少量a,滴加KSCN溶液至过量溶液呈血红色。 |
| 方案二 | 用KOH溶液充分洗涤C中所得固体再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有C12产生。 |
 将Cl-氧化,还可能由
将Cl-氧化,还可能由②根据
 的制备实验得出:氧化性Cl2
的制备实验得出:氧化性Cl2 (填“>”或“<”),而方案二实验表明,Cl2和
(填“>”或“<”),而方案二实验表明,Cl2和 的氧化性强弱关系相反,原因是
的氧化性强弱关系相反,原因是
您最近一年使用:0次
名校
解题方法
2 . 为了防止食品变质,常在食品袋中放入小袋的铁粉,这是利用铁的
| A.还原性 | B.氧化性 | C.酸性 | D.碱性 |
您最近一年使用:0次
2023-09-23更新
|
293次组卷
|
5卷引用:黑龙江省佳木斯市三校联考2023-2024学年高一上学期1月期末化学试题
黑龙江省佳木斯市三校联考2023-2024学年高一上学期1月期末化学试题黑龙江省七台河市第六中学2022-2023学年高一上学期期末考试化学试题(已下线)【精品卷】3.1.1 铁的单质课堂例题-人教版2023-2024学年必修第一册(已下线)专题03 铁 金属材料-【寒假自学课】2024年高一化学寒假提升学与练(人教版2019)安徽省宿州市十三校联考2023-2024学年高一上学期1月期末考试化学试题
名校
解题方法
3 . 比较下列性质(用“>”、“=”、“<”填空)
①半径 P________ F
②酸性 H3PO4________ H2SO4
③碱性Mg(OH)2________ Al(OH)3
④稳定性 H2S________ H2O
⑤还原性H2S________ HCl
⑥氧化性 Cl2________ Br2 .
①半径 P
②酸性 H3PO4
③碱性Mg(OH)2
④稳定性 H2S
⑤还原性H2S
⑥氧化性 Cl2
您最近一年使用:0次
2020-03-06更新
|
473次组卷
|
2卷引用:黑龙江省桦南县第二中学2019-2020学年高二下学期期中考试化学试题
14-15高一上·浙江宁波·期末
4 . 如图所示是验证氯气性质的微型实验,a、b、c、d、e是浸有相关溶液的滤纸。向KMnO4晶体滴加一滴浓盐酸后,立即用另一培养皿扣在上面。
已知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O
已知:2KMnO4+16HCl=2KCl+5Cl2↑+2MnCl2+8H2O

| 选项 | 实验现象 | 解释或结论 |
| A | a处变蓝,b处变红棕色 | 氧化性:Cl2>Br2>I2 |
| B | c处先变红,后褪色 | 氯气与水生成了酸性物质 |
| C | d处立即褪色 | 氯气与水生成了漂白性物质 |
| D | e处变血红色 | 还原性:Fe2+>Cl- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-21更新
|
887次组卷
|
54卷引用:黑龙江省佳木斯市第十二中学2022-2023学年高三上学期期中考试化学试题
黑龙江省佳木斯市第十二中学2022-2023学年高三上学期期中考试化学试题(已下线)2013-2014学年浙江省宁波市八校高一上学期期末联考化学试卷(已下线)2014高考化学专题突破训练 专题10非金属及其化合物练习卷(已下线)2014高考名师推荐化学氯、溴、碘及其化合物主要性质(已下线)2013-2014学年浙江省杭州地区六校高二下学期期中联考化学试卷(已下线)2013-2014河北省石家庄一中上学期开学考试高二化学试卷(已下线)2015届湖南省长沙市长郡中学高三第一次月考化学试卷2015届辽宁省抚顺市二中高三上学期期中考试化学试卷2014-2015河北唐山市一中高一下学期开学调研考试化学试卷2015-2016学年黑龙江省大庆铁人中学高一上期末化学试卷2015-2016学年湖南省长沙市望城一中高一上期末化学试卷河南省南阳市2016-2017学年高一上学期期终质量评估化学试题2016-2017学年江西省南昌市第二中学高一上学期期末考试化学试卷河北省涞水波峰中学2018届高三第一次调研考试化学试题甘肃省兰州市第一中学2018届高三8月月考化学试题天津市和平区2017-2018学年高一上学期期末考试化学试题(已下线)2019高考备考一轮复习精品资料 第四章 常见的非金属及其化合物 第2讲 氯及其化合物【押题专练】辽宁省阜新市海州高级中学2019届高三上学期第一次月考化学试题河北省承德市第一中学2018-2019学年高一上学期第三次月考化学试题黑龙江省大庆市铁人中学2018-2019学年高一下学期开学考试化学试题陕西省榆林市第二中学2018-2019学年高二下学期期中考试化学试题2019届上海奉贤区高考第一次模拟化学试题陕西省西安电子科技大学附属中学2019-2020学年高一上学期期末考试化学试题2020届上海市奉贤区高考化学一模试卷2012年上海市高考化学试题(已下线)【南昌新东方】师大附中2019-2020 高一(上) 期末安徽省肥东县第二中学2019-2020学年高一下学期期中考试(共建班)化学试题河南省信阳市罗山县2021届高三第一次调研(8月联考)化学试题江西省奉新县第一中学2021届高三上学期第一次月考化学试题内蒙古自治区呼和浩特市和林格尔县第一中学2018-2019学年高二上学期第一次月考化学试题人教版(2019)高一必修第一册 第二章 海水中的重要元素 第二节 氯及其化合物 教材帮江西省上饶市横峰中学2021届高三上学期第一次月考化学试题宁夏青铜峡市高级中学2021届高三上学期期中考试化学试题黑龙江伊春林业管理局第二中学2021届高三上学期期中考试化学试题(已下线)第12讲 富集在海水中的元素——卤素(精讲)-2022年一轮复习讲练测(已下线)考点09 氯及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点09 氯及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)内蒙古自治区包钢第一中学2021-2022学年高三上学期10月月考化学试题浙江省绍兴市第一中学2016-2017学年高一下学期期末考试化学试题宁夏青铜峡市高级中学2021-2022学年高三上学期11月测试化学试题浙江省宁波中学2021-2022学年高一上学期期中考试化学试题(已下线)考点09 氯及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第12讲 富集在海水中的元素——卤素(讲)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第05练 氯及其化合物-2023年高考化学一轮复习小题多维练(全国通用)(已下线)第05练 氯及其化合物-2023年高考化学一轮复习小题多维练(全国通用)天津市红桥区2019-2020学年高一上学期期末考试化学试题(已下线)2.2.2 氯气与金属、非金属及还原性化合物的反应-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)福建省龙岩第一中学2022-2023学年高一上学期第二次月考化学试题江西省景德镇一中2022-2023学年高一上学期期中(18班)化学试题.广东省广州市第八十六中学2022-2023学年高一上学期期中考试化学试题(已下线)【知识图鉴】单元讲练测必修第一册第二单元03巩固练(已下线)考点09 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)安徽省当涂第一中学2023-2024学年高二上学期开学考试化学试题山西省阳泉市城区瑞源教育培训学校2023-2024学年高二上学期12月大联考化学试题
名校
解题方法
5 . 高锰酸钾溶液常用于物质的定性检验与定量分析。
(1)实验室里欲用KMnO4固体来配制250.00 mL 0.1000 mol•L-1的KMnO4酸性溶液。
①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、_________ 、_________ 。
②下列关于“容量瓶及其使用”的叙述中正确的是_________ (填序号)。
A.使用前必须检查是否漏水 B.能配制一定体积准确浓度的标准溶液
C.可用来长期贮存溶液 D.能用作溶解固体、稀释浓溶液的容器
③下列操作对实验结果的影响偏高的是_________ (填序号)。
A.加水定容时俯视刻度线
B.未洗涤溶解后的烧杯和玻璃棒
C.颠倒摇匀后发现凹液面低于刻度线,没有加水补到刻度线
D.未经冷却趁热将溶液注入容量瓶中并进行定容
(2)用上述酸性KMnO4溶液来测定FeSO4溶液中Fe2+的物质的量浓度。原理如下:FeSO4 + KMnO4 + H2SO4 — K2SO4 + MnSO4 + Fe2(SO4)3 + H2O (未配平),实验时应测定的数据有:量取FeSO4溶液的体积和__________________ 。该反应中还原剂与氧化剂的物质的量之比为_________ 。
(3)维生素C的水溶液能使高锰酸钾溶液褪色,根据这一原理,常用高锰酸钾测定蔬菜或水果中的维生素C的含量。上述实验原理体现了维生素C具有_____ (填氧化性、还原性)。
(1)实验室里欲用KMnO4固体来配制250.00 mL 0.1000 mol•L-1的KMnO4酸性溶液。
①需用的仪器有天平、药匙、烧杯、玻璃棒、量筒、
②下列关于“容量瓶及其使用”的叙述中正确的是
A.使用前必须检查是否漏水 B.能配制一定体积准确浓度的标准溶液
C.可用来长期贮存溶液 D.能用作溶解固体、稀释浓溶液的容器
③下列操作对实验结果的影响偏高的是
A.加水定容时俯视刻度线
B.未洗涤溶解后的烧杯和玻璃棒
C.颠倒摇匀后发现凹液面低于刻度线,没有加水补到刻度线
D.未经冷却趁热将溶液注入容量瓶中并进行定容
(2)用上述酸性KMnO4溶液来测定FeSO4溶液中Fe2+的物质的量浓度。原理如下:FeSO4 + KMnO4 + H2SO4 — K2SO4 + MnSO4 + Fe2(SO4)3 + H2O (未配平),实验时应测定的数据有:量取FeSO4溶液的体积和
(3)维生素C的水溶液能使高锰酸钾溶液褪色,根据这一原理,常用高锰酸钾测定蔬菜或水果中的维生素C的含量。上述实验原理体现了维生素C具有
您最近一年使用:0次
2023-01-06更新
|
208次组卷
|
2卷引用:黑龙江省富锦市第一中学2022-2023学年高一上学期期末考试化学试题
解题方法
6 . 利用下图可以从不同角度研究含硫物质的性质及其转化关系。

回答下列问题:
(1) 与
与 反应的化学方程式为
反应的化学方程式为____________ ,反应中 体现
体现___________ (填“氧化性”或“还原性”)。
(2)加热时,浓硫酸与木炭反应的化学方程式为____________ ,下列试剂不能用于验证生成物中含有 的是
的是___________ (填标号)。
a. 品红溶液 b. 酸性 溶液 c. 澄清石灰水
溶液 c. 澄清石灰水

回答下列问题:
(1)
 与
与 反应的化学方程式为
反应的化学方程式为 体现
体现(2)加热时,浓硫酸与木炭反应的化学方程式为
 的是
的是a. 品红溶液 b. 酸性
 溶液 c. 澄清石灰水
溶液 c. 澄清石灰水
您最近一年使用:0次
2021-10-09更新
|
497次组卷
|
4卷引用:黑龙江省佳木斯市农垦建三江管理局第二高级中学2021-2022学年高一下学期第一次月考化学试题
黑龙江省佳木斯市农垦建三江管理局第二高级中学2021-2022学年高一下学期第一次月考化学试题山东省2021年普通高中合格考化学试题山东省2021年夏季普通高中学业水平合格考试化学试题(已下线)3.3.1 硫循环-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)
7 . KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯,其变化可表述为:
______KClO3+______HCl(浓)=______KCl+______ClO2↑+______Cl2↑+______H2O
(1)请配平上述化学方程式_____ 。
(2)浓盐酸在反应中显示出来的性质是___ (填编号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)氧化剂是____ ,氧化产物是___ 。
______KClO3+______HCl(浓)=______KCl+______ClO2↑+______Cl2↑+______H2O
(1)请配平上述化学方程式
(2)浓盐酸在反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(3)氧化剂是
您最近一年使用:0次
2021-10-11更新
|
234次组卷
|
3卷引用:黑龙江省佳木斯学校(佳木斯市实验中学)2021-2022学年高一10月月考化学试题
名校
解题方法
8 . H2O2在实验、医疗、化工等方面有广泛的应用。
(1)H2O2中O的化合价为_____ ,具有____ (填“氧化性”“还原性”或“氧化性和还原性”)。
(2)酸性高锰酸钾溶液可与H2O2反应,其化学方程式是5H2O2+2KMnO4+3H2SO4=X+2MnSO4+5O2 +8H2O。已知:稀MnSO4溶液几乎无色。
+8H2O。已知:稀MnSO4溶液几乎无色。
①X的化学式是_______ 。
②用双线桥法标出,上述反应中电子转移的方向和数目_____ 。
③上述反应中的还原剂为_____ (填化学式),被还原的元素是______ (填元素符号)。
④高锰酸钾溶液呈_____ 色,向酸性KMnO4溶液中滴入双氧水,观察到的现象是______ 。
(1)H2O2中O的化合价为
(2)酸性高锰酸钾溶液可与H2O2反应,其化学方程式是5H2O2+2KMnO4+3H2SO4=X+2MnSO4+5O2
 +8H2O。已知:稀MnSO4溶液几乎无色。
+8H2O。已知:稀MnSO4溶液几乎无色。①X的化学式是
②用双线桥法标出,上述反应中电子转移的方向和数目
③上述反应中的还原剂为
④高锰酸钾溶液呈
您最近一年使用:0次
名校
9 . ClO2气体的氧化性与Cl2的氧化性相近,是安全、无毒的绿色消毒剂和保鲜剂。某兴趣小组对其制备、吸收、释放和应用进行了研究,如图。
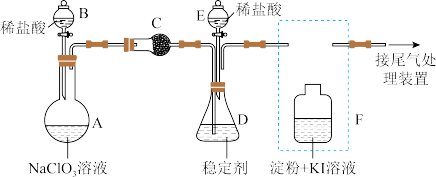
(1)安装F中导管时,应选用如图中的_______ (填字母)。
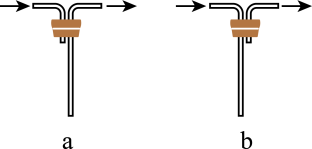
(2)A装置用于制备ClO2,在制备过程中会生成Cl2,则发生反应的化学方程式为:___________ 。C装置的作用____________ ,ClO2在D中会被稳定剂完全吸收生成NaClO2,整个过程中,F溶液的颜色不变。
(3)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为___________ 。设计实验证明NaClO2具有氧化性:__________________ (可供选择的试剂:稀HNO3、稀H2SO4、K2SO3溶液、BaCl2溶液、FeCl2溶液、KSCN溶液)
(4)ClO2和Cl2在消毒时自身均被还原为Cl-,则常温常压下,等体积的ClO2的消毒能力是Cl2的____ 倍。

(1)安装F中导管时,应选用如图中的

(2)A装置用于制备ClO2,在制备过程中会生成Cl2,则发生反应的化学方程式为:
(3)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
(4)ClO2和Cl2在消毒时自身均被还原为Cl-,则常温常压下,等体积的ClO2的消毒能力是Cl2的
您最近一年使用:0次
2020-09-25更新
|
183次组卷
|
4卷引用:黑龙江省农垦建三江管理局第一高级中学2021届高三上学期期中考试化学试题
名校
10 . 下列关于氯元素的说法正确的是
| A.HCl具有很强的酸性,且只有氧化性没有还原性 |
B. 、 、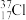 为不同的核素,有完全不同的化学性质 为不同的核素,有完全不同的化学性质 |
| C.1.12L含有1 .7NA个质子(NA表示阿伏伽德罗常数) |
| D.氯气可从KI溶液中置换出I2,说明氯的非金属性比碘强 |
您最近一年使用:0次



