名校
1 . 如图是元素周期表的一部分,表中所列字母分别代表一种元素。根据表中所列元素回答下列问题:_______ ,a的离子结构示意图是_______ 。
(2)h在元素周期表中的位置为_______ ,下列说法能证明元素f和h非金属性强弱的是_______ (填字母)。
a.比较两种元素简单阴离子的还原性
b.比较两种元素简单氢化物的热稳定性
c.比较两种元素单质的沸点
d.比较两种元素氧化物对应水化物的酸性
(3)元素e与元素b的最高价氧化物对应的水化物按计量数1∶2反应,写出反应的化学方程式_______ 。
(4)镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。酸性:
_______  (填“>”或“<”),氧化镓与
(填“>”或“<”),氧化镓与 反应的离子方程式为
反应的离子方程式为_______ 。
(5)写出实验室制备g单质的离子方程式_______ 。
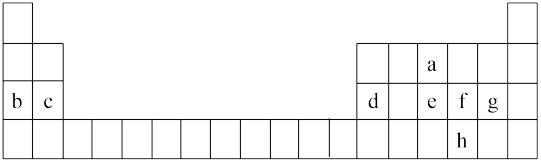
(2)h在元素周期表中的位置为
a.比较两种元素简单阴离子的还原性
b.比较两种元素简单氢化物的热稳定性
c.比较两种元素单质的沸点
d.比较两种元素氧化物对应水化物的酸性
(3)元素e与元素b的最高价氧化物对应的水化物按计量数1∶2反应,写出反应的化学方程式
(4)镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。酸性:

 (填“>”或“<”),氧化镓与
(填“>”或“<”),氧化镓与 反应的离子方程式为
反应的离子方程式为(5)写出实验室制备g单质的离子方程式
您最近一年使用:0次
2022-12-11更新
|
193次组卷
|
3卷引用:黑龙江省绥化市绥棱县第一中学2023-2024学年高一上学期1月期末化学试题
2 . 下列有关实验装置的说法中正确的是
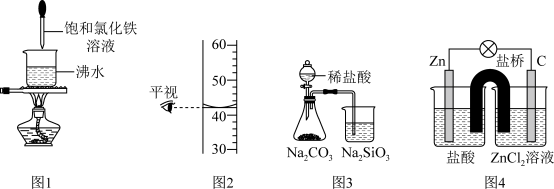

| A.用图1装置可以制备少量氢氧化铁胶体 |
B.图2装置中读取的数据为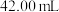 |
C.用图3可证明酸性强弱顺序为: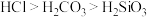 |
| D.用图4装置可以实现化学能持续转化为电能 |
您最近一年使用:0次
2022-03-07更新
|
257次组卷
|
2卷引用:黑龙江省海伦市第二中学2022-2023学年高三上学期期末考试化学试题
3 . 如图是实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。下列有关说法正确的是
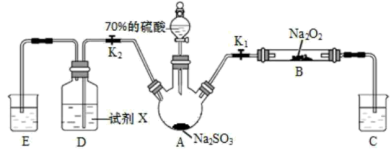

| A.为防止环境污染,装置C和E中的试剂均取用饱和的石灰水 |
| B.关闭K1,打开K2,试剂X是酸性KMnO4或FeCl3溶液,均可证明SO2有还原性 |
| C.实验过程中体现了硫酸的酸性、吸水性、难挥发性、强氧化性 |
| D.关闭K2,打开K1,滴加硫酸,则装置B中每消耗1molNa2O2,转移1mol电子 |
您最近一年使用:0次
2021-10-21更新
|
124次组卷
|
2卷引用:黑龙江省绥化市第二中学2022-2023年高三上学期第一次月考化学试题
名校
4 . 下列说法不正确的是( )
| A.Na2CO3溶液蒸干并灼烧可得无水Na2CO3 |
| B.pH相同的HA和HB溶液,分别与一定浓度的氢氧化钠溶液完全中和,HA消耗的氢氧化钠溶液体积多,则可证明酸性HA<HB |
| C.任何温度下均能自发进行2H2O2(l)=2H2O(l) +O2(g),则该反应的△H<0,△S>0 |
| D.除去MgCl2溶液中混有的少量FeCl3,可向溶液中加入足量MgCO3,过滤 |
您最近一年使用:0次
2019-12-30更新
|
124次组卷
|
3卷引用:黑龙江省绥化市安达市第七中学2019-2020学年高二下学期期中考试化学试题
5 . 将SO2分别通入下列4种溶液中,有关说法不正确的是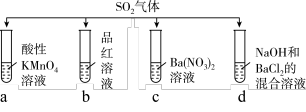
| A.试管a中实验可以证明SO2具有还原性 | B.试管b中溶液褪色,说明SO2具有漂白性 |
| C.试管c中能产生白色沉淀,说明SO2具有氧化性 | D.试管d中能产生白色沉淀,该沉淀不溶于稀硝酸 |
您最近一年使用:0次
2018-03-03更新
|
582次组卷
|
10卷引用:黑龙江省肇东市第四中学2021-2022学年高一下学期期中考试化学试题
黑龙江省肇东市第四中学2021-2022学年高一下学期期中考试化学试题黑龙江省大庆实验中学2017-2018学年高一上学期期末考试化学试题鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第2节 硫的转化 课时1 硫、二氧化硫和三氧化硫高一必修第二册(人教2019版)第五章 第一节 硫及其化合物 课时1 硫和二氧化硫重庆实验中学2021届高三第一学月测试化学试题(已下线)4.1.1 二氧化硫的性质和应用(备作业)-【上好课】2021-2022学年高一化学同步备课系列(苏教版2019必修第一册)山东省枣庄市滕州市第五中学2022-2023学年高一上学期第二次线上考试化学试题广东省广州科学城中学2022-2023学年高一下学期期中考试化学试题作业(二十一) 实验室里研究不同价态硫元素之间的转化四川省华蓥中学2023-2024学年高一下学期5月期中化学试题
解题方法
6 . 草酸(H2C2O4)、草酸铵[(NH4)2C2O4]是重要的化合物。回答下列问题:
(1)实验表明,加热条件下,H2C2O4可分解生成CO2、CO和H2O。为了验证产物中的CO,设计如下实验装置:_______________ (装置可重复利用)。装置F中发生的化学反应方程式为_______________ 。
②能证明草酸晶体分解产物中有CO的现象是_______________ 。
(2)H2C2O4能与酸性高锰酸钾溶液反应,离子方程式为 。该反应中,还原剂为
。该反应中,还原剂为______________ (填化学式),若称取mg草酸晶体(H2C2O4·2H2O)粗产品,配成100mL溶液于锥形瓶中,加入V mL a mol·L-1KMnO4溶液,恰好完全反应,则该草酸晶体的纯度为______________ %[M(H2C2O4·2H2O)=126g·mol-1]。
(3)(NH4)2C2O4是良好的Co2+的沉淀剂,如下为(NH4)2C2O4加入CoSO4溶液中制备CoO的流程图:______________ (填化学式)。
②称量mg CoC2O4·2H2O[M(CoC2O4·2H2O)=183g·mol-1]“高温分解”,测得固体的失重率( )与温度的关系曲线如图所示:
)与温度的关系曲线如图所示:_______________ ;“高温分解”需控制的最低温度为_______________ (经测定290~890℃过程中产生的气体只有CO2)。
(1)实验表明,加热条件下,H2C2O4可分解生成CO2、CO和H2O。为了验证产物中的CO,设计如下实验装置:
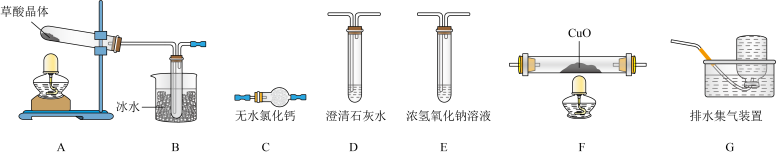
②能证明草酸晶体分解产物中有CO的现象是
(2)H2C2O4能与酸性高锰酸钾溶液反应,离子方程式为
 。该反应中,还原剂为
。该反应中,还原剂为(3)(NH4)2C2O4是良好的Co2+的沉淀剂,如下为(NH4)2C2O4加入CoSO4溶液中制备CoO的流程图:
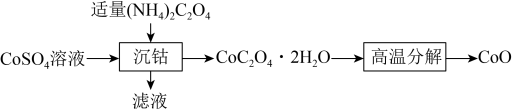
②称量mg CoC2O4·2H2O[M(CoC2O4·2H2O)=183g·mol-1]“高温分解”,测得固体的失重率(
 )与温度的关系曲线如图所示:
)与温度的关系曲线如图所示: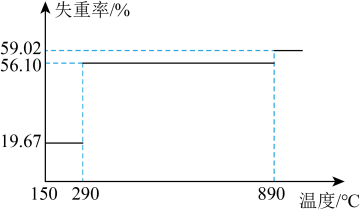
您最近一年使用:0次
名校
7 . 四氮化四硫( ,S为
,S为 价)是重要的硫氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于
价)是重要的硫氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于 等有机溶剂,可用
等有机溶剂,可用 与
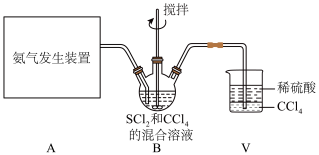
与 (红棕色液体)反应制备,反应装置如图所示(夹持装置已省略)。
(红棕色液体)反应制备,反应装置如图所示(夹持装置已省略)。
已知: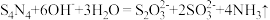
(1)氨气发生装置可以选用___________ (填字母)。 的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为
的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为___________ ;证明 反应完全的现象是
反应完全的现象是______________________ 。
(3)装置C的作用是___________________ ,其中 的作用是
的作用是______________ 。
(4)测定产品纯度:
i.蒸氨:取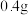 固体样品加入三颈烧瓶中,再加入足量
固体样品加入三颈烧瓶中,再加入足量 溶液并加热,将蒸出的
溶液并加热,将蒸出的 通入含有
通入含有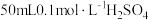 标准溶液的锥形瓶中。
标准溶液的锥形瓶中。
ii.滴定:用 的
的 溶液滴定剩余的
溶液滴定剩余的 ,记录消
,记录消 溶液的体积。重复实验3次,数据如下表所示:
溶液的体积。重复实验3次,数据如下表所示:
用 标准溶液滴定硫酸溶液之前,需要润洗滴定管,润洗滴定管的操作为
标准溶液滴定硫酸溶液之前,需要润洗滴定管,润洗滴定管的操作为______________________ ,滴定时选用的指示剂为___________ ,制得的 的纯度为
的纯度为___________ (保留两位有效数字)。
 ,S为
,S为 价)是重要的硫氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于
价)是重要的硫氮二元化合物,室温下为橙黄色固体,难溶于水,能溶于 等有机溶剂,可用
等有机溶剂,可用 与
与 (红棕色液体)反应制备,反应装置如图所示(夹持装置已省略)。
(红棕色液体)反应制备,反应装置如图所示(夹持装置已省略)。已知:
(1)氨气发生装置可以选用
a. 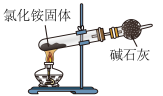 b.
b. c.
c. 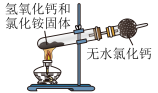 d.
d.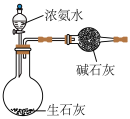
 的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为
的同时,还生成一种常见固体单质和一种盐,该反应的化学方程式为 反应完全的现象是
反应完全的现象是(3)装置C的作用是
 的作用是
的作用是(4)测定产品纯度:
i.蒸氨:取
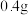 固体样品加入三颈烧瓶中,再加入足量
固体样品加入三颈烧瓶中,再加入足量 溶液并加热,将蒸出的
溶液并加热,将蒸出的 通入含有
通入含有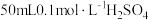 标准溶液的锥形瓶中。
标准溶液的锥形瓶中。ii.滴定:用
 的
的 溶液滴定剩余的
溶液滴定剩余的 ,记录消
,记录消 溶液的体积。重复实验3次,数据如下表所示:
溶液的体积。重复实验3次,数据如下表所示:实验序号 | 初始读数( | 最终读数( |
① | 0.20 | 20.22 |
② | 0.40 | 24.85 |
③ | 1.00 | 20.98 |
 标准溶液滴定硫酸溶液之前,需要润洗滴定管,润洗滴定管的操作为
标准溶液滴定硫酸溶液之前,需要润洗滴定管,润洗滴定管的操作为 的纯度为
的纯度为
您最近一年使用:0次
2024-03-26更新
|
491次组卷
|
4卷引用:2024届黑龙江省绥化市高三下学期3月联考模拟检测化学试卷
2024届黑龙江省绥化市高三下学期3月联考模拟检测化学试卷 (已下线)题型9 实验综合题(25题)-2024年高考化学常考点必杀300题(新高考通用)(已下线)提升练08 化学实验综合-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)黑龙江省2023-2024学年高三下学期3月期中联合考试化学试卷
名校
解题方法
8 . 下列由实验现象所得结论不正确 的是
A.向 溶液中滴加氢硫酸,立即产生淡黄色沉淀,证明 溶液中滴加氢硫酸,立即产生淡黄色沉淀,证明 具有氧化性 具有氧化性 |
B.向酸性 溶液中加入 溶液中加入 粉末,紫色褪去,证明 粉末,紫色褪去,证明 中含Fe(Ⅱ) 中含Fe(Ⅱ) |
C.向某溶液中滴加盐酸酸化的氯化钡溶液,有白色沉淀生成,证明溶液存在 |
D.向 溶液中加入几滴氯水振荡,再加 溶液中加入几滴氯水振荡,再加 萃取,下层呈紫色,上层无色,证明还原性 萃取,下层呈紫色,上层无色,证明还原性 |
您最近一年使用:0次
2023-05-27更新
|
372次组卷
|
4卷引用:黑龙江省肇东市第四中学校2023-2024学年高三上学期第二次月考化学试卷
黑龙江省肇东市第四中学校2023-2024学年高三上学期第二次月考化学试卷北京市中国人民大学附属中学2023届高三三模化学试题(已下线)考点45 物质的分离、提纯和检验(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)天津北京师范大学静海附属学校 (天津市静海区北师大实验学校)2023-2024学年高三上学期第二次阶段检测(期中)化学试题
名校
解题方法
9 . 镍氢电池是一种新型绿色电池,利用废旧镍氢电池的金属电极芯[主要成分为Ni(OH)2、Co(OH)2及少量铁、铝的氧化物等]生产硫酸镍、碳酸钴的工艺流程如图。

已知:部分金属阳离子以氢氧化物的形式沉淀时溶液的pH见表:
回答下列问题:
(1)步骤①用稀硫酸浸取金属电极芯前,提高浸取率方法___________________ (写一种)。
(2)沉淀A的主要成分___________ ,步骤②调pH的范围为___________ ,证明沉淀A已经洗净的实验操作为______________ 。
(3)将“母液1”的pH调至3~4,再加入NaClO,NaClO的作用是__________ 。
(4)步骤④离子方程式___________ ,若用盐酸代替H2SO4和H2O2的混合液也能达到目的,从环保角度分析不采用盐酸的原因:___________________________ 。
(5)步骤⑤中“母液3”与NaHCO3溶液反应的离子方程式为___________________ 。
(6)步骤⑧的操作为___________________ 。

已知:部分金属阳离子以氢氧化物的形式沉淀时溶液的pH见表:
| 金属阳离子 | Fe2+ | Fe3+ | Al3+ | Ni2+ | Co2+ |
| 开始沉淀时pH | 6.3 | 1.5 | 3.4 | 6.2 | 7.15 |
| 完全沉淀时pH(金属阳离子浓度<10-5mol/L) | 9.0 | 3.2 | 4.7 | 9.2 | 9.15 |
(1)步骤①用稀硫酸浸取金属电极芯前,提高浸取率方法
(2)沉淀A的主要成分
(3)将“母液1”的pH调至3~4,再加入NaClO,NaClO的作用是
(4)步骤④离子方程式
(5)步骤⑤中“母液3”与NaHCO3溶液反应的离子方程式为
(6)步骤⑧的操作为
您最近一年使用:0次
10 . 下列不能达到实验目的的是
| A.证明溶液中仅含Fe2+、不含Fe3+,向溶液先滴入KSCN溶液,再滴新制氯水 |
| B.证明溶液中含Cl-,先加Ba(NO3)2溶液,再加入硝酸酸化的硝酸银溶液 |
| C.证明溶液中含Na+,用洁净铂丝随取待测溶液,在酒精灯外焰上灼烧,观察火焰颜色 |
D.证明溶液中含CO ,将溶液逐滴加入稀盐酸中,并将产生的气体通入澄清石灰水 ,将溶液逐滴加入稀盐酸中,并将产生的气体通入澄清石灰水 |
您最近一年使用:0次

 )
)

