1 . 回答下列问题。
(1)镍元素基态原子的核外电子排布式为___________ ,3d能级上的未成对电子数为___________ 。
(2)基态Ge原子的价层电子排布式为___________ ,有___________ 个未成对电子。
(3)Zn2+基态核外电子排布式为___________ 。
(4)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用___________ 形象化描述。在基态 14C原子中,核外存在___________ 对自旋相反的电子。
(5)基态Fe原子有___________ 个未成对电子。Fe3+的电子排布式为___________ 。
(1)镍元素基态原子的核外电子排布式为
(2)基态Ge原子的价层电子排布式为
(3)Zn2+基态核外电子排布式为
(4)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用
(5)基态Fe原子有
您最近一年使用:0次
名校
解题方法
2 . 下列离子方程式书写正确的是
A.向Mg(HCO3)2溶液中加入足量的澄清石灰水:Mg2++2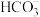 +Ca2++2OH-=MgCO3↓+CaCO3↓+2H2O +Ca2++2OH-=MgCO3↓+CaCO3↓+2H2O |
| B.XeF2通入水中:2XeF2+2H2O=2Xe+4F-+4H++O2 |
C.向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰使 沉淀完全 沉淀完全 +Al3++2 +Al3++2 +2Ba2++4OH-=Al(OH)3↓+NH3·H2O+2BaSO4↓ +2Ba2++4OH-=Al(OH)3↓+NH3·H2O+2BaSO4↓ |
| D.CuCl2溶液中加入NaHS溶液Cu 2++2HS-+2H2O=Cu(OH)2↓+2H2S↑ |
您最近一年使用:0次
名校
解题方法
3 . 下图是正四面体的原子簇Aun的一个三角形面图,根据该图,确定Aun中n的数值为
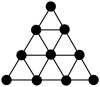
| A.17 | B.18 | C.19 | D.20 |
您最近一年使用:0次
名校
解题方法
4 . 1994年度诺贝尔化学奖授予为研究臭氧做出特殊贡献的化学家。O3能吸收有害紫外线,保护人类赖以生存的空间。O3分子的结构如图,呈V形,键角116.5o,与SO2近似,三个原子以一个O原子为中心,与另外两个O原子分别构成一个极性共价键;中间O原子提供2个电子,旁边两个O原子各提供1个电子,构成一个大π键——三个O原子均等地享有这4个电子。在1.01×105Pa,273K时,O3在催化剂作用下能迅速转化为O2,当生成该状态下22.4L O2时,转移电子数的物质的量为
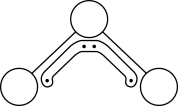
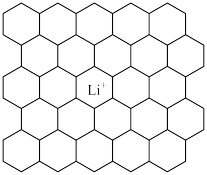
| A.1 mol | B.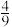 mol mol | C.0 mol | D.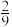 mol mol |
您最近一年使用:0次
名校
解题方法
5 . 石墨和金刚石均属于碳的同素异形体,物理性质相差很大,归根结底是晶体结构不同造成的。已知石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如下图所示,图中用虚线标出了石墨的一个六方晶胞。___________ 。
(2)已知石墨的层间距为334.8 pm,C-C键长为142 pm,计算石墨晶体的密度为___________ (单位:g·cm-3)。
(3)石墨可用作锂离子电池的负极材料,充电时发生下述反应:Li1-xC6+x Li++x e-→ LiC6 其结果是,Li+嵌入石墨的A、B层间,导致石墨的层堆积方式发生改变,形成化学式为LiC6的嵌入化合物。
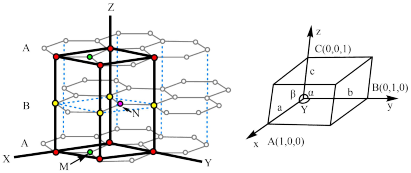
Ⅰ.下图给出了一个Li+沿C轴投影在A层上的位置,试在下图上标出与该离子临近的其他6个Li+的投影位置___________ 。
Ⅱ.在LiC6中,Li+与相邻石墨六元环的作用力属于何种键型___________ ?
Ⅲ.某石墨嵌入化合物每个六元环都对应一个Li+,写出它的化学式___________ 。
(2)已知石墨的层间距为334.8 pm,C-C键长为142 pm,计算石墨晶体的密度为
(3)石墨可用作锂离子电池的负极材料,充电时发生下述反应:Li1-xC6+x Li++x e-→ LiC6 其结果是,Li+嵌入石墨的A、B层间,导致石墨的层堆积方式发生改变,形成化学式为LiC6的嵌入化合物。
Ⅰ.下图给出了一个Li+沿C轴投影在A层上的位置,试在下图上标出与该离子临近的其他6个Li+的投影位置
Ⅱ.在LiC6中,Li+与相邻石墨六元环的作用力属于何种键型
Ⅲ.某石墨嵌入化合物每个六元环都对应一个Li+,写出它的化学式
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题。
(1)下面是一种有机物A的合成路线,请回答有关问题:
已知:d的分子式为:C2H4O___________ , f___________ 。
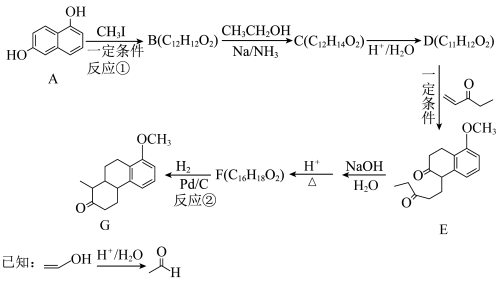
(2)以1,6-二酚(化合物A)为原料合成药物中间体F及其衍生物G的一种路线如下:___________ F___________ 。
(1)下面是一种有机物A的合成路线,请回答有关问题:
已知:d的分子式为:C2H4O
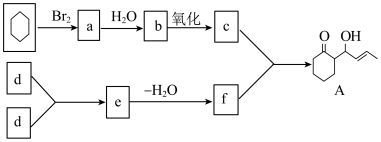
(2)以1,6-二酚(化合物A)为原料合成药物中间体F及其衍生物G的一种路线如下:
您最近一年使用:0次
名校
解题方法
7 . 根据Bronsted酸碱质子理论,酸是能放出质子的物质,碱是能接受质子的物质,酸性或碱性强弱与物质的结构有很大关系,试完成以下各题
(1)下列化合物酸性由大到小的顺序是___________ (填序号)。
①NCCOOH ②CH3CH2COOH ③CH2=CHCOOH ④CH3COOH
(2)已知化合物A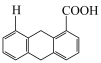 的pKa=6.04,化合物B
的pKa=6.04,化合物B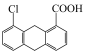 的pKa=6.25,试分析B的pKa比A大的原因
的pKa=6.25,试分析B的pKa比A大的原因___________ 。
(3)已知硝基化合物①CH3CH2CH2NO2 ②(CH3)3CNO2 ③(CH3)2CHNO2。上述三种化合物哪些可溶于NaOH溶液___________ ?其中一种在NaOH溶液中容易与溴作用且生成的溴化物可继续与NaOH溶液作用生成盐,分析该盐的结构简式___________ 。
(1)下列化合物酸性由大到小的顺序是
①NCCOOH ②CH3CH2COOH ③CH2=CHCOOH ④CH3COOH
(2)已知化合物A
 的pKa=6.04,化合物B
的pKa=6.04,化合物B 的pKa=6.25,试分析B的pKa比A大的原因
的pKa=6.25,试分析B的pKa比A大的原因(3)已知硝基化合物①CH3CH2CH2NO2 ②(CH3)3CNO2 ③(CH3)2CHNO2。上述三种化合物哪些可溶于NaOH溶液
您最近一年使用:0次
名校
解题方法
8 . 光催化是新发展的一个催化技术,TiO2是目前研究成功的应用广泛的光催化剂,它是由金红石矿(主要成分为TiO2)先制备为TiCl4,再转化为纯TiO2。
请根据表中数据作答:
(1)计算反应:TiO2(s) + 2Cl2(g)= TiCl4(g) + O2(g) 298K的ΔrΗΘm和ΔrSΘm,该反应能否正向进行___________ ?
(2)计算反应2C(s) + O2(g) = 2CO(g) 298K的ΔrΗΘm和ΔrSΘm,并判据反应在298K进行的方向___________ 。
(3)为得到纯的TiCl4,有人设计如下方案:TiO2(s) + 2Cl2(g) + 2C(s) = TiCl4(g ) + 2CO(g)。计算该反应298K的ΔrΗΘm和ΔrSΘm,并判据反应进行的方向___________ 。
| 物种 | TiO2(s) | TiCl4(g) | Cl2(g) | O2(g) | C(s) | CO(g) |
| ΔrΗΘm /kJ∙molˉ1 | –944.7 | –763.2 | 0 | 0 | 0 | –110.5 |
| SΘm/J∙molˉ1∙Kˉ1 | 55.02 | 354.9 | 223.1 | 205.1 | 5.74 | 197.7 |
(1)计算反应:TiO2(s) + 2Cl2(g)= TiCl4(g) + O2(g) 298K的ΔrΗΘm和ΔrSΘm,该反应能否正向进行
(2)计算反应2C(s) + O2(g) = 2CO(g) 298K的ΔrΗΘm和ΔrSΘm,并判据反应在298K进行的方向
(3)为得到纯的TiCl4,有人设计如下方案:TiO2(s) + 2Cl2(g) + 2C(s) = TiCl4(g ) + 2CO(g)。计算该反应298K的ΔrΗΘm和ΔrSΘm,并判据反应进行的方向
您最近一年使用:0次
名校
解题方法
9 . 根据要求完成下列方程式。
(1)K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,其光解反应的化学方程式为:2K3[Fe(C2O4)3] 2FeC2O4 +3K2C2O4 +2CO2↑。
2FeC2O4 +3K2C2O4 +2CO2↑。
①草酸亚铁在隔绝空气的条件下加热会分解,可以制得黑色粉末状的氧化亚铁,写出该反应的化学方程式___________ 。
②氢氧化亚铁的制备过程中要注意隔绝空气,否则白色沉淀会迅速转化为灰绿色,最后得到红褐色物质,写出该转化过程的化学方程式___________ 。
③高铁酸钠是新型的净水剂,在强碱中氢氧化铁可以被氯气氧化生成紫色的高铁酸根,完成该反应的离子方程式___________ 。
(2)黄血盐(K4[Fe(CN)6] )是合法的食品添加剂,用作抗结剂;黄血盐在溶液中遇到Fe3+ ,生成普鲁士蓝沉淀。
①铊是一种剧毒化学品,若出现了中毒症状,应立即就医,在医学上,医生通常建议中毒者服用一种可溶性普鲁士蓝(KFe[Fe(CN)6])解毒,Tl+ 与K+ 性质接近,铊可置换普鲁士兰中的钾后,形成不溶性物质,随粪便排出,对治疗经口急慢性铊中毒有一定疗效,写出解铊毒反应的离子方程式___________ 。
②无水黄血盐可被浓硫酸分解,生成三种常见的盐和一种常见的无色无味气体,分析完成该反应的化学方程式___________ 。(提示:反应中价态不变)
(3)基于生成滕氏蓝的化学反应原理发展起来的晒制蓝图技术在复印机诞生之前广泛用于工程图纸的复制。赤血盐溶液遇到Fe2+ ,可以生成蓝色的滕氏蓝沉淀,写出得到滕氏蓝沉淀反应的离子方程式___________ 。(已知:氯气遇到黄血盐可以得到赤血盐)
(1)K3[Fe(C2O4)3]·3H2O(三草酸合铁酸钾)为亮绿色晶体,可用于晒制蓝图。晒制蓝图时,用K3[Fe(C2O4)3]·3H2O作感光剂,其光解反应的化学方程式为:2K3[Fe(C2O4)3]
 2FeC2O4 +3K2C2O4 +2CO2↑。
2FeC2O4 +3K2C2O4 +2CO2↑。①草酸亚铁在隔绝空气的条件下加热会分解,可以制得黑色粉末状的氧化亚铁,写出该反应的化学方程式
②氢氧化亚铁的制备过程中要注意隔绝空气,否则白色沉淀会迅速转化为灰绿色,最后得到红褐色物质,写出该转化过程的化学方程式
③高铁酸钠是新型的净水剂,在强碱中氢氧化铁可以被氯气氧化生成紫色的高铁酸根,完成该反应的离子方程式
(2)黄血盐(K4[Fe(CN)6] )是合法的食品添加剂,用作抗结剂;黄血盐在溶液中遇到Fe3+ ,生成普鲁士蓝沉淀。
①铊是一种剧毒化学品,若出现了中毒症状,应立即就医,在医学上,医生通常建议中毒者服用一种可溶性普鲁士蓝(KFe[Fe(CN)6])解毒,Tl+ 与K+ 性质接近,铊可置换普鲁士兰中的钾后,形成不溶性物质,随粪便排出,对治疗经口急慢性铊中毒有一定疗效,写出解铊毒反应的离子方程式
②无水黄血盐可被浓硫酸分解,生成三种常见的盐和一种常见的无色无味气体,分析完成该反应的化学方程式
(3)基于生成滕氏蓝的化学反应原理发展起来的晒制蓝图技术在复印机诞生之前广泛用于工程图纸的复制。赤血盐溶液遇到Fe2+ ,可以生成蓝色的滕氏蓝沉淀,写出得到滕氏蓝沉淀反应的离子方程式
您最近一年使用:0次
名校
解题方法
10 . 反应A+B→P符合Arrhenius公式,[已知Arrhenius经验公式为Rlnk=–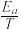 +C(Ea为活化能,k为速率常数,R和C为常数)]。当使用催化剂时,其活化能降低了80kJ·mol-1,在室温(298K)下进行反应时,催化剂使其反应速率常数约提高了倍。
+C(Ea为活化能,k为速率常数,R和C为常数)]。当使用催化剂时,其活化能降低了80kJ·mol-1,在室温(298K)下进行反应时,催化剂使其反应速率常数约提高了倍。
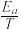 +C(Ea为活化能,k为速率常数,R和C为常数)]。当使用催化剂时,其活化能降低了80kJ·mol-1,在室温(298K)下进行反应时,催化剂使其反应速率常数约提高了倍。
+C(Ea为活化能,k为速率常数,R和C为常数)]。当使用催化剂时,其活化能降低了80kJ·mol-1,在室温(298K)下进行反应时,催化剂使其反应速率常数约提高了倍。| A.2×105 | B.1014 | C.5000 | D.29×1012 |
您最近一年使用:0次



