名校
1 . 钒属于稀有金属,在天然矿物中含量很低。从硫酸厂废弃的钒触媒(主要成分为 、
、 、
、 、
、 )中回收
)中回收 的流程如图所示。
的流程如图所示。
(1)V元素在元素周期表中的位置为___________ 。
(2)“活化焙烧”的目的是使 转化为
转化为 。已知反应过程中
。已知反应过程中 能被
能被 氧化生成
氧化生成 ,
, 自身分解也可以生成
自身分解也可以生成 ,则该步骤所得尾气中硫元素的主要存在形式有
,则该步骤所得尾气中硫元素的主要存在形式有___________ (填化学式)。
(3)常温下稀 溶液的pH
溶液的pH___________ 7(填“>”“<”或“=”,已知 的
的 ,
, ,
, 的
的 )。“浸出”步骤中有
)。“浸出”步骤中有 生成,写出该步骤中
生成,写出该步骤中 转化为
转化为 的离子方程式
的离子方程式___________ 。“活化焙烧”时可能有少量的 未完全转化,推测“浸出”步骤中加入少量
未完全转化,推测“浸出”步骤中加入少量 的主要作用是
的主要作用是___________ 。
(4)“浓缩”后,溶液中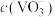 的浓度为0.2mo/L,“沉钒”步骤中钒元素的沉降率为98%,则沉钒后溶液中
的浓度为0.2mo/L,“沉钒”步骤中钒元素的沉降率为98%,则沉钒后溶液中
___________ mol/L[ ,假设沉钒过程中溶液体积不变]。
,假设沉钒过程中溶液体积不变]。
(5)含钒离子在储能领域应用广泛。如图所示的全钒液储能电池装置可实现化学能和电能相互转化,该装置储能时电势高的电极的电极反应式为___________ ,若储能时转移2mol电子,则正极液储罐中 的净变化为
的净变化为___________ mol。
 、
、 、
、 、
、 )中回收
)中回收 的流程如图所示。
的流程如图所示。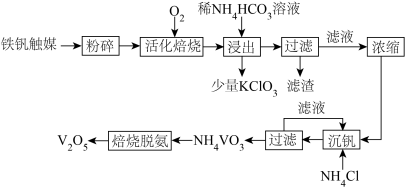
(1)V元素在元素周期表中的位置为
(2)“活化焙烧”的目的是使
 转化为
转化为 。已知反应过程中
。已知反应过程中 能被
能被 氧化生成
氧化生成 ,
, 自身分解也可以生成
自身分解也可以生成 ,则该步骤所得尾气中硫元素的主要存在形式有
,则该步骤所得尾气中硫元素的主要存在形式有(3)常温下稀
 溶液的pH
溶液的pH 的
的 ,
, ,
, 的
的 )。“浸出”步骤中有
)。“浸出”步骤中有 生成,写出该步骤中
生成,写出该步骤中 转化为
转化为 的离子方程式
的离子方程式 未完全转化,推测“浸出”步骤中加入少量
未完全转化,推测“浸出”步骤中加入少量 的主要作用是
的主要作用是(4)“浓缩”后,溶液中
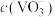 的浓度为0.2mo/L,“沉钒”步骤中钒元素的沉降率为98%,则沉钒后溶液中
的浓度为0.2mo/L,“沉钒”步骤中钒元素的沉降率为98%,则沉钒后溶液中
 ,假设沉钒过程中溶液体积不变]。
,假设沉钒过程中溶液体积不变]。(5)含钒离子在储能领域应用广泛。如图所示的全钒液储能电池装置可实现化学能和电能相互转化,该装置储能时电势高的电极的电极反应式为
 的净变化为
的净变化为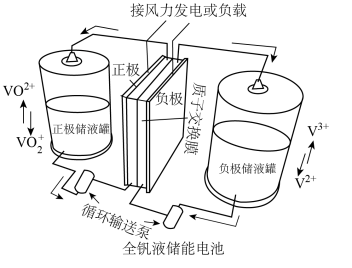
您最近一年使用:0次
2024-05-27更新
|
43次组卷
|
2卷引用:广东省名校教研联盟2023-2024学年高三下学期5月测试化学试题
解题方法
2 . 三位科学家“发现和合成量子点”获得2023年诺贝尔化学奖。量子点又称为半导体荧光纳米晶,主要是由ⅡA-ⅥA族元素(如CdS、CdSe、ZnSe等)和ⅢA-ⅤA族元素(如GaN、InP、InAs等)组成的纳米颗粒,元素周期表从此有了第三个维度。元素周期表反映元素之间的内在联系,是研究物质性质的重要工具。下表列出了a~h8种元素在周期表的位置,请回答下列问题:
(1)某量子点含有e元素。e原子结构示意图为:___________ 。
(2)GaN量子点中的Ga与d同族。Ga与d两种元素最高价氧化物对应的水化物碱性较强的是___________ (填化学式)。
(3)CdSe量子点中的Se是34号元素,在周期表中的位置是___________ ;Se与f的简单氢化物稳定性较弱的是___________ (填化学式)。
(4)单质c在单质b中燃烧火焰呈___________ 色,所得产物的电子式为___________ ,该产物与a的最高价氧化物反应的化学方程式为___________ 。
(5)写出一条能证明h的金属性强于c的实验事实___________ 。
| 周期 | 族 | |||||||
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | a | b | ||||||
| 3 | c | d | e | f | g | |||
| 4 | h | |||||||
(2)GaN量子点中的Ga与d同族。Ga与d两种元素最高价氧化物对应的水化物碱性较强的是
(3)CdSe量子点中的Se是34号元素,在周期表中的位置是
(4)单质c在单质b中燃烧火焰呈
(5)写出一条能证明h的金属性强于c的实验事实
您最近一年使用:0次
3 . 锗是重要的半导体材料,但Ge是地球上最分散的元素之一,被称为“稀散金属”。现利用云南临沧地区富锗的褐煤矿(锗质量分数约为0.01%~0.05%)提取高纯二氧化锗,其工艺流程如图所示:
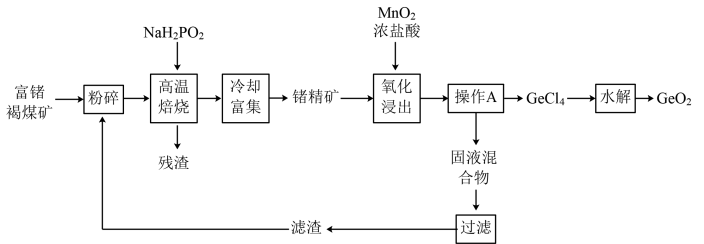
已知含锗化合物的物理性质如下表:
回答下列问题:
(1)Ge的原子序数为32,Ge在元素周期表中的位置是_______ 。
(2)对富锗褐煤矿进行“粉碎”的目的是_______ 。
(3)高温焙烧过程中, 可将
可将 转化为GeO,同时生成
转化为GeO,同时生成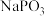 ,试写出该转化过程的化学方程式
,试写出该转化过程的化学方程式_______ 。高温焙烧过程中加入 的目的是
的目的是_______ 。
(4)在“氧化浸出”过程中,反应温度过高时发生的副反应的离子方程式为_______ 。
(5)“氧化浸出”过程中加入过量浓盐酸,其作用除了可以将 转化为
转化为 外,还能
外,还能_______ ,从而提高 的产率。
的产率。
(6)操作A的名称为_______ 。

已知含锗化合物的物理性质如下表:
| 物质 | GeO |  |  |
| 熔点/℃ | 700(升华) | 1116 |  |
| 沸点/℃ | - | 1200 | 86.5 |
回答下列问题:
(1)Ge的原子序数为32,Ge在元素周期表中的位置是
(2)对富锗褐煤矿进行“粉碎”的目的是
(3)高温焙烧过程中,
 可将
可将 转化为GeO,同时生成
转化为GeO,同时生成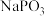 ,试写出该转化过程的化学方程式
,试写出该转化过程的化学方程式 的目的是
的目的是(4)在“氧化浸出”过程中,反应温度过高时发生的副反应的离子方程式为
(5)“氧化浸出”过程中加入过量浓盐酸,其作用除了可以将
 转化为
转化为 外,还能
外,还能 的产率。
的产率。(6)操作A的名称为
您最近一年使用:0次
2022-03-10更新
|
179次组卷
|
2卷引用:广东省珠海市2021-2022学年高三上学期期末考试化学试题
解题方法
4 . 十种元素A~J在元素周期表中的相对位置如表所示:
回答下列问题:
(1)A、C元素组成的常见化合物分别为M和N,其中M含有18个电子。
①M的电子式为______ 。
②实验室制取N的化学方程式为______ 。
(2)元素C、H、J的最高价含氧酸的酸性从强到弱的顺序为______ (用相应酸的化学式表示)。
(3)不同价态的I元素可以相互转化,若反应前后存在4种价态的I元素,写出该反应的化学方程式:______ 。
(4)请用一个化学方程式证明元素D和E的非金属性强弱关系:______ 。
(5)某研究学习小组用如图装置探究F、G的金属性强弱。

当试管(Ⅰ)出现______ 的现象、且试管(Ⅱ)出现______ 的现象时,能说明金属性F大于G,写出试管(Ⅱ)依次发生反应的离子方程式:______ 、_____ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | B | C | D | E | ||||
| 3 | F | G | H | Ⅰ | J | |||
(1)A、C元素组成的常见化合物分别为M和N,其中M含有18个电子。
①M的电子式为
②实验室制取N的化学方程式为
(2)元素C、H、J的最高价含氧酸的酸性从强到弱的顺序为
(3)不同价态的I元素可以相互转化,若反应前后存在4种价态的I元素,写出该反应的化学方程式:
(4)请用一个化学方程式证明元素D和E的非金属性强弱关系:
(5)某研究学习小组用如图装置探究F、G的金属性强弱。

当试管(Ⅰ)出现
您最近一年使用:0次
名校
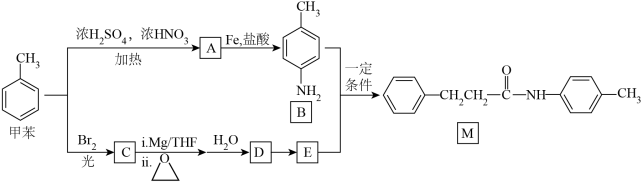
5 . 一种以甲苯为原料合成有机物M的设计路线如下: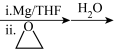
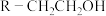
回答下列问题:
(1)B所含官能团的名称是_____ 。
(2)A的名称是_____ ,A→B中加入Fe的目的是_____ 。
(3)甲苯→A的反应类型是_____ ,甲苯→C的化学方程式为_____ 。
(4)在制药行业中常用“成盐修饰”改善物质的理化性质,若用饱和 溶液对E进行“成盐修饰”,可将E转化为
溶液对E进行“成盐修饰”,可将E转化为_____ (用结构简式表示)。
(5)用结构简式表示满足下列条件的D的同分异构体_____ 。
①苯环上只有两个取代基;
②核磁共振氢谱中有6组吸收峰;
③分子中只含有1个手性碳原子
(6)根据已有知识并结合上述合成路线图的相关信息,写出以乙烯为原料,选用必要的无机试剂,合成高分子物质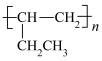 的路线图(请用结构简式表示有机物,用“→”表示转化关系,并在“→”上注明试剂和反应条件)
的路线图(请用结构简式表示有机物,用“→”表示转化关系,并在“→”上注明试剂和反应条件)_____ 。

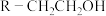
回答下列问题:
(1)B所含官能团的名称是
(2)A的名称是
(3)甲苯→A的反应类型是
(4)在制药行业中常用“成盐修饰”改善物质的理化性质,若用饱和
 溶液对E进行“成盐修饰”,可将E转化为
溶液对E进行“成盐修饰”,可将E转化为(5)用结构简式表示满足下列条件的D的同分异构体
①苯环上只有两个取代基;
②核磁共振氢谱中有6组吸收峰;
③分子中只含有1个手性碳原子
(6)根据已有知识并结合上述合成路线图的相关信息,写出以乙烯为原料,选用必要的无机试剂,合成高分子物质
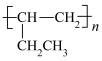 的路线图(请用结构简式表示有机物,用“→”表示转化关系,并在“→”上注明试剂和反应条件)
的路线图(请用结构简式表示有机物,用“→”表示转化关系,并在“→”上注明试剂和反应条件)
您最近一年使用:0次
2023-08-15更新
|
253次组卷
|
4卷引用:广东省珠海市斗门区第一中学2023-2024学年高三上学期阶段性考试化学试题
广东省珠海市斗门区第一中学2023-2024学年高三上学期阶段性考试化学试题广西桂林市2022-2023学年高二下学期期末考试化学试题(已下线)题型04 有机合成设计-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(人教版2019)(已下线)期末押题卷01-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(天津专用)
名校
解题方法
6 . 现以乙烷为主要原料合成化合物G,其合成路线如下图:___________ 。
(2)C的名称是________ ,其官能团名称是_________ ,空间结构是___________ 。
(3)写出B的结构式,并用*标出发生反应②时B的断键位置___________ 。
(4)步骤③的反应类型是___________ ,步骤⑤的反应类型是___________ 。
(5)写出步骤④的化学方程式___________ 。
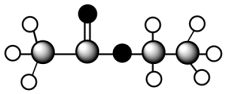
(6)G由C、H、O三种元素组成,球棍模型如下图,则G的结构简式为___________ 。___________ ,写出H可能的结构简式___________ 。

(2)C的名称是
(3)写出B的结构式,并用*标出发生反应②时B的断键位置
(4)步骤③的反应类型是
(5)写出步骤④的化学方程式
(6)G由C、H、O三种元素组成,球棍模型如下图,则G的结构简式为
您最近一年使用:0次
2023-06-27更新
|
149次组卷
|
2卷引用:广东省广州市执信中学2020-2021学年高一下学期期中考试化学试题
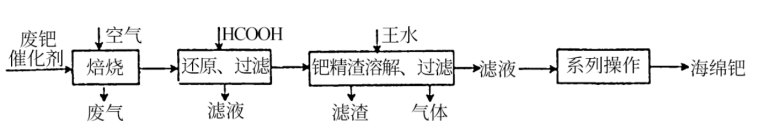
7 . 钯(Pd)是一种不活泼金属,性质与铂相似。含钯催化剂不仅在科研和工业生产中用途广泛,而且用量大,因此从废催化剂中回收钯具有巨大的经济效益。已知某废催化剂的主要成分是钯和活性炭,还含有少量铁、镁、铝、硅、铜等杂质元素,提取海绵钯的工艺流程如下:
(1)Pd的价电子排布式为4d10,指出它在元素周期表中的位置_______ 。
(2)“焙烧”步骤中,通入的空气一定要足量,理由是_______ 。
(3)写出甲酸还原过程发生反应的化学方程式_______ 。
(4)钯在王水中溶解生成化合物X(由3种元素组成)、种无色有毒的气体Y和水。
①如何配置王水_______ 。
②写出钯与王水反应的化学方程式_______ 。
(5)金属钯具有显著的吸氢性能,其密度为12.0g·cm-3。
①在标准状况下,海绵钯吸收氢气的体积约为其体积的840倍,求海绵钯的吸附容量R=_______ (mL·g-1)、氢气的浓度r=_______ (1molPd吸收氢气的物质的量)。
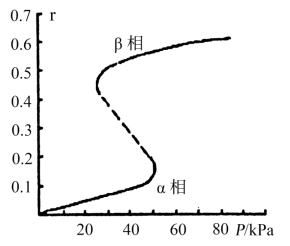
②金属钯中,氢气的r与压强之间的变化关系如图所示,试解释该图的变化趋势_______ 。
(相对原子质量:Pd106.4,理想气体常数R=8.314J·mol-l·K-1)

(1)Pd的价电子排布式为4d10,指出它在元素周期表中的位置
(2)“焙烧”步骤中,通入的空气一定要足量,理由是
(3)写出甲酸还原过程发生反应的化学方程式
(4)钯在王水中溶解生成化合物X(由3种元素组成)、种无色有毒的气体Y和水。
①如何配置王水
②写出钯与王水反应的化学方程式
(5)金属钯具有显著的吸氢性能,其密度为12.0g·cm-3。
①在标准状况下,海绵钯吸收氢气的体积约为其体积的840倍,求海绵钯的吸附容量R=
②金属钯中,氢气的r与压强之间的变化关系如图所示,试解释该图的变化趋势

(相对原子质量:Pd106.4,理想气体常数R=8.314J·mol-l·K-1)
您最近一年使用:0次
名校
解题方法
8 . 氮气及其重要化合物的转化关系如如图,则下列说法正确的是

| A.路线Ⅰ、Ⅱ、Ⅲ是工业生产硝酸的主要途径 |
| B.反应①②③均需要使用催化剂 |
C.路线Ⅲ的另一种反应物为水时,每1mol 反应,转移电子数目为NA 反应,转移电子数目为NA |
D.已知某条件下 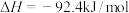 ,该条件下每合成1molNH3放出的热量为46.2kJ ,该条件下每合成1molNH3放出的热量为46.2kJ |
您最近一年使用:0次
2022-10-09更新
|
679次组卷
|
3卷引用:广东省六校2022-2023学年高三上学期第二次联考化学试题
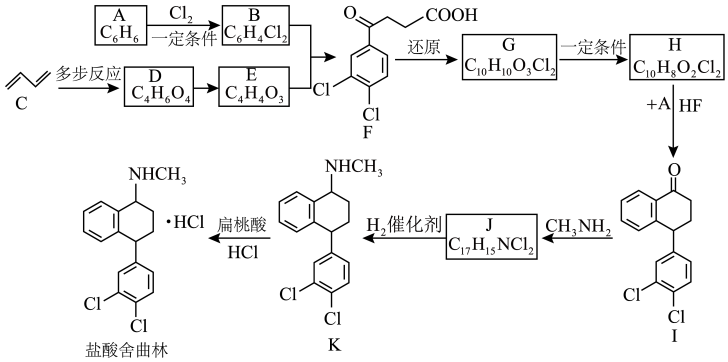
9 . 盐酸舍曲林是一种精神类药物,一种合成盐酸舍曲林的路线如图。
已知:有机化合物的结构可用键线式表示,如(CH3)2NCH2CH3的键线式为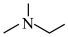 。
。
(1)A→B的反应类型是____ 。
(2)C中所含官能团的名称_____ 。
(3)D属于二元羧酸,E含有五元环,E的核磁共振氢谱只有1组吸收峰。E的键线式是____ 。
(4)H含有1个苯环和1个五元环,G→H的化学方程式是_____ 。
(5)J的结构简式是____ 。
(6)A的一种同系物的分子式是C7H8,其二氯代物有____ 种,写出其中一种含有亚甲基(—CH2—)的结构简式_____ 。
(7)以C(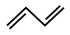 )为起始原料,选用必要的无机试剂合成D,写出合成路线(用结构简式或键线式表示有机化合物,用箭头表示转化关系,箭头上注明试剂和反应条件)
)为起始原料,选用必要的无机试剂合成D,写出合成路线(用结构简式或键线式表示有机化合物,用箭头表示转化关系,箭头上注明试剂和反应条件)_____ 。


已知:有机化合物的结构可用键线式表示,如(CH3)2NCH2CH3的键线式为
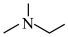 。
。(1)A→B的反应类型是
(2)C中所含官能团的名称
(3)D属于二元羧酸,E含有五元环,E的核磁共振氢谱只有1组吸收峰。E的键线式是
(4)H含有1个苯环和1个五元环,G→H的化学方程式是
(5)J的结构简式是
(6)A的一种同系物的分子式是C7H8,其二氯代物有
(7)以C(
 )为起始原料,选用必要的无机试剂合成D,写出合成路线(用结构简式或键线式表示有机化合物,用箭头表示转化关系,箭头上注明试剂和反应条件)
)为起始原料,选用必要的无机试剂合成D,写出合成路线(用结构简式或键线式表示有机化合物,用箭头表示转化关系,箭头上注明试剂和反应条件)
您最近一年使用:0次
10 . 化学在“三废”治理方面发挥着重要的作用。回答下列问题:
Ⅰ.制革厂含硫废水中主要含有 ,需要对含硫废水进行处理与利用。
,需要对含硫废水进行处理与利用。
(1) 的电子式为
的电子式为___________ ;
(2)废水混合处理不但可以同时处理不同类型的废水,同时可以获得某些化工原料。某地区使用含有硫离子的废水治理含有铜离子的废水,写出该反应的离子方程式___________ 。
(3)部分地区采用空气催化氧化法脱硫。该方法以空气中的氧作为氧化剂,将废水中的 转化为
转化为 ,反应中还原剂与氧化剂的物质的量之比为
,反应中还原剂与氧化剂的物质的量之比为___________ 。
Ⅱ.工业上用烟气制酸的废料(主要含S、Se、 、CuO、ZnO、
、CuO、ZnO、 等)为原料提取硒,流程如图:
等)为原料提取硒,流程如图:
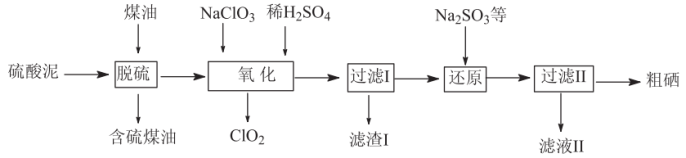
(4)硒与硫是同主族的相邻元素,其在周期表中的位置是___________ 。
(5)“脱硫”过程中,温度控制在95℃,原因是___________ 。
(6)“氧化”过程中,Se转化成弱酸 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
Ⅲ.粗硒经过下列流程可获得亚硒酸钠(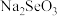 )。
)。
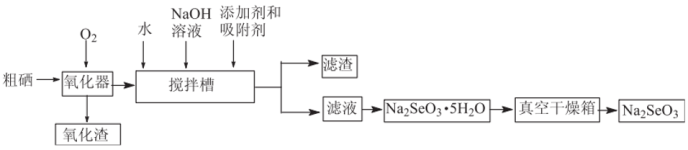
(7)已知在上述合成路线中粗硒在转化为二氧化硒时损失4%,搅拌槽中二氧化硒的利用率为95%,其他损耗忽略不计,试计算利用1t含硒79%的粗硒最终可生产___________ t(精确到0.01t)含亚硒酸钠95%的产品。
Ⅰ.制革厂含硫废水中主要含有
 ,需要对含硫废水进行处理与利用。
,需要对含硫废水进行处理与利用。(1)
 的电子式为
的电子式为(2)废水混合处理不但可以同时处理不同类型的废水,同时可以获得某些化工原料。某地区使用含有硫离子的废水治理含有铜离子的废水,写出该反应的离子方程式
(3)部分地区采用空气催化氧化法脱硫。该方法以空气中的氧作为氧化剂,将废水中的
 转化为
转化为 ,反应中还原剂与氧化剂的物质的量之比为
,反应中还原剂与氧化剂的物质的量之比为Ⅱ.工业上用烟气制酸的废料(主要含S、Se、
 、CuO、ZnO、
、CuO、ZnO、 等)为原料提取硒,流程如图:
等)为原料提取硒,流程如图:
(4)硒与硫是同主族的相邻元素,其在周期表中的位置是
(5)“脱硫”过程中,温度控制在95℃,原因是
(6)“氧化”过程中,Se转化成弱酸
 ,该反应的离子方程式为
,该反应的离子方程式为Ⅲ.粗硒经过下列流程可获得亚硒酸钠(
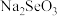 )。
)。
(7)已知在上述合成路线中粗硒在转化为二氧化硒时损失4%,搅拌槽中二氧化硒的利用率为95%,其他损耗忽略不计,试计算利用1t含硒79%的粗硒最终可生产
您最近一年使用:0次



