名校
1 . 氯及其化合物有重要用途,以下是氯元素的“价类二维图”的部分信息。请回答下列问题:
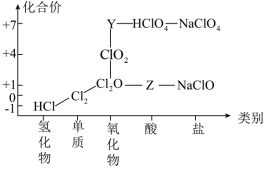
(1)根据图中信息写出Z的化学式_______ 。
(2)已知高氯酸(HClO4)是强酸,写出高氯酸在水中的电离方程式________ 。
(3)氯气既有氧化性又有还原性,结合上图说明理由________ 。
(4)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为2HCl + NaClO = NaCl + Cl2↑ + H2O,在该反应中,氧化剂是_______ ,当生成标准状况下的22.4 L Cl2时,NaClO转移的电子数为_______ 。
(5)某游泳池常用NaClO来抑制藻类生长,工作人员一次错用H2O2消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了O2和NaCl,写出相应的化学方程式_______ 。

(1)根据图中信息写出Z的化学式
(2)已知高氯酸(HClO4)是强酸,写出高氯酸在水中的电离方程式
(3)氯气既有氧化性又有还原性,结合上图说明理由
(4)84消毒液使用说明中特别提醒不可与洁厕灵混合使用,否则会产生氯气,有关反应方程式为2HCl + NaClO = NaCl + Cl2↑ + H2O,在该反应中,氧化剂是
(5)某游泳池常用NaClO来抑制藻类生长,工作人员一次错用H2O2消毒,因两种物质相互反应,使游泳池的藻类疯长。已知该反应产生了O2和NaCl,写出相应的化学方程式
您最近一年使用:0次
2 . 下列物质的性质与用途(或储存方法)都正确且有逻辑关系的是
| A.碱石灰具有吸水性,所以可用于干燥氯气 |
| B.氯气具有强氧化性,所以可用湿润的氯气漂白红纸条 |
| C.过氧化钠为碱性氧化物,所以可用于呼吸面具中吸收二氧化碳 |
| D.钠有较强的还原性,所以可用于钛、锆、铌等金属的冶炼 |
您最近一年使用:0次
3 . 物质的性质决定用途。下列物质的性质和用途不匹配的是
| 选项 | 性质 | 用途 |
| A | 氮气的化学性质稳定 | 常作粮食的保护气 |
| B |  具有漂白性 具有漂白性 | 常作红葡萄酒的保鲜剂 |
| C | 活性炭具有强还原性 | 常作冰箱和汽车的除味剂 |
| D |  具有强氧化性 具有强氧化性 | 常作饮用水的消毒剂 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-16更新
|
218次组卷
|
2卷引用:海南省2023-2024学年高三上学期高考全真模拟卷(四)化学试题
名校
4 . 下列物质的性质与用途(或储存方法)都正确且有逻辑关系的是
| A.碱石灰具有吸水性,所以可用于干燥氯气 |
| B.氯气具有强氧化性,所以可用干燥的氯气漂白红纸条 |
| C.过氧化钠为碱性氧化物,所以可用于呼吸面具中吸收二氧化碳 |
| D.钠有较强的还原性,所以可用于钛、锆、铌等金属的冶炼 |
您最近一年使用:0次
2024-03-25更新
|
29次组卷
|
2卷引用:海南省海口中学2023-2024学年高一上学期期中考试化学试卷
名校
解题方法
5 . 草酸是一种用途广泛的二元有机中强酸,某同学通过查阅资料设计了如图所示的装置(夹持仪器省略)制备一定量的草酸晶体( ),并验证其具有的某些性质。回答下列问题:
),并验证其具有的某些性质。回答下列问题:
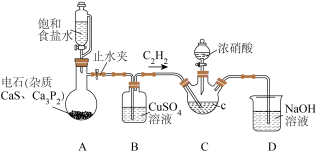
(1)装置B的作用是
 溶液检验有乙炔生成,则气体通过B后应先通入到盛有
溶液检验有乙炔生成,则气体通过B后应先通入到盛有 溶液中。
溶液中。(2)草酸在装置C中生成,反应的化学方程式为
(3)待反应结束后,从C中分离出草酸晶体,然后用0.1000 mol/L的酸性
 溶液进行滴定以测定其纯度。
溶液进行滴定以测定其纯度。①称量3.500 g草酸晶体配制100 mL溶液,下列配制操作中错误的是

②三次平行滴定实验中消耗 溶液的体积如表所示,其中第一次实验滴定后的液面位置如图所示:
溶液的体积如表所示,其中第一次实验滴定后的液面位置如图所示:
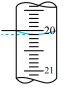
滴定次数 | 待测溶液体积/mL | 标准溶液的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液的体积/mL | ||
第一次 | 20.00 | 0.20 |
| |
第二次 | 20.00 | 2.56 | 28.40 | |
第三次 | 20.00 | 0.22 | 20.32 | |
则
您最近一年使用:0次
6 . 下列仪器和用途对应错误的是
选项 | A | B | C | D |
仪器 |
|
|
|
|
用途 | 蒸发溶液 | 过滤 | 除去气体中杂质 | 配制溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 运用分类的方法研究物质性质及变化的规律是学习化学的有效途径
I.二氧化硅和碳酸钙是牙膏中常用的摩擦剂。
(1)物质分类。判断二氧化硅和碳酸钙所属的物质类别并填入下表(填“酸”“碱”“盐“酸性氧化物”或“碱性氧化物”)。
(2)性质预测。根据用途可推测二氧化硅________ (填“易溶”或“难溶”)于水。根据二氧化硅所属的物质类别,预测其与CaO在高温下反应的化学方程式:________ 。
(3)物质制备。以石灰石为原料制备摩擦剂碳酸钙的实验方案如下:
方案 1:石灰石 生石灰
生石灰 熟石灰
熟石灰 碳酸钙
碳酸钙
方案 2:石灰石 氯化钙
氯化钙 碳酸钙
碳酸钙
①写出方案 2 中石灰石与稀盐酸反应的离子方程式:________ 。
②为了减少碳排放,上述两个方案中,均需回收利用的物质是________ (填化学式);与方案1相比,方案2的优点是________ 。
Ⅱ.可以从不同角度认识化学反应,四种基本反应类型与氧化还原反应的关系如图所示
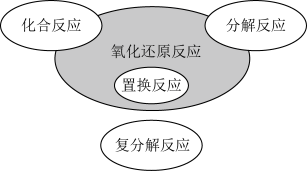
(4)下列化学反应属于阴影区域的是________ (填字母序号)。
a.SO2+H2O2=H2SO4 b.Fe2O3+3CO=2Fe+3CO2
c.2Na2O2+2CO2 = 2Na2CO3+O2 d.Br2+2KI=l2+2KBr
e.2Fe(OH)3=Fe2O3+3H2O
I.二氧化硅和碳酸钙是牙膏中常用的摩擦剂。
(1)物质分类。判断二氧化硅和碳酸钙所属的物质类别并填入下表(填“酸”“碱”“盐“酸性氧化物”或“碱性氧化物”)。
| 摩擦剂 | 二氧化硅 | 磷酸钙 |
| 物质类别 |
(2)性质预测。根据用途可推测二氧化硅
(3)物质制备。以石灰石为原料制备摩擦剂碳酸钙的实验方案如下:
方案 1:石灰石
 生石灰
生石灰 熟石灰
熟石灰 碳酸钙
碳酸钙方案 2:石灰石
 氯化钙
氯化钙 碳酸钙
碳酸钙①写出方案 2 中石灰石与稀盐酸反应的离子方程式:
②为了减少碳排放,上述两个方案中,均需回收利用的物质是
Ⅱ.可以从不同角度认识化学反应,四种基本反应类型与氧化还原反应的关系如图所示

(4)下列化学反应属于阴影区域的是
a.SO2+H2O2=H2SO4 b.Fe2O3+3CO=2Fe+3CO2
c.2Na2O2+2CO2 = 2Na2CO3+O2 d.Br2+2KI=l2+2KBr
e.2Fe(OH)3=Fe2O3+3H2O
您最近一年使用:0次
名校
解题方法
8 . 化学与生活、环境和生产密切相关。下列物质的用途不涉及氧化还原反应的是
| A.用氯气对自来水进行消毒 | B.用氢氧化铝治疗胃酸过多 |
| C.用铁粉作食品脱氧保鲜剂 | D.用氯化铁溶液制作印刷电路铜板 |
您最近一年使用:0次
名校
9 . 铁元素被称为“人类第一元素”,铁及其化合物具有广泛的用途。
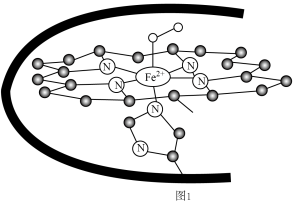
(1)血红蛋白在血液中输送氧气,其结构如图1所示, 的配位数为
的配位数为___________ ,当空气中 浓度较大时,人体会缺氧窒息,甚至死亡,请从配位键的视角分析其原理是
浓度较大时,人体会缺氧窒息,甚至死亡,请从配位键的视角分析其原理是___________ 。
(2)水体中过量的 是一种污染物,可利用纳米铁粉将其除去。相同条件下,向含有
是一种污染物,可利用纳米铁粉将其除去。相同条件下,向含有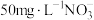 的两份水样中分别加入纳米铁粉、纳米铁粉-活性炭-铜粉,
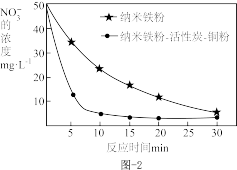
的两份水样中分别加入纳米铁粉、纳米铁粉-活性炭-铜粉, 的去除速率差异如图2所示,产生该差异的可能原因为
的去除速率差异如图2所示,产生该差异的可能原因为___________ 。
(3)铁镁合金是目前储氢密度最高的材料之一,其晶胞结构如图3所示。储氢后, 分子位于晶胞体心和棱的中心位置。该合金储满氢后所得晶体的化学式是
分子位于晶胞体心和棱的中心位置。该合金储满氢后所得晶体的化学式是___________ 。

(4)在生产中,常用 处理
处理 的含
的含 (
( 价)废水得到
价)废水得到 和
和 ,检验产物
,检验产物 常用的试剂是:
常用的试剂是:___________ ; 易被氧化为
易被氧化为 ,请利用核外电子排布的相关原理解释共原因:
,请利用核外电子排布的相关原理解释共原因:___________ 。
(1)血红蛋白在血液中输送氧气,其结构如图1所示,
 的配位数为
的配位数为 浓度较大时,人体会缺氧窒息,甚至死亡,请从配位键的视角分析其原理是
浓度较大时,人体会缺氧窒息,甚至死亡,请从配位键的视角分析其原理是
(2)水体中过量的
 是一种污染物,可利用纳米铁粉将其除去。相同条件下,向含有
是一种污染物,可利用纳米铁粉将其除去。相同条件下,向含有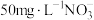 的两份水样中分别加入纳米铁粉、纳米铁粉-活性炭-铜粉,
的两份水样中分别加入纳米铁粉、纳米铁粉-活性炭-铜粉, 的去除速率差异如图2所示,产生该差异的可能原因为
的去除速率差异如图2所示,产生该差异的可能原因为
(3)铁镁合金是目前储氢密度最高的材料之一,其晶胞结构如图3所示。储氢后,
 分子位于晶胞体心和棱的中心位置。该合金储满氢后所得晶体的化学式是
分子位于晶胞体心和棱的中心位置。该合金储满氢后所得晶体的化学式是
(4)在生产中,常用
 处理
处理 的含
的含 (
( 价)废水得到
价)废水得到 和
和 ,检验产物
,检验产物 常用的试剂是:
常用的试剂是: 易被氧化为
易被氧化为 ,请利用核外电子排布的相关原理解释共原因:
,请利用核外电子排布的相关原理解释共原因:
您最近一年使用:0次
10 . 构建美好生活,离不开化学的贡献。下列物质的用途与性质不匹配的是
| 选项 | 用途 | 性质 |
| A | 用 漂白纸浆、毛、丝等 漂白纸浆、毛、丝等 |  具有漂白性 具有漂白性 |
| B | 化妆品中添加甘油作吸湿剂 | 甘油具有较强的吸水性 |
| C | 饮用水中添加 作净水剂 作净水剂 | 铁盐具有较强的还原性 |
| D | 汽车里放活性炭粉作除味剂 | 活泼炭化学性质稳定 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次