1 . VA族元素氮、磷、砷(As)、锑(Sb)、铋(Bi)的单质及其化合物在科研和生产中有许多重要用途。
(1)铋合金可用于自动喷水器的安全塞,铋的价电子排布式为_______ 。
(2)第三周期元素中第一电离能大于磷的元素有_______ (填元素符号)。
(3)Pt(NH3)2C12具有如图所示的两种平面四边形结构(一种有抗癌作用),其中在水中的溶解度较小是_______ (填“顺式”或“反式”)。

(4)偏亚砷酸钠(NaAsO2)是一种灭生性除草剂,其阴离子的立体构型为_______ 。
(5)化肥厂生产的(NH4)2SO4中往往含有少量极易被植物根系吸收的具有正四面体结构的N4H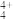 ,其结构式为
,其结构式为_______ ,其中N原子的杂化方式为_______ 。
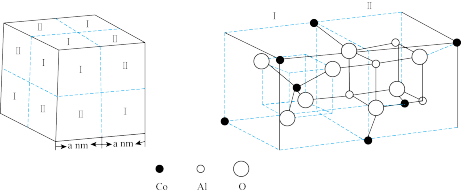
(6)钴蓝晶体结构如下图,该立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,其化学式为_______ ,晶体中Al3+占据O2-形成的_______ (填“四面体空隙”或“八面体空隙”)。
(1)铋合金可用于自动喷水器的安全塞,铋的价电子排布式为
(2)第三周期元素中第一电离能大于磷的元素有
(3)Pt(NH3)2C12具有如图所示的两种平面四边形结构(一种有抗癌作用),其中在水中的溶解度较小是

(4)偏亚砷酸钠(NaAsO2)是一种灭生性除草剂,其阴离子的立体构型为
(5)化肥厂生产的(NH4)2SO4中往往含有少量极易被植物根系吸收的具有正四面体结构的N4H
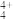 ,其结构式为
,其结构式为(6)钴蓝晶体结构如下图,该立方晶胞由4个Ⅰ型和4个Ⅱ型小立方体构成,其化学式为

您最近一年使用:0次
解题方法
2 . 氧族元素包括氧、硫、硒等,这些元素的单质及其化合物在工农业生产和科学研究中具有广泛的用途。回答下列问题:
(1)下列属于氧原子激发态的轨道表示式的有___________ (填字母,下同),其中失去最外层上一个电子所需能量最低的是___________ 。
a. b.
b.
c.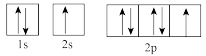 d.
d.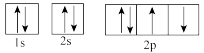
(2)科学研究表明,过硫化氢(也叫二硫化氢)加入烯烃中可制备硫醇,其熔沸点及制备方法如下表所示:
① 的结构为
的结构为 ,其中2个S原子的
,其中2个S原子的___________ 杂化轨道形成S—S___________ (填“ ”或“
”或“ ”)共价键。
”)共价键。
② 分子结构中H—O—O键角为
分子结构中H—O—O键角为 ,则
,则 分子结构中H—S—S键角
分子结构中H—S—S键角___________ (填“=”“>”或“<”) 。
。
③ 的熔沸点比
的熔沸点比 的熔沸点低的原因是
的熔沸点低的原因是___________ 。
(3)在能源逐渐匮乏的形势下,超导材料显得尤为重要。Li、Fe、Se三种元素组成的某新型超导材料的晶胞结构如图所示:
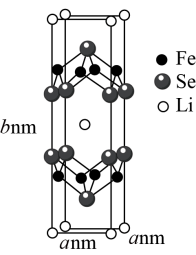
1个晶胞中的Se原子数为___________ 。晶胞的部分参数如图所示,且晶胞棱边夹角均为90°,晶体密度为 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为___________ (列式表示)。
(1)下列属于氧原子激发态的轨道表示式的有
a.
 b.
b.
c.
 d.
d.
(2)科学研究表明,过硫化氢(也叫二硫化氢)加入烯烃中可制备硫醇,其熔沸点及制备方法如下表所示:
| 物质 | 熔点/℃ | 沸点/℃ |  制备方法 制备方法 |
 | -90.0 | 71.0 | 加热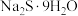 至熔融,再把硫溶入其中,得多硫化钠溶液。在263K下,将该溶液注入稀硫酸中,得多硫化氢混合物,分离、干燥、真空蒸馏,即得 至熔融,再把硫溶入其中,得多硫化钠溶液。在263K下,将该溶液注入稀硫酸中,得多硫化氢混合物,分离、干燥、真空蒸馏,即得 |
 | -0.4 | 150.0 |
 的结构为
的结构为 ,其中2个S原子的
,其中2个S原子的 ”或“
”或“ ”)共价键。
”)共价键。②
 分子结构中H—O—O键角为
分子结构中H—O—O键角为 ,则
,则 分子结构中H—S—S键角
分子结构中H—S—S键角 。
。③
 的熔沸点比
的熔沸点比 的熔沸点低的原因是
的熔沸点低的原因是(3)在能源逐渐匮乏的形势下,超导材料显得尤为重要。Li、Fe、Se三种元素组成的某新型超导材料的晶胞结构如图所示:

1个晶胞中的Se原子数为
 ,则阿伏加德罗常数的值为
,则阿伏加德罗常数的值为
您最近一年使用:0次
名校
解题方法
3 . 甘氨酸亚铁[(H2NCH2COO)2Fe]是新一代畜禽饲料补铁添加剂。某实验小组以碳酸亚铁和甘氨酸反应制备甘氨酸亚铁的装置如下(夹持和加热仪器略去):
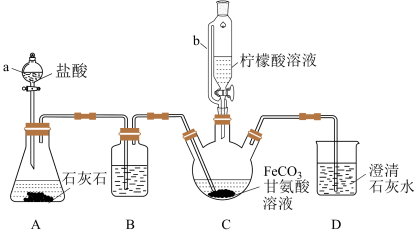
已知:①反应原理为2H2NCH2COOH+FeCO3 (H2NCH2COO)2Fe+CO2↑+H2O。
(H2NCH2COO)2Fe+CO2↑+H2O。
②甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性和酸性。
实验过程:I.装置C中盛有过量的FeCO3和200mL 1.0 mol·L-1甘氨酸溶液。实验时,先打开仪器a的活塞,待装置C中的空气排净后,加热并不断搅拌;然后向三颈烧瓶中滴加柠檬酸溶液。
II.反应结束后过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
(1)装置B中的试剂为_______ 。
(2)装置A制备CO2的用途是_______ 。
(3)向FeSO4溶液中加入NH4HCO3溶液可制得FeCO3,该反应的离子方程式为_______ 。
(4)过程I加入柠檬酸溶液促进FeCO3溶解并调节溶液pH,溶液pH与甘氨酸亚铁产率的关系如图所示。

①pH过低或过高均导致产率下降,pH过高导致产率下降的原因是_______ 。
②柠檬酸溶液除了起酸性作用外,还有的作用是_______ 。
(5)过程II中加入无水乙醇的目的是_______ 。
(6)本实验制得15.3 g甘氨酸亚铁(Mr=204g/mol),则其产率是_______ %。

已知:①反应原理为2H2NCH2COOH+FeCO3
 (H2NCH2COO)2Fe+CO2↑+H2O。
(H2NCH2COO)2Fe+CO2↑+H2O。②甘氨酸易溶于水,微溶于乙醇;甘氨酸亚铁易溶于水,难溶于乙醇。
③柠檬酸易溶于水和乙醇,具有较强的还原性和酸性。
实验过程:I.装置C中盛有过量的FeCO3和200mL 1.0 mol·L-1甘氨酸溶液。实验时,先打开仪器a的活塞,待装置C中的空气排净后,加热并不断搅拌;然后向三颈烧瓶中滴加柠檬酸溶液。
II.反应结束后过滤,将滤液进行蒸发浓缩;加入无水乙醇,过滤、洗涤并干燥。
(1)装置B中的试剂为
(2)装置A制备CO2的用途是
(3)向FeSO4溶液中加入NH4HCO3溶液可制得FeCO3,该反应的离子方程式为
(4)过程I加入柠檬酸溶液促进FeCO3溶解并调节溶液pH,溶液pH与甘氨酸亚铁产率的关系如图所示。

①pH过低或过高均导致产率下降,pH过高导致产率下降的原因是
②柠檬酸溶液除了起酸性作用外,还有的作用是
(5)过程II中加入无水乙醇的目的是
(6)本实验制得15.3 g甘氨酸亚铁(Mr=204g/mol),则其产率是
您最近一年使用:0次
名校
解题方法
4 . 硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰化钾的实验装置如图所示。
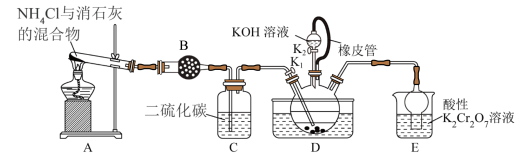
已知:① 不溶于
不溶于 ,
, 密度比水大且不溶于水;
密度比水大且不溶于水;
②三颈烧瓶内盛放: 、水和催化剂;
、水和催化剂;
③ ,该反应比较缓慢且
,该反应比较缓慢且 在高于170℃易分解,而
在高于170℃易分解,而 在105℃就会完全分解。
在105℃就会完全分解。
回答问题:
(1)装置B中的试剂是_______ 。
(2)三颈烧瓶的下层 液体必须浸没导气管口,目的是
液体必须浸没导气管口,目的是_______ 。
(3)制备KSCN溶液:打开 ,加热装置A、D,使A中产生的气体通入D中,发生反应,一段时间后熄灭A处的酒精灯,关闭
,加热装置A、D,使A中产生的气体通入D中,发生反应,一段时间后熄灭A处的酒精灯,关闭 ,保持三颈烧瓶内液温105℃一段时间,然后打开
,保持三颈烧瓶内液温105℃一段时间,然后打开 ,继续保持液温105℃,缓缓滴入适量的KOH溶液。写出装置D中生成KSCN的化学方程式
,继续保持液温105℃,缓缓滴入适量的KOH溶液。写出装置D中生成KSCN的化学方程式_______ 。
(4)装置E的作用为吸收尾气,防止污染环境,写出吸收 时的发生反应的离子方程式
时的发生反应的离子方程式_______ 。
(5)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩、_______ 、过滤、洗涤、干燥,得到硫氰化钾晶体。
(6)测定晶体中KSCN晶体的含量:称取10.0 g样品,配成1000 mL溶液,量取20.00 mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴a作指示剂,用0.1000 mol·L
 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 标准溶液18.00 mL。
标准溶液18.00 mL。
已知:滴定时发生的反应: (白色)。
(白色)。
①滴定过程的指示剂a为_______ 。
②晶体中KSCN的质量分数为_______ 。

已知:①
 不溶于
不溶于 ,
, 密度比水大且不溶于水;
密度比水大且不溶于水;②三颈烧瓶内盛放:
 、水和催化剂;
、水和催化剂;③
 ,该反应比较缓慢且
,该反应比较缓慢且 在高于170℃易分解,而
在高于170℃易分解,而 在105℃就会完全分解。
在105℃就会完全分解。回答问题:
(1)装置B中的试剂是
(2)三颈烧瓶的下层
 液体必须浸没导气管口,目的是
液体必须浸没导气管口,目的是(3)制备KSCN溶液:打开
 ,加热装置A、D,使A中产生的气体通入D中,发生反应,一段时间后熄灭A处的酒精灯,关闭
,加热装置A、D,使A中产生的气体通入D中,发生反应,一段时间后熄灭A处的酒精灯,关闭 ,保持三颈烧瓶内液温105℃一段时间,然后打开
,保持三颈烧瓶内液温105℃一段时间,然后打开 ,继续保持液温105℃,缓缓滴入适量的KOH溶液。写出装置D中生成KSCN的化学方程式
,继续保持液温105℃,缓缓滴入适量的KOH溶液。写出装置D中生成KSCN的化学方程式(4)装置E的作用为吸收尾气,防止污染环境,写出吸收
 时的发生反应的离子方程式
时的发生反应的离子方程式(5)制备KSCN晶体:先滤去三颈烧瓶中的固体催化剂,再减压蒸发浓缩、
(6)测定晶体中KSCN晶体的含量:称取10.0 g样品,配成1000 mL溶液,量取20.00 mL溶液于锥形瓶中,加入适量稀硝酸,再加入几滴a作指示剂,用0.1000 mol·L

 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 标准溶液18.00 mL。
标准溶液18.00 mL。已知:滴定时发生的反应:
 (白色)。
(白色)。①滴定过程的指示剂a为
②晶体中KSCN的质量分数为
您最近一年使用:0次
5 . 氧化还原反应是一类重要的反应,在工农业生产、实验室、日常生活中都有广泛的用途。
(1)实验室用 和浓盐酸制氯气的反应为
和浓盐酸制氯气的反应为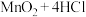 (浓)
(浓)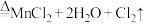
其中还原剂是_____ (填化学式,下同),氧化产物是_____ 。
(2)实验室为监测空气中汞蒸气的含量,往往悬挂涂有 的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为
的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为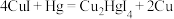
产物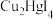 中
中 元素化合价是
元素化合价是_____ 价,上述反应的氧化剂为_____ (填化学式)。
(3)过氧化氢( )俗名双氧水,医疗上可作外科消毒剂。
)俗名双氧水,医疗上可作外科消毒剂。
①双氧水能与酸化的高锰酸钾溶液发生反应: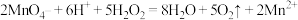 此时双氧水表现出
此时双氧水表现出_____ 性。
②将双氧水加入到 溶液中,溶液出现黄色沉淀(生成了
溶液中,溶液出现黄色沉淀(生成了 单质),该反应的化学方程式为
单质),该反应的化学方程式为_____ 。
(1)实验室用
 和浓盐酸制氯气的反应为
和浓盐酸制氯气的反应为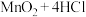 (浓)
(浓)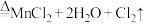
其中还原剂是
(2)实验室为监测空气中汞蒸气的含量,往往悬挂涂有
 的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为
的滤纸,根据滤纸是否变色或颜色发生变化所用去的时间来判断空气中的含汞量,其反应为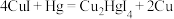
产物
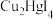 中
中 元素化合价是
元素化合价是(3)过氧化氢(
 )俗名双氧水,医疗上可作外科消毒剂。
)俗名双氧水,医疗上可作外科消毒剂。①双氧水能与酸化的高锰酸钾溶液发生反应:
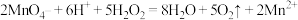 此时双氧水表现出
此时双氧水表现出②将双氧水加入到
 溶液中,溶液出现黄色沉淀(生成了
溶液中,溶液出现黄色沉淀(生成了 单质),该反应的化学方程式为
单质),该反应的化学方程式为
您最近一年使用:0次
解题方法
6 . 明末科学家宋应星出版的《天工开物》中记载了有关“五金”的内容: 黄金美者,其值去黑铁(生铁)一万六千倍,然使釜、鬵(xín,一种炊具)、斤(这里指菜刀、镰刀、锄头等)、斧不呈效于日用之间
黄金美者,其值去黑铁(生铁)一万六千倍,然使釜、鬵(xín,一种炊具)、斤(这里指菜刀、镰刀、锄头等)、斧不呈效于日用之间 贸迁有无,
贸迁有无, 。下列解释错误的是
。下列解释错误的是
 黄金美者,其值去黑铁(生铁)一万六千倍,然使釜、鬵(xín,一种炊具)、斤(这里指菜刀、镰刀、锄头等)、斧不呈效于日用之间
黄金美者,其值去黑铁(生铁)一万六千倍,然使釜、鬵(xín,一种炊具)、斤(这里指菜刀、镰刀、锄头等)、斧不呈效于日用之间 贸迁有无,
贸迁有无, 。下列解释错误的是
。下列解释错误的是| A.明代使用的釜、鬵一类的炊具都属于青铜合金 |
| B.添加了铬、镍的不锈钢菜刀和农具使用后若不保养,也会生锈 |
| C.金属的另一个用途就是铸成钱币作为贸易交往中的流通手段 |
| D.黑铁在空气中发生的腐蚀主要是电化学腐蚀 |
您最近一年使用:0次
7 . 钒(V)是一种重要的金属,有金属“维生素”之称,用途涵盖了航空航天、电池、光学、医药等众多领域,主要由五氧化二钒冶炼得到。某种由钒精矿(含 及少量MgO、
及少量MgO、 等杂质)提取五氧化二钒的工艺流程如图所示。
等杂质)提取五氧化二钒的工艺流程如图所示。
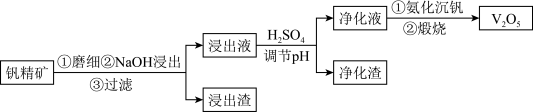
[资料]1:+5价钒在溶液中的主要存在形式与溶液pH的关系:
[资料]2: 能溶于强碱
能溶于强碱
(1)钒精矿磨细的目的是______________________________ 。
(2)浸出液中含有钒酸钠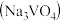 ,请写出相关的化学方程式:
,请写出相关的化学方程式:____________________ 。
(3)浸出渣的成分主要是:__________ 。
(4) 中V的化合价为:
中V的化合价为: __________ .
(5)用硫酸缓慢调节浸出液的pH为7,得到净化液中主要的阴离子是__________ 。
 及少量MgO、
及少量MgO、 等杂质)提取五氧化二钒的工艺流程如图所示。
等杂质)提取五氧化二钒的工艺流程如图所示。
[资料]1:+5价钒在溶液中的主要存在形式与溶液pH的关系:
| pH | 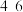 |  |  | 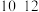 |
| 主要离子 | VO | VO | V2O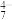 | VO |
 能溶于强碱
能溶于强碱(1)钒精矿磨细的目的是
(2)浸出液中含有钒酸钠
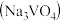 ,请写出相关的化学方程式:
,请写出相关的化学方程式:(3)浸出渣的成分主要是:
(4)
 中V的化合价为:
中V的化合价为: (5)用硫酸缓慢调节浸出液的pH为7,得到净化液中主要的阴离子是
您最近一年使用:0次
解题方法
8 . 砷(As)与磷同主族,砷的化合物在药物,半导体,科研中具有较为广泛的用途。回答下列问题:
(1)基态磷原子的核外电子排布式是____ ,基态砷原子的价电子中有____ 个未成对电子。
(2)As,Se为同周期相邻元素,则第一电离能:As_______ Se(填“>”“<”或“=”)。
(3)在 存在下,将适量的乙炔气体通入
存在下,将适量的乙炔气体通入 溶液中可得到
溶液中可得到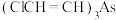 。
。
① 的熔沸点低,易升华,原因是
的熔沸点低,易升华,原因是_______ 。
② 在蒸气状态下存在双聚氯化铝[
在蒸气状态下存在双聚氯化铝[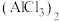 ],结构如图所示,双聚氧化铝中存在配位键,该配位键形成时,提供孤对电子的原子是
],结构如图所示,双聚氧化铝中存在配位键,该配位键形成时,提供孤对电子的原子是_______ (用元素符号表示)。

③800℃时,双聚氯化铝完全分解为 ,单分子
,单分子 的空间构型是
的空间构型是_______ ,而 的空间构型是
的空间构型是_______ 。
(4)砷化镓是一种新型的半导体材料,其晶胞结构如图1所示,图2为晶胞沿z轴的平面投影图,图中a点的原子坐标为 ,则b点的原子坐标为
,则b点的原子坐标为_______ 。

(1)基态磷原子的核外电子排布式是
(2)As,Se为同周期相邻元素,则第一电离能:As
(3)在
 存在下,将适量的乙炔气体通入
存在下,将适量的乙炔气体通入 溶液中可得到
溶液中可得到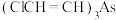 。
。①
 的熔沸点低,易升华,原因是
的熔沸点低,易升华,原因是②
 在蒸气状态下存在双聚氯化铝[
在蒸气状态下存在双聚氯化铝[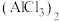 ],结构如图所示,双聚氧化铝中存在配位键,该配位键形成时,提供孤对电子的原子是
],结构如图所示,双聚氧化铝中存在配位键,该配位键形成时,提供孤对电子的原子是
③800℃时,双聚氯化铝完全分解为
 ,单分子
,单分子 的空间构型是
的空间构型是 的空间构型是
的空间构型是(4)砷化镓是一种新型的半导体材料,其晶胞结构如图1所示,图2为晶胞沿z轴的平面投影图,图中a点的原子坐标为
 ,则b点的原子坐标为
,则b点的原子坐标为
您最近一年使用:0次
名校
解题方法
9 . 磷、碳、氢、氧等非金属及其化合物用途广泛。回答下列问题:
(1)白磷(P4)在氯气中燃烧可生成PCl3和PCl5。
①31 g白磷(P4)中含有化学键的数目为_______ 。(用NA表示阿伏伽德罗常数的值)
②形成PCl5时,P原子的一个3s电子激发入3d轨道后参与成键,该激发态的价电子排布式为_______ 。
③研究表明,在加压条件下PCl5于148℃液化时能发生与水类似的自耦电离,形成一种能导电的熔体,其电离方程式为_______ ,产生的阳离子的空间结构为_______ 。
(2)分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为  )。一种观点认为,苯酚羟基中的O原子是sp2杂化则苯酚中的大π键可表示为
)。一种观点认为,苯酚羟基中的O原子是sp2杂化则苯酚中的大π键可表示为_______ ,一定在同一平面上的原子有_______ 个;乙醇显中性而苯酚显酸性的原因是:在大π键中氧的p电子云向苯环转移,_______ 。
(3)可溶性普鲁士蓝晶体属立方晶系,晶胞棱长为a pm,铁-氰骨架组成的小立方体中,Fe粒子在顶点,CN—在棱上,两端均与Fe相连,立方体中心空隙可容纳K+,如图所示(CN—在图中省略)。
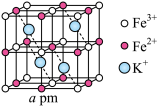
①该化合物的化学式为_______ 。
②若所有铁粒子均视为等径小球,则K+与Fe2+之间最近距离为_______ pm;该晶体的密度为_______ g•cm-3(阿伏加德罗常数为NA)
(1)白磷(P4)在氯气中燃烧可生成PCl3和PCl5。
①31 g白磷(P4)中含有化学键的数目为
②形成PCl5时,P原子的一个3s电子激发入3d轨道后参与成键,该激发态的价电子排布式为
③研究表明,在加压条件下PCl5于148℃液化时能发生与水类似的自耦电离,形成一种能导电的熔体,其电离方程式为
(2)分子中的大π键可用符号
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为  )。一种观点认为,苯酚羟基中的O原子是sp2杂化则苯酚中的大π键可表示为
)。一种观点认为,苯酚羟基中的O原子是sp2杂化则苯酚中的大π键可表示为(3)可溶性普鲁士蓝晶体属立方晶系,晶胞棱长为a pm,铁-氰骨架组成的小立方体中,Fe粒子在顶点,CN—在棱上,两端均与Fe相连,立方体中心空隙可容纳K+,如图所示(CN—在图中省略)。

①该化合物的化学式为
②若所有铁粒子均视为等径小球,则K+与Fe2+之间最近距离为
您最近一年使用:0次
名校
解题方法
10 . 化学与生活密切相关,下列物质与其用途不符合的是
| A.纯碱——治疗胃酸过多 | B.次氯酸钠——消毒剂 |
| C.过氧化钠——漂白剂 | D.小苏打——制作馒头和面包的膨松剂 |
您最近一年使用:0次
2023-04-04更新
|
91次组卷
|
3卷引用:海南省海口市秀英区某校2023-2024学年高一上学期期中检测化学试题



