名校
解题方法
1 . 现有五种元素A、B、C、D、E,其中A、B、C为三个不同周期的短周期元素,E为第四周期元素.请根据下列相关信息,回答下列问题:
(1)C基态原子中能量最高的电子,其电子云在空间有____ 个方向,原子轨道呈__________ 形,C简单离子核外有______ 种运动状态不同的电子.
(2) 难溶于
难溶于 ,简要说明理由:
,简要说明理由:________________ .
(3) 分子的空间构型为
分子的空间构型为__________ ,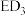 分子的
分子的 模型名称为
模型名称为__________ .
(4)下列气态分子 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为_______________ .
| 元素 | 相关信息 |
| A | 核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B | 原子核外p电子数与s电子数相等 |
| C | 基态原子的价电子排布为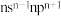 |
| D | 能层数与C相同,且电负性比C大 |
| E | 元素的主族序数与周期数的差为1,且第一电离能比同周期相邻两种元素都大 |
(2)
 难溶于
难溶于 ,简要说明理由:
,简要说明理由:(3)
 分子的空间构型为
分子的空间构型为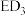 分子的
分子的 模型名称为
模型名称为(4)下列气态分子
 和
和 中,其键角由大到小的顺序为
中,其键角由大到小的顺序为
您最近一年使用:0次
名校
2 . 下列实验的反应原理用离子方程式表示正确的是
A.氯化铜溶液中通入硫化氢: |
B.用铜作电极电解 溶液: 溶液: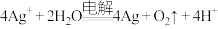 |
C.向 悬浊液中滴加 悬浊液中滴加 溶液,白色沉淀变成黑色: 溶液,白色沉淀变成黑色: |
D.泡沫灭火器的反应原理: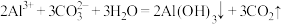 |
您最近一年使用:0次
名校
3 . 设 为阿伏加德罗常数的值.下列说法正确的是
为阿伏加德罗常数的值.下列说法正确的是
 为阿伏加德罗常数的值.下列说法正确的是
为阿伏加德罗常数的值.下列说法正确的是A.电解精炼铜时,若阴极析出 铜,则阳极失电子数大于 铜,则阳极失电子数大于 |
B. 蔗糖溶液中所含分子数等于 蔗糖溶液中所含分子数等于 |
C.氢氧燃料电池工作时,正极消耗 气体,电路中转移电子数为 气体,电路中转移电子数为 |
D. 时, 时, 的 的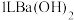 溶液中含有的 溶液中含有的 数目为 数目为 |
您最近一年使用:0次
名校
4 . 下列事实不能用勒夏特列原理解释的是
A.在 的气流中加热 的气流中加热 制备无水 制备无水 |
B. 溶液中加入少量 溶液中加入少量 固体后颜色变深 固体后颜色变深 |
C.一定条件下,当反应 达到平衡后,缩小容积,气体颜色加深 达到平衡后,缩小容积,气体颜色加深 |
D.分别用等体积的蒸馏水和稀盐酸洗涤 沉淀,后者 沉淀,后者 损失少 损失少 |
您最近一年使用:0次
名校
5 . 化学与生产、生活、科技等密切相关。下列说法不正确的是
A.用 溶液和 溶液和 溶液反应可制取硫化铝 溶液反应可制取硫化铝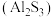 |
| B.牙膏中添加氟化物用于预防龋齿 |
| C.处理锅炉水垢中的硫酸钙,可以先用饱和碳酸钠溶液浸泡,再用酸除去 |
D. 可用作白色颜料和阻燃剂等,在实验室中可用 可用作白色颜料和阻燃剂等,在实验室中可用 的水解反应制取 的水解反应制取 |
您最近一年使用:0次
解题方法
6 . 防疫所用普通体温计中装有金属汞,汞的一种同位素为 。下列关于
。下列关于 的说法错误的是
的说法错误的是
 。下列关于
。下列关于 的说法错误的是
的说法错误的是| A.质子数为80 | B.核外电子数为80 | C.核电荷数为120 | D.中子数为120 |
您最近一年使用:0次
7 . 有以下物质:①石墨;②钠:③酒精;④氨气;⑤硫化氢;⑥碳酸氢钠固体;⑦氢氧化钡溶液;⑧纯醋酸;⑨氧化钠固体;⑩液态氯化氢。
(1)其中能导电的是___________ ;属于非电解质的是___________ 。
(2)等质量④和⑤中氢原子的数目之比为___________ ;若④和⑤中所含氢原子数相等,则④和⑤的质量之比为___________ 。
(3)写出⑥和⑩在水溶液中的离子方程式___________ 。
(4)雷雨天闪电时空气中有O3生成。O2与O3的关系是互为___________ ,等质量的O2和O3的分子数之比为___________ 。
(5)高温下Al粉与Fe2O3发生置换反应生成Fe,该反应能用来焊接钢轨,其中被还原的物质是___________ (填化学式)。NaOH溶液可检验反应后的固体中是否有Al残留,用离子方程式说明其原理___________ 。
(1)其中能导电的是
(2)等质量④和⑤中氢原子的数目之比为
(3)写出⑥和⑩在水溶液中的离子方程式
(4)雷雨天闪电时空气中有O3生成。O2与O3的关系是互为
(5)高温下Al粉与Fe2O3发生置换反应生成Fe,该反应能用来焊接钢轨,其中被还原的物质是
您最近一年使用:0次
8 . 分别向500mL浓度均为2molL的盐酸和NaOH溶液中加入5.4g金属铝,充分反应产生的气体在同温同压下体积比为
| A.1:6 | B.2:3 | C.3:2 | D.1:1 |
您最近一年使用:0次
9 .  代表阿伏加德罗常数的值,下列叙述不正确的是
代表阿伏加德罗常数的值,下列叙述不正确的是
 代表阿伏加德罗常数的值,下列叙述不正确的是
代表阿伏加德罗常数的值,下列叙述不正确的是A.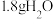 中含有的质子数为 中含有的质子数为 |
B.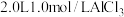 溶液中 溶液中 的数目小于 的数目小于 |
C. 时, 时, 为12的 为12的 溶液中含有 溶液中含有 数目为 数目为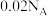 |
D. 和 和 于密闭容器中充分反应后,容器中分子总数为 于密闭容器中充分反应后,容器中分子总数为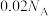 |
您最近一年使用:0次
解题方法
10 . 用一种试剂可以区别 五种溶液的试剂是
五种溶液的试剂是
 五种溶液的试剂是
五种溶液的试剂是| A.盐酸 | B. 溶液 溶液 | C.氨水 | D. 溶液 溶液 |
您最近一年使用:0次



