解题方法
1 . I.高铁酸盐是一种新型、高效、多功能绿色水处理剂,工业上可用湿法制备高铁酸钾:2Fe(OH)3+3ClO-+4OH-=2FeO +3Cl-+5H2O。
+3Cl-+5H2O。
(1)FeO 中铁元素的化合价为
中铁元素的化合价为___________ ,在该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)请用单线桥表示反应中电子转移情况:___________ 。
(3)在下列反应中,水既不作氧化剂又不作还原剂是___________(填序号)。
II.为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素。请按题目要求回答下列问题:___________ (填元素符号);它在周期表中的位置为___________ 。
(5)上述元素对应的单质中,既能与酸反应又能与碱反应的是___________ (填化学式),写出该单质与氢氧化钠反应的离子方程式___________ 。
 +3Cl-+5H2O。
+3Cl-+5H2O。(1)FeO
 中铁元素的化合价为
中铁元素的化合价为(2)请用单线桥表示反应中电子转移情况:
(3)在下列反应中,水既不作氧化剂又不作还原剂是___________(填序号)。
A.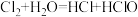 | B. |
C. | D. |
II.为了庆祝元素周期表诞生150周年,联合国将2019年定为“国际化学元素周期表年”。元素周期表反映了元素之间的内在联系,是学习、研究和应用化学的一种重要工具。下表是元素周期表的一部分,数字①~⑦代表前四周期七种主族元素。请按题目要求回答下列问题:

(5)上述元素对应的单质中,既能与酸反应又能与碱反应的是
您最近一年使用:0次
2 . 铁在地壳中含量丰富,也是重要的人体微量元素之一。下列有关说法正确的是
| A.铁与水蒸气反应生成氢氧化铁和氢气 |
| B.为了防止缺铁性贫血,麦片中可以添加微量的还原铁粉 |
| C.将饱和FeCl3溶液滴入沸水中,小心加热后制得红褐色Fe(OH)3胶体 |
| D.取新鲜菠菜切开表皮,在内部组织上滴加KSCN溶液,无颜色变化说明菠菜不含铁 |
您最近一年使用:0次
3 . 中华文明源远流长。下列文物的材质属于合金的是
| |
|
|
| A.三星堆青铜面具 | B.仰韶文化彩陶壶 | C.元代青花瓷 | D.西汉素纱衣 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 下列离子方程式正确的是
| A.Na2O2放入水中:Na2O2+H2O=2Na++2OH-+O2↑ |
| B.Na投入FeSO4溶液:2Na+Fe2+=2Na++Fe |
| C.用铝粉和NaOH溶液反应制取少量H2:Al+OH-+3H2O=2[Al(OH)4]-+3H2↑ |
D.向AlCl3溶液中滴加足量氨水:Al3++3NH3·H2O=Al(OH)3↓+3NH |
您最近一年使用:0次
解题方法
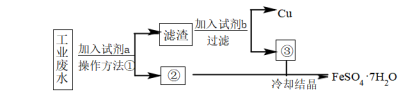
5 . 某工厂的酸性废水中含有大量的 FeSO4和较多的 Cu2+。为了减少污染并变废为宝, 工厂计划从该废水中回收 FeSO4和金属铜。请根据以下流程图,回答下列问题。___________ ,加入试剂 b是___________ (填写试剂化学式)。
(2)为保证反应完全,流程中加入的试剂a、b均过量,溶液③中所含的阳离子有___________ (填写离子符号)。
(3)若取2mL 溶液②加入试管中,然后滴加氢氧化钠溶液,产生的现象___________ 。
(4)若取少量溶液②加入试管中,滴加一定量的 H2O2,写出反应离子方程式___________ 。
(5)产品取样研究:取 20g FeSO4·7H2O 产品加水溶解,滴加0.2mol/LBaCl2 溶液至不再产生沉淀,共消耗 BaCl2 溶液250mL,计算取样产品的纯度___________ 。
(2)为保证反应完全,流程中加入的试剂a、b均过量,溶液③中所含的阳离子有
(3)若取2mL 溶液②加入试管中,然后滴加氢氧化钠溶液,产生的现象
(4)若取少量溶液②加入试管中,滴加一定量的 H2O2,写出反应离子方程式
(5)产品取样研究:取 20g FeSO4·7H2O 产品加水溶解,滴加0.2mol/LBaCl2 溶液至不再产生沉淀,共消耗 BaCl2 溶液250mL,计算取样产品的纯度
您最近一年使用:0次
6 . 某同学按下列步骤配制500 mL 0.2 mol·L-1Na2SO4溶液,完成表格并回答有关问题。
(1)填写步骤中的空白。
(2)上述实验中使用容量瓶前应___________ 。
(3)取出该Na2SO4溶液10 mL加水稀释到100 mL,稀释后溶液中Na+的物质的量浓度是___________ 。
(4)上述配制溶液的过程缺少步骤⑤,⑤是___________ 。
(5)在实验中,以下操作造成实验结果偏低的是___________(填字母)。
(1)填写步骤中的空白。
| 实验步骤 | 有关问题 |
| ①计算所需Na2SO4固体的质量 | 需要称量Na2SO4固体的质量为 |
| ②称量Na2SO4固体 | 称量需要用到的主要仪器是 |
| ③将Na2SO4固体加入200 mL烧杯中,并加入适量水 | 为了加快溶解速率,用玻璃棒搅拌 |
| ④将烧杯中溶液转移至500 mL容量瓶中 | 为了防止溶液溅出,应采取的措施是: |
| ⑥向容量瓶中加蒸馏水至刻度线 | 在进行此操作时当加水至刻度线以下1~2厘米处接下来应如何操作: |
(3)取出该Na2SO4溶液10 mL加水稀释到100 mL,稀释后溶液中Na+的物质的量浓度是
(4)上述配制溶液的过程缺少步骤⑤,⑤是
(5)在实验中,以下操作造成实验结果偏低的是___________(填字母)。
| A.在转移溶液时有液体溅到容量瓶外 |
| B.定容时仰视刻度线 |
| C.转移前没有将使用的容量瓶烘干 |
| D.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管加蒸馏水至刻度线 |
您最近一年使用:0次
7 . 下列粒子中,与OH-具有相同质子数和电子数的是
| A.Cl- | B.F- | C.NH3 | D.NH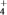 |
您最近一年使用:0次
8 . 科学家指出:多种海产品如虾、蟹、牡蛎等,体内含有+5价的砷(33As),它对人体是无毒的,但+3价的砷有毒。下列有关说法错误的是
| A.砷元素是第VA元素,原子最外层有5个电子 |
| B.+5价的砷有氧化性 |
| C.砷从+5价转变为+3价,发生还原反应 |
| D.从合理膳食的角度,建议食用大量海鲜时饮用富含维生素 C(有还原性) 的饮料 |
您最近一年使用:0次
9 . 侯氏制碱法的第一步反应为CO2+NH3+NaCl+H2O=NH4Cl+NaHCO3↓。用NA表示阿伏加德罗常
的数值,下列说法正确的是
的数值,下列说法正确的是
| A.44 g CO2含有的分子数为3 NA | B.1 mol NH3含有的氢原子数为NA |
| C.1 mol NaCl固体中含有的Na+数目为NA | D.标准状况下,2.24LH2O含有的分子数为0.1 NA |
您最近一年使用:0次
10 . 某无色透明的酸性溶液中,能大量共存的离子组是
A.Mg2+、Na+、SO 、Cl− 、Cl− | B.Na+、K+、MnO 、OH− 、OH− |
C.Ba2+、Al3+、NO 、SO 、SO | D.Na+、Fe2+、Cl−、CO |
您最近一年使用:0次







