名校
解题方法
1 . 可逆反应 在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
 在不同条件下的化学反应速率如下,其中表示的反应速率最快的是
在不同条件下的化学反应速率如下,其中表示的反应速率最快的是A. | B.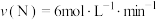 |
C.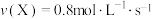 | D.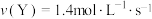 |
您最近一年使用:0次
名校
2 . 关于铅蓄电池,下列说法正确的是
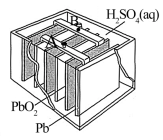
A.放电时,溶液中 移向Pb电极 移向Pb电极 |
B.放电时,负极的电极反应式为 |
| C.该电池工作时,电能转化为化学能 |
| D.放电时,正极电极质量增加 |
您最近一年使用:0次
解题方法
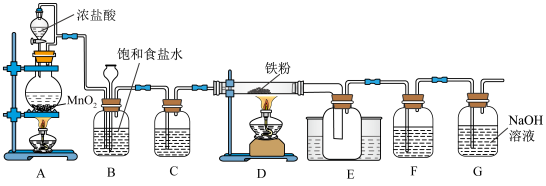
3 . 氯化铁是一种重要的工业试剂,可用于五金刻蚀、污水处理、催化剂等。实验室用纯净的氯气和铁粉制备氯化铁固体的装置如图所示。
(1)实验装入药品前,应该_______ 。
(2)装置A中盛放MnO2的仪器名称为_______ ,装置A中发生反应的化学方程式为_______ 。
(3)装置B中饱和食盐水的作用是_______ 。
(4)实验时应该先点燃_______ 处的酒精灯(填“A”或者“D”),理由是_______ 。
(5)装置C、F中所装试剂为浓 ,是否能去掉装置F
,是否能去掉装置F_______ (填“是”或者“否”),理由是_______ 。
(6)装置G的作用为_______ 。
(1)实验装入药品前,应该
(2)装置A中盛放MnO2的仪器名称为
(3)装置B中饱和食盐水的作用是
(4)实验时应该先点燃
(5)装置C、F中所装试剂为浓
 ,是否能去掉装置F
,是否能去掉装置F(6)装置G的作用为
您最近一年使用:0次
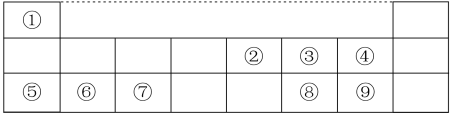
4 . 下表是元素周期表的一部分,数字①~⑨代表九种常见的短周期元素,请按题目要求回答下列问题:_______ 周期第_______ 族,元素⑦的离子结构示意图_______ 。
(2)元素③、④、⑧的简单气态氢化物稳定性由强到弱的顺序是:_______ (用化学式表示)。
(3)元素①、②、⑨形成的常见化合物中含有的化学键类型有_______ (填“离子键”“极性键”“非极性键”),③、④、⑤、⑥四种元素形成的简单离子,半径最大的是_______ (填离子符号)。
(4)用以下对比实验探究Mg、Al的金属性强弱以及Cl、I的非金属性强弱。
(2)元素③、④、⑧的简单气态氢化物稳定性由强到弱的顺序是:
(3)元素①、②、⑨形成的常见化合物中含有的化学键类型有
(4)用以下对比实验探究Mg、Al的金属性强弱以及Cl、I的非金属性强弱。
| 比较Mg、Al金属性强弱 | 比较Cl、I非金属性强弱 |
| 试剂:水、酚酞 | 试剂:新制氯水、KI溶液 |
| 操作:向两支试管中加入打磨好的镁片和铝片,分别加入2 mL水,并滴入两滴酚酞溶液,加热试管至液体沸腾 | 操作:向盛有4 mLKI溶液的试管中加入1 mL新制氯水,振荡 |
| 现象:Mg片表面逐渐产生气泡,溶液变为浅红色,铝片的表面和溶液无明显变化 | 现象: 离子方程式: |
| 结论: | 结论:非金属性C1大于I |
您最近一年使用:0次
5 . 生产、生活中处处有化学,利用所学化学知识回答下列问题。
(1) 气体是一种高效、环保的消毒剂,可代替氯气用于饮用水的消毒。对水进行消毒时,还可将水中的
气体是一种高效、环保的消毒剂,可代替氯气用于饮用水的消毒。对水进行消毒时,还可将水中的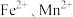 等转化为
等转化为 和
和 等难溶物除去,由此说明
等难溶物除去,由此说明 具有
具有_______ 性。
(2)工业上可以通过 与
与 反应的方法制取
反应的方法制取 ,请完成该化学反应方程式:
,请完成该化学反应方程式: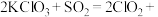
_______ 。
(3)查阅资料显示: 处理污水后的还原产物为
处理污水后的还原产物为 ,检验处理后的溶液中是否存在
,检验处理后的溶液中是否存在 的方法是
的方法是_______ 。
(4)为验证次氯酸光照分解的产物,分别利用氯离子传感器、 传感器、氧气传感器采集数据并绘制变化图像如下,其中能表示氯水的
传感器、氧气传感器采集数据并绘制变化图像如下,其中能表示氯水的 随时间变化的图像是
随时间变化的图像是_______ (填字母),用化学方程式说明这一变化的原因_______ 。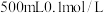 的稀盐酸,
的稀盐酸,
①需要用量筒量取 的稀盐酸
的稀盐酸_______  。
。
②需要用到的玻璃仪器除烧杯、量筒、胶头滴管、玻璃棒外,还需要_______ 。
③下列操作会使配制的溶液物质的量浓度偏低的是_______ 。
A.定容时俯视容量瓶刻度线 B.容量瓶用蒸馏水洗涤后未干燥
C.未将洗涤液转移进容量瓶 D.定容时水加多了用胶头滴管吸出
E.摇匀静置,液面下降
(1)
 气体是一种高效、环保的消毒剂,可代替氯气用于饮用水的消毒。对水进行消毒时,还可将水中的
气体是一种高效、环保的消毒剂,可代替氯气用于饮用水的消毒。对水进行消毒时,还可将水中的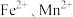 等转化为
等转化为 和
和 等难溶物除去,由此说明
等难溶物除去,由此说明 具有
具有(2)工业上可以通过
 与
与 反应的方法制取
反应的方法制取 ,请完成该化学反应方程式:
,请完成该化学反应方程式: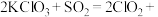
(3)查阅资料显示:
 处理污水后的还原产物为
处理污水后的还原产物为 ,检验处理后的溶液中是否存在
,检验处理后的溶液中是否存在 的方法是
的方法是(4)为验证次氯酸光照分解的产物,分别利用氯离子传感器、
 传感器、氧气传感器采集数据并绘制变化图像如下,其中能表示氯水的
传感器、氧气传感器采集数据并绘制变化图像如下,其中能表示氯水的 随时间变化的图像是
随时间变化的图像是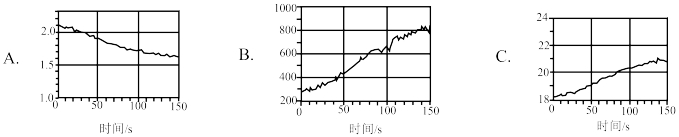
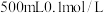 的稀盐酸,
的稀盐酸,①需要用量筒量取
 的稀盐酸
的稀盐酸 。
。②需要用到的玻璃仪器除烧杯、量筒、胶头滴管、玻璃棒外,还需要
③下列操作会使配制的溶液物质的量浓度偏低的是
A.定容时俯视容量瓶刻度线 B.容量瓶用蒸馏水洗涤后未干燥
C.未将洗涤液转移进容量瓶 D.定容时水加多了用胶头滴管吸出
E.摇匀静置,液面下降
您最近一年使用:0次
6 . 高铁酸钾(K2FeO4)是一种重要的绿色净水剂,具有净水和消毒双重功能。某学习小组设计如图所示方案制备高铁酸钾,下列说法不正确的是
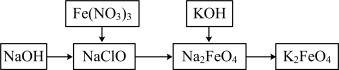
| A.高铁酸钾中铁元素的化合价为+6,具有强氧化性 |
| B.由该流程发生的反应可推测:Na2FeO4的氧化性强于NaClO |
C.由制备高铁酸钾的原理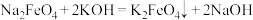 ,推测高铁酸钠的溶解度大于高铁酸钾的溶解度 ,推测高铁酸钠的溶解度大于高铁酸钾的溶解度 |
D.反应 中,生成2 mol 中,生成2 mol 时,转移6 mol电子 时,转移6 mol电子 |
您最近一年使用:0次
解题方法
7 . 下列实验操作、现象和结论都正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 石墨电极放入装有 溶液的烧杯,接通电源后观察现象 溶液的烧杯,接通电源后观察现象 | 灵敏电流计指针偏转 |  是电解质 是电解质 |
| B | 向装有铜片的试管中先加入稀硫酸,过一段时间再加入少量双氧水 | 开始时无明显现象,加入双氧水后溶液变为蓝色 | 该反应中 表现出氧化性 表现出氧化性 |
| C | 将 通入到紫色石蕊试液中 通入到紫色石蕊试液中 | 溶液先变红后褪色 |  具有漂白性 具有漂白性 |
| D | 向碳酸氢钠溶液中滴加稀盐酸 | 产生气泡 | 非金属性: |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 纳米级Fe3O4可用于以太阳能为热源分解水制H2,其过程如图所示,下列说法不正确的是
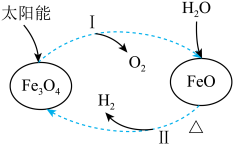
| A.过程Ⅰ中O2是氧化产物 |
B.过程Ⅱ的反应: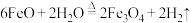 |
| C.反应Ⅱ中氧化剂与还原剂的物质的量之比为3:1 |
| D.铁氧化合物循环制H2具有节约能源、产物易分离等优点 |
您最近一年使用:0次
解题方法
9 . 以不同类别物质间的转化为线索,认识钠及其化合物,下列分析正确的是
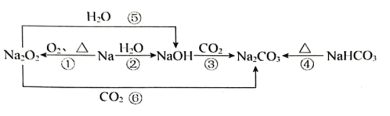
| A.NaHCO3比Na2CO3更稳定 |
| B.金属钠着火时,可以用H2O来灭火 |
| C.该转化图中涉及的氧化还原反应有3个 |
| D.向足量Na2O2固体中通入1 mol H2O和CO2混合气体充分反应,共产生16 gO2 |
您最近一年使用:0次
10 . 类比和推理是学习化学的重要思维方法,下列说法正确的是
| A.Cl-能使酸性高锰酸钾溶液褪色,则I-也能使酸性高锰钾溶液褪色 |
| B.Na在空气中燃烧生成Na2O2,则Li在空气中燃烧生成Li2O2 |
| C.Fe能从CuSO4溶液中置换Cu,则Na也能从CuSO4溶液中置换出Cu |
| D.Cl2和H2O反应生成HCl和HClO,则F2和H2O反应生成HF和HFO |
您最近一年使用:0次



