解题方法
1 . 安息香常用作医用中间体,也可以用作感光性树脂的光增感剂,其结构简式如图。下列有关安息香的说法错误的是

| A.含有两种含氧官能团 |
| B.1mol该物质最多与7mol H2加成 |
| C.能与NaOH溶液发生中和反应 |
| D.分子中所有碳原子可能共面 |
您最近一年使用:0次
解题方法
2 . 化学与生活密切相关,下列说法正确的是
| A.Fe3O4常用于制作红色油漆和涂料 |
| B.回收废旧电池的主要目的是解决资源匮乏 |
| C.氢氟酸为强酸,可以用于玻璃上雕刻花纹 |
| D.燃煤中加入CaO以减少酸雨的形成 |
您最近一年使用:0次
3 . 已知水煤气反应: ,
, 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是
 ,
, 为阿伏加德罗常数的值,下列叙述正确的是
为阿伏加德罗常数的值,下列叙述正确的是| A.所得混合气体产物的平均摩尔质量为15g |
B.若反应得到2g  ,则生成的CO体积为22.4L ,则生成的CO体积为22.4L |
C.每消耗18g  ,反应转移电子数为 ,反应转移电子数为 |
D.当断裂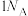 极性共价键时反应生成 极性共价键时反应生成 |
您最近一年使用:0次
2024-04-01更新
|
228次组卷
|
2卷引用:四川省乐山市2024届高三第二次调查研究考试理科综合-化学试题
名校
解题方法
4 . W、X、Y、Z为短周期主族元素,原子序数依次增大,且位于三个不同周期;W与X的最外层电子数之和与Y的最外层电子数相等,Y的L层电子数与Z的M层电子数相等,X的氧化物可导致硝酸型酸雨,下列说法正确的是
A.简单氢化物沸点: | B.对应含氧酸的酸性:X的一定强于Z的 |
| C.W、X、Y三元素只能形成共价化合物 | D.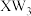 中所有原子均满足8电子结构 中所有原子均满足8电子结构 |
您最近一年使用:0次
2024-03-29更新
|
326次组卷
|
5卷引用:四川省乐山市2024届高三第二次调查研究考试理科综合-化学试题
5 . 化学为满足人民日益增长的美好生活需要做出突出贡献。下列说法不合理的是
| A.FAST用到的碳化硅是一种无机非金属材料 |
| B.硫酸铁用于净水是利用其强氧化性进行杀菌消毒 |
| C.乙烯可以用作水果的催熟剂,以使水果尽快成熟 |
| D.“深海一号”从深海中开采的石油和天然气都属于混合物 |
您最近一年使用:0次
2024-03-29更新
|
290次组卷
|
3卷引用:四川省乐山市2024届高三第二次调查研究考试理科综合-化学试题
6 . 镓(Ga)是一种重要金属,常用于制造低温合金和半导体材料等。一种从炼锌矿渣[主要含铁酸镓 和铁酸锌
和铁酸锌 ]回收镓的工艺流程如下:
]回收镓的工艺流程如下:
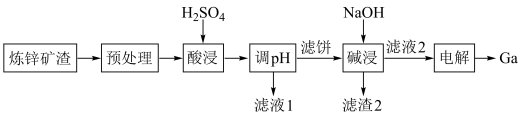
已知:①Ga与Al同主族,化学性质相似。
②铁酸镓 和铁酸锌
和铁酸锌 均为易溶于水的强电解质。
均为易溶于水的强电解质。
③常温下,工艺中相关金属离子在水溶液中沉淀的pH范围如下表所示:
回答下列问题:
(1)“预处理”时需将炼锌矿渣粉碎,其目的是___________ 。
(2)“酸浸”时 转化为
转化为 和
和 ,写出该反应的离子方程式
,写出该反应的离子方程式___________ 。
(3)“调pH”时应控制溶液的pH范围为___________ 。
(4)“碱浸”时发生反应的离子方程式为___________ 。
(5)用惰性电极电解“滤液1”,可回收金属___________ ,电解后的电解液经处理后可返回___________ 工序循环利用。
(6)用惰性电极电解“滤液2”回收镓时,镓主要附着在电解池的___________ 极。
 和铁酸锌
和铁酸锌 ]回收镓的工艺流程如下:
]回收镓的工艺流程如下:
已知:①Ga与Al同主族,化学性质相似。
②铁酸镓
 和铁酸锌
和铁酸锌 均为易溶于水的强电解质。
均为易溶于水的强电解质。③常温下,工艺中相关金属离子在水溶液中沉淀的pH范围如下表所示:
| 物质 |  |  |  |
| 开始沉淀的pH | 1.9 | 3.0 | 5.5 |
| 完全沉淀的pH | 3.2 | 4.8 | 8.0 |
(1)“预处理”时需将炼锌矿渣粉碎,其目的是
(2)“酸浸”时
 转化为
转化为 和
和 ,写出该反应的离子方程式
,写出该反应的离子方程式(3)“调pH”时应控制溶液的pH范围为
(4)“碱浸”时发生反应的离子方程式为
(5)用惰性电极电解“滤液1”,可回收金属
(6)用惰性电极电解“滤液2”回收镓时,镓主要附着在电解池的
您最近一年使用:0次
7 . 氮氧化合物的排放造成了一系列环境问题,研究氮氧化合物的治理有利于环境保护。回答下列问题:
(1)在催化剂作用下,用 还原NO能较好消除烟气中的NO,发生反应的过程如图所示。
还原NO能较好消除烟气中的NO,发生反应的过程如图所示。
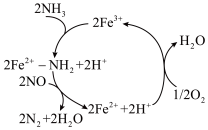
①铁元素在周期表中位于___________ 族,属于___________ 区,基态 的价电子排布式为
的价电子排布式为___________ 。
②该反应的催化剂是___________ ,用 还原NO的总反应为
还原NO的总反应为___________ 。
(2)为实现NO再利用,可以用烟气中NO制作燃料电池,其工作原理如图所示,其中电极a和电极b均为石墨电极, 在电池反应中可以循环使用。
在电池反应中可以循环使用。
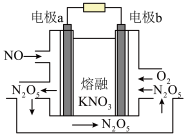
①电极b为燃料电池的_______ 极,放电时熔融 中
中 向
向________ (填“左”或“右”)移动。
②电极a上的电极反应式为___________ 。
(3)工业上还可以通过电解NO制备 ,其工作原理如图所示,其中电极均为石墨电极。
,其工作原理如图所示,其中电极均为石墨电极。
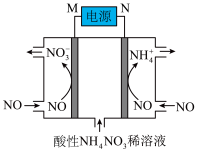
①M为电源的___________ 极,NO在M极发生___________ 反应。
②N电极上的电极反应式为___________ 。
③电解结束后,为使电解产物完全转化为 ,需补充物质
,需补充物质___________ 。
(1)在催化剂作用下,用
 还原NO能较好消除烟气中的NO,发生反应的过程如图所示。
还原NO能较好消除烟气中的NO,发生反应的过程如图所示。
①铁元素在周期表中位于
 的价电子排布式为
的价电子排布式为②该反应的催化剂是
 还原NO的总反应为
还原NO的总反应为(2)为实现NO再利用,可以用烟气中NO制作燃料电池,其工作原理如图所示,其中电极a和电极b均为石墨电极,
 在电池反应中可以循环使用。
在电池反应中可以循环使用。
①电极b为燃料电池的
 中
中 向
向②电极a上的电极反应式为
(3)工业上还可以通过电解NO制备
 ,其工作原理如图所示,其中电极均为石墨电极。
,其工作原理如图所示,其中电极均为石墨电极。
①M为电源的
②N电极上的电极反应式为
③电解结束后,为使电解产物完全转化为
 ,需补充物质
,需补充物质
您最近一年使用:0次
8 . 草酸钠( )常用作还原剂。已知常温下,草酸的电离常数
)常用作还原剂。已知常温下,草酸的电离常数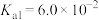 ,
,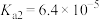 ,碳酸的电离常数
,碳酸的电离常数 ,
, 。回答下列问题:
。回答下列问题:
(1) 发生第一步水解的离子方程式为
发生第一步水解的离子方程式为___________ 。
(2)相同条件下,同浓度的① ,②
,② ,③
,③ ,④
,④ 四种溶液的pH由大到小的顺序为
四种溶液的pH由大到小的顺序为___________ (用编号表示)。
(3)将等浓度、等体积的 溶液与盐酸混合,溶液显酸性。混合后所得溶液中下列关系成立的是
溶液与盐酸混合,溶液显酸性。混合后所得溶液中下列关系成立的是___________ 。
a.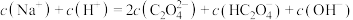
b.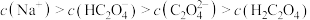
c.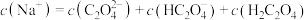
d.
(4) 溶液常用作氧化还原滴定的标准液。实验室欲配制250mL0.10mol⋅L-1的
溶液常用作氧化还原滴定的标准液。实验室欲配制250mL0.10mol⋅L-1的 溶液。
溶液。
①需称取 固体
固体___________ g。
②配制溶液时,需要的玻璃仪器除烧杯、玻璃棒、量筒外还应有___________ 。
(5)用 标准液测定某高锰酸钾样品的纯度:
标准液测定某高锰酸钾样品的纯度:
步骤I:称取2.0g高锰酸钾样品,配成100mL溶液,取20mL溶液于锥形瓶中,并加入少量硫酸酸化。
步骤Ⅱ:用(4)中配制的 标准液进行滴定,平行滴定三次,记录消耗
标准液进行滴定,平行滴定三次,记录消耗 溶液的体积如下表:
溶液的体积如下表:
①滴定终点判断的依据是___________ 。
②平均消耗 溶液的体积为
溶液的体积为_________ mL,样品中 的质量分数为
的质量分数为_________ 。
③若(4)中称取的 固体已部分吸水潮解,会使测得的样品中
固体已部分吸水潮解,会使测得的样品中 的质量分数
的质量分数_________ (填“偏高”、“偏低”或“不变”)。
 )常用作还原剂。已知常温下,草酸的电离常数
)常用作还原剂。已知常温下,草酸的电离常数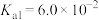 ,
,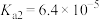 ,碳酸的电离常数
,碳酸的电离常数 ,
, 。回答下列问题:
。回答下列问题:(1)
 发生第一步水解的离子方程式为
发生第一步水解的离子方程式为(2)相同条件下,同浓度的①
 ,②
,② ,③
,③ ,④
,④ 四种溶液的pH由大到小的顺序为
四种溶液的pH由大到小的顺序为(3)将等浓度、等体积的
 溶液与盐酸混合,溶液显酸性。混合后所得溶液中下列关系成立的是
溶液与盐酸混合,溶液显酸性。混合后所得溶液中下列关系成立的是a.
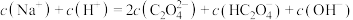
b.
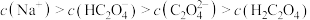
c.
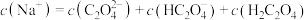
d.

(4)
 溶液常用作氧化还原滴定的标准液。实验室欲配制250mL0.10mol⋅L-1的
溶液常用作氧化还原滴定的标准液。实验室欲配制250mL0.10mol⋅L-1的 溶液。
溶液。①需称取
 固体
固体②配制溶液时,需要的玻璃仪器除烧杯、玻璃棒、量筒外还应有
(5)用
 标准液测定某高锰酸钾样品的纯度:
标准液测定某高锰酸钾样品的纯度:步骤I:称取2.0g高锰酸钾样品,配成100mL溶液,取20mL溶液于锥形瓶中,并加入少量硫酸酸化。
步骤Ⅱ:用(4)中配制的
 标准液进行滴定,平行滴定三次,记录消耗
标准液进行滴定,平行滴定三次,记录消耗 溶液的体积如下表:
溶液的体积如下表:| 第1次 | 第2次 | 第3次 | |
消耗 溶液的体积/mL 溶液的体积/mL | 49.80 | 46.75 | 50.20 |
②平均消耗
 溶液的体积为
溶液的体积为 的质量分数为
的质量分数为③若(4)中称取的
 固体已部分吸水潮解,会使测得的样品中
固体已部分吸水潮解,会使测得的样品中 的质量分数
的质量分数
您最近一年使用:0次
9 . 某种强碱性电解质的Zn-NiOOH蓄电池有很好的稳定性,其电池反应为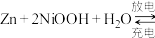
 ,下列说法错误的是
,下列说法错误的是
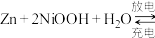
 ,下列说法错误的是
,下列说法错误的是A.放电时, 向Zn极移动 向Zn极移动 |
B.放电时,正极反应为: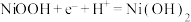 |
C.充电时, 被氧化 被氧化 |
| D.充电时,阴极附近pH增大 |
您最近一年使用:0次
解题方法
10 . 用下列装置进行实验,不能达到实验目的的是
| 选项 | A | B | C | D |
| 实验装置 | 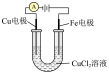 | 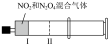 | 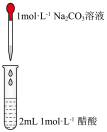 | 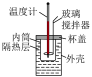 |
| 实验目的 | 铁电极上镀铜 | 探究压强对化学平衡的影响 | 比较 的 的 与 与 的 的 的大小 的大小 | 测定盐酸与NaOH反应的中和热 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



