1 .  是一种用途广泛的磁性材料,以
是一种用途广泛的磁性材料,以 为原料制备
为原料制备 并获得副产物
并获得副产物 水合物的工艺如下。
水合物的工艺如下。 时各物质溶度积见下表:
时各物质溶度积见下表:
回答下列问题:
(1) 中
中 元素的化合价是
元素的化合价是 和
和_______ 。 的核外电子排布式为
的核外电子排布式为_______ 。
(2)反应釜1中的反应需在隔绝空气条件下进行,其原因是_______ 。
(3)反应釜2中,加入 和分散剂的同时通入空气。
和分散剂的同时通入空气。
①反应的离子方程式为_______ 。
②为加快反应速率,可采取的措施有_______ 。(写出两项即可)。
(4)①反应釜3中, 时,
时, 浓度为
浓度为 ,理论上
,理论上 不超过
不超过_______ 。
②称取 水合物
水合物 ,加水溶解,加入过量
,加水溶解,加入过量 ,将所得沉淀过滤洗涤后,溶于热的稀硫酸中,用
,将所得沉淀过滤洗涤后,溶于热的稀硫酸中,用 标准溶液滴定,消耗
标准溶液滴定,消耗 。滴定达到终点的现象为
。滴定达到终点的现象为_______ ,该副产物中 的质量分数为
的质量分数为_______ 。
 是一种用途广泛的磁性材料,以
是一种用途广泛的磁性材料,以 为原料制备
为原料制备 并获得副产物
并获得副产物 水合物的工艺如下。
水合物的工艺如下。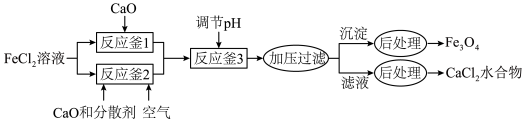
 时各物质溶度积见下表:
时各物质溶度积见下表:| 物质 |  |  |  |
溶度积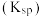 |  |  |  |
(1)
 中
中 元素的化合价是
元素的化合价是 和
和 的核外电子排布式为
的核外电子排布式为(2)反应釜1中的反应需在隔绝空气条件下进行,其原因是
(3)反应釜2中,加入
 和分散剂的同时通入空气。
和分散剂的同时通入空气。①反应的离子方程式为
②为加快反应速率,可采取的措施有
(4)①反应釜3中,
 时,
时, 浓度为
浓度为 ,理论上
,理论上 不超过
不超过②称取
 水合物
水合物 ,加水溶解,加入过量
,加水溶解,加入过量 ,将所得沉淀过滤洗涤后,溶于热的稀硫酸中,用
,将所得沉淀过滤洗涤后,溶于热的稀硫酸中,用 标准溶液滴定,消耗
标准溶液滴定,消耗 。滴定达到终点的现象为
。滴定达到终点的现象为 的质量分数为
的质量分数为
您最近一年使用:0次
2023-09-28更新
|
4717次组卷
|
5卷引用:2023年重庆市高考化学试卷
真题
2 . 固态化合物A由两种短周期元素组成,可与水放生复分解反应,甲组同学用如图装置(夹持装置略)对其进行探究实验。
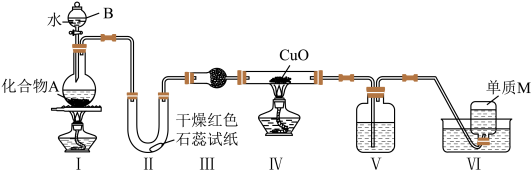
(1)仪器B的名称是____________ 。
(2)试验中,Ⅱ中的试纸变蓝,Ⅳ中黑色粉末逐渐变为红色并有M生成,则Ⅲ中的试剂为__________________ ;Ⅳ发生反应的化学方程式为____________ ;Ⅴ中的试剂为____________________ 。
(3)乙组同学进行同样实验,但装置连接顺序为Ⅰ——Ⅲ——Ⅳ——Ⅱ——Ⅴ——Ⅵ,此时Ⅱ中现象为________ ,原因是__________________ 。
(4)经上述反应,2.5 g化合物A理论上可得0.56L(标准状况)M;则A的化学式为________________ 。

(1)仪器B的名称是
(2)试验中,Ⅱ中的试纸变蓝,Ⅳ中黑色粉末逐渐变为红色并有M生成,则Ⅲ中的试剂为
(3)乙组同学进行同样实验,但装置连接顺序为Ⅰ——Ⅲ——Ⅳ——Ⅱ——Ⅴ——Ⅵ,此时Ⅱ中现象为
(4)经上述反应,2.5 g化合物A理论上可得0.56L(标准状况)M;则A的化学式为
您最近一年使用:0次
3 . 某兴趣小组设计出右图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化。

(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是____________________________ 。
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸。c中反应的化学方程式是__________________ 。再由a向c中加2 mL蒸馏水,c中的实验现象是___________________________ 。
(3)右表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是_______________ 。理由是_____________ 。
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2。操作步骤为___________ ,实验现象为____________ ;但此实验的不足之处是________________ 。

(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c。其目的是
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2 mL浓硝酸。c中反应的化学方程式是
| 方案 | 反应物 |
| 甲 | Cu、浓HNO3 |
| 乙 | Cu、稀HNO3 |
| 丙 | Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2。操作步骤为
您最近一年使用:0次
2019-01-30更新
|
1052次组卷
|
5卷引用:2007年普通高等学校招生全国统一考试(重庆卷)理综化学部分
2007年普通高等学校招生全国统一考试(重庆卷)理综化学部分(已下线)2012年苏教版高中化学必修1 4.2生产生活中的含氮化合物练习卷河南省林州市第一中学2017-2018学年高二上学期开学考试化学试题云南省腾冲市第八中学2017-2018学年高一下学期第一次月考化学试题(人教版2019)必修第二册 第八章 化学与可持续发展 第三节 环境保护与绿色化学
4 . 研究小组以无水甲苯为溶剂,PCl5(易水解)和NaN3为反应物制备纳米球状红磷。该红磷可提高钠离子电池的性能。
(1)甲苯干燥和收集的回流装置如图1所示(夹持及加热装置略)。以二苯甲酮为指示剂,无水时体系呈蓝色。_____ 中。
②冷凝水的进口是______ (填“a”或“b”)。
③用Na干燥甲苯的原理是_____ (用化学方程式表示)。
④回流过程中,除水时打开的活塞是_____ ;体系变蓝后,改变开关状态收集甲苯。
(2)纳米球状红磷的制备装置如图2所示(搅拌和加热装置略)。_____ 。用Ar气赶走空气的目的是_____ 。
②经冷却、离心分离和洗涤得到产品,洗涤时先后使用乙醇和水,依次洗去的物质是_____ 和_____ 。
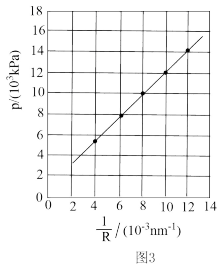
③所得纳米球状红磷的平均半径R与B装置中气体产物的压强p的关系如图3所示。欲控制合成R=125nm的红磷,气体产物的压强为_____ kPa,需NaN3的物质的量为______ mol(保留3位小数)。已知:p=a×n,其中a=2.5×105kPa•mol-1,n为气体产物的物质的量。
(1)甲苯干燥和收集的回流装置如图1所示(夹持及加热装置略)。以二苯甲酮为指示剂,无水时体系呈蓝色。

②冷凝水的进口是
③用Na干燥甲苯的原理是
④回流过程中,除水时打开的活塞是
(2)纳米球状红磷的制备装置如图2所示(搅拌和加热装置略)。
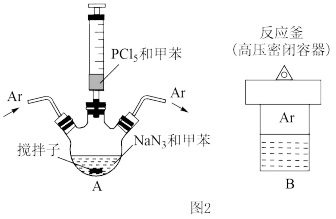
②经冷却、离心分离和洗涤得到产品,洗涤时先后使用乙醇和水,依次洗去的物质是
③所得纳米球状红磷的平均半径R与B装置中气体产物的压强p的关系如图3所示。欲控制合成R=125nm的红磷,气体产物的压强为
您最近一年使用:0次
2023-02-22更新
|
5601次组卷
|
10卷引用:2022年重庆高考真题化学试题
2022年重庆高考真题化学试题(已下线)2022年重庆高考真题化学试题变式题(实验探究题)重庆市第一中学校2023-2024学年高一下学期定时练习化学试题(已下线)专题16 化学实验综合题-2022年高考真题模拟题分项汇编(已下线)专题19 实验综合题(已下线)专题19 实验综合题(已下线)专题14 化学实验综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点48 实验方案设计与评价(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)广东省佛山市第四中学2023-2024学年上学期高二开学考试化学试题(已下线)题型四 以无机物制备为载体的综合实验-备战2024年高考化学答题技巧与模板构建
5 . 下列实验装置(夹持装置略)及操作正确的是
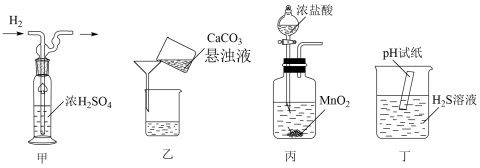

| A.装置甲气体干燥 | B.装置乙固液分离 | C.装置丙Cl2制备 | D.装置丁pH测试 |
您最近一年使用:0次
2023-02-22更新
|
7071次组卷
|
11卷引用:2022年重庆高考真题化学试题
2022年重庆高考真题化学试题(已下线)2022年重庆高考真题化学试题变式题(选择题6-10)(已下线)专题11 化学实验基础-2022年高考真题模拟题分项汇编湖南省长沙市湖南师大附中2022-2023学年高二下学期第一次月考化学试题(已下线)专题13 化学实验基础(已下线)专题13 化学实验基础(已下线)第08练 实验仪器的选用与基本操作 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)第15讲物质的检验、分离和提纯(已下线)专题05 化学实验基础-2023年高考化学真题题源解密(全国通用)吉林省长春外国语学校2023-2024学年高三上学期开学考试化学试题(已下线)考点44 化学实验基础(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
真题
解题方法
6 . 如图实验装置 (夹持装置略)或操作正确的是
A.SO2制备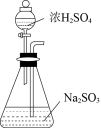 | B.液液分离 |
C.HCl吸收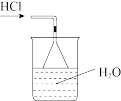 | D.酸碱滴定 |
您最近一年使用:0次
真题
解题方法
7 . 立方体形的三氧化二铟(In2O3),具有良好的气体传感性能。研究小组用水热法(密闭反应釜中以水作溶剂的高温高压条件下的化学制备方法)制备该In2O3,其主要实验过程及装置示意图如图所示。
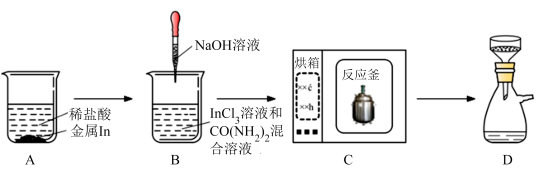
回答下列问题:
(1)前驱体的制备
①实验中使用的NaOH溶液盛装在_______ 的试剂瓶中(填“带橡皮塞”或“带玻璃塞”)。
②A装置中的反应现象是_______ ;为加快金属In的溶解,可采取的措施有_______ (写出两条即可)。
③B装置中,滴加NaOH溶液调节pH=3.02,测定pH需用的仪器名称是_______ 。
④C装置中,CO(NH2)2与水反应生成两种气体,其中酸性气体是_______ ,另一种气体与InCl3溶液反应生成前驱体的化学方程式为_______ 。
⑤D装置减压过滤时,用蒸馏水洗涤前驱体,判断前驱体洗净的实验操作和现象是_______ 。
(2)In2O3的制备
将前驱体煅烧得In2O3,反应的化学方程式为_______ 。
(3)有研究发现,其它方法制备的In(OH)3经煅烧得In2O3的过程中存在两步失重,第二步失重5.40%,推断中间产物中In的质量分数为_______ % (保留小数点后两位)。

回答下列问题:
(1)前驱体的制备
①实验中使用的NaOH溶液盛装在
②A装置中的反应现象是
③B装置中,滴加NaOH溶液调节pH=3.02,测定pH需用的仪器名称是
④C装置中,CO(NH2)2与水反应生成两种气体,其中酸性气体是
⑤D装置减压过滤时,用蒸馏水洗涤前驱体,判断前驱体洗净的实验操作和现象是
(2)In2O3的制备
将前驱体煅烧得In2O3,反应的化学方程式为
(3)有研究发现,其它方法制备的In(OH)3经煅烧得In2O3的过程中存在两步失重,第二步失重5.40%,推断中间产物中In的质量分数为
您最近一年使用:0次
8 . 某研究小组利用如图装置探究温度对CO还原Fe2O3的影响(固定装置略)
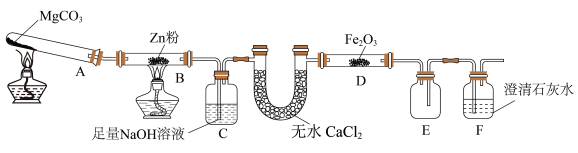
(1)MgCO3的分解产物为_______ 。
(2)装置C的作用是_______ ,处理尾气的方法为_______ 。
(3)将研究小组分为两组,按图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。(Fe2+遇K3[Fe(CN)6]溶液会生成蓝色沉淀)
①乙组得到的黑色粉末是_______ 。
②甲组步骤1中反应的离子方程式为_______ 。
③乙组步骤4中,溶液变红的原因为_______ ;溶液褪色可能的原因为_______ 。
④从实验安全考虑,题图装置还可采取的改进措施是_______ 。

(1)MgCO3的分解产物为
(2)装置C的作用是
(3)将研究小组分为两组,按图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置D加热,反应产物均为黑色粉末(纯净物),两组分别用产物进行以下实验。(Fe2+遇K3[Fe(CN)6]溶液会生成蓝色沉淀)
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加K3[Fe(CN)6]溶液 | 蓝色沉淀 | 蓝色沉淀 |
| 3 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无现象 |
| 4 | 向步骤3溶液中滴加新制氯水 | 红色褪去 | 先变红,后褪色 |
②甲组步骤1中反应的离子方程式为
③乙组步骤4中,溶液变红的原因为
④从实验安全考虑,题图装置还可采取的改进措施是
您最近一年使用:0次
2016-12-09更新
|
1224次组卷
|
5卷引用:2013年全国普通高等学校招生统一考试理科综合能力测试化学(重庆卷)
9 . ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究。
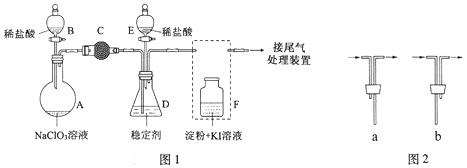
(1)仪器D的名称是____ 。安装F中导管时,应选用图2中的_____ 。
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜____ (填“快”或“慢”)。
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是_____ 。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为____ ,在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是______ 。
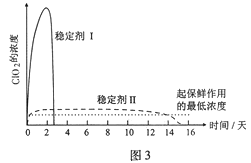
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示。若将其用于水果保鲜,你认为效果较好的稳定剂是_______ ,原因是_________ 。

(1)仪器D的名称是
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O。为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2,此时F中溶液的颜色不变,则装置C的作用是
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
(5)已吸收ClO2气体的稳定剂Ⅰ和稳定剂Ⅱ,加酸后释放ClO2的浓度随时间的变化如图3所示。若将其用于水果保鲜,你认为效果较好的稳定剂是

您最近一年使用:0次
2019-01-30更新
|
4467次组卷
|
21卷引用:2015年全国普通高等学校招生统一考试化学(重庆卷)
2015年全国普通高等学校招生统一考试化学(重庆卷)2016届浙江省舟山中学高三上学期期中考试化学试卷2016届吉林省长春十一高三下考前冲刺二理综化学试卷2016届吉林省长春十一高三下考前冲刺理综化学试卷二2016-2017学年安徽省黄山屯溪一中高二上开学测化学试卷2017届辽宁省大连市第二十中学高三上学期10月月考化学试卷河北省武邑中学2016-2017学年高一下学期期中考试化学试题2【全国百强校】河北省武邑中学2016-2017学年高一下学期期中考试化学试题福建省福州市八县(市)协作校2018届高三上学期期中联考化学试题广东省揭阳市第一中学2018届高三上学期第二次阶段考试化学试题四川省内江铁路中学2019届高三上学期入学考试化学试题【区级联考】山东省济南市莱芜区2019届高三第一学期期末质量检测化学试题安徽省合肥一六八中学2019-2020学年高一下学期入学考试化学试题(已下线)专题3.3 氯及其化合物 -巅峰冲刺山东省2020年高考化学一轮考点扫描《2020年新高考政策解读与配套资源》河北省衡水中学2020届高三下学期二月份网络教学质量监测理科综合化学试题贵州省遵义市南白中学2019-2020学年高一下学期第二次月考化学试题(已下线)期末模拟卷(二)-2020-2021学年高一化学必修第一册同步单元AB卷(新教材人教版)浙江省丽水市五校共同体2020-2021学年高二10月阶段性考试化学试题黑龙江省哈尔滨市南岗区哈尔滨师范大学附属中学2021届高三上学期期中考试化学试题河北省武邑中学2016-2017学年高一下学期期中考试化学试题1(已下线)微专题20 新型含氯化合物的制备与性质探究(ClO2、NOCl等)-备战2023年高考化学一轮复习考点微专题
真题
10 . N2O5—是一种新型硝化剂,其性质和制备受到人们的关注.
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是_______________ 。
(2)2N2O5(g)→4NO2(g)+O2(g);ΔH>0
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将___________ 填“增大”、“减小”、“不变”)。
②下表为反应在T1温度下的部分实验数据:
则500 s内N2O5的分解速率为____________ 。
③在T2温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2_________ T1。
(3)如图所示装置可用于制备N2O5,则N2O5在电解池的_________ 区生成,其电极反应式为______________________________ 。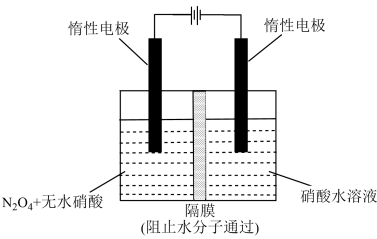
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是
(2)2N2O5(g)→4NO2(g)+O2(g);ΔH>0
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将
②下表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| e(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
则500 s内N2O5的分解速率为
③在T2温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2
(3)如图所示装置可用于制备N2O5,则N2O5在电解池的

您最近一年使用:0次



