名校
解题方法
1 . 下列变化是通过取代反应来实现的是
| A.CH3CH2OH→CH3 CHO | B.CH2=CHCH3→CH2=CHCH2Cl |
C.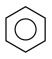 → →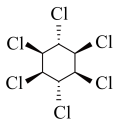 | D.CH3 CHO→CH3 CH2OH |
您最近一年使用:0次
名校
解题方法
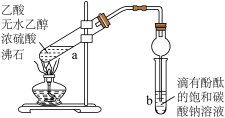
2 . 可用如图所示装置制取少量乙酸乙酯(酒精灯等在图中均已略去)。请填空:___________ 。
(2)反应的化学方程式:___________ 。
(3)球形干燥管c的作用是___________ 。
(4)饱和Na2CO3溶液,其作用是___________ ,若反应前向饱和Na2CO3溶液中加入几滴石蕊,溶液呈蓝色,反应结束后b中的现象是___________ 。
(5)浓硫酸在该反应中的作用主要有___________ 作用,该作用能使乙酸乙酯的产量增加,从反应速率和平衡的角度解释其原因是___________ 。
(6)已知:CaCl2分别与H2O、NH3、C2H5OH反应生成CaCl2·6H2O、CaCl2·8NH3、CaCl2·6C2H5OH。乙酸乙酯粗产品精制提纯的流程如下。___________ (填序号,下同),试剂X为___________ ,操作2的名称是___________ 。
A.萃取 B.分液 C.过滤 D.蒸馏 E.浓硫酸 F.饱和氯化钙溶液 G.无水硫酸镁 H.无水氯化钙
(2)反应的化学方程式:
(3)球形干燥管c的作用是
(4)饱和Na2CO3溶液,其作用是
(5)浓硫酸在该反应中的作用主要有
(6)已知:CaCl2分别与H2O、NH3、C2H5OH反应生成CaCl2·6H2O、CaCl2·8NH3、CaCl2·6C2H5OH。乙酸乙酯粗产品精制提纯的流程如下。
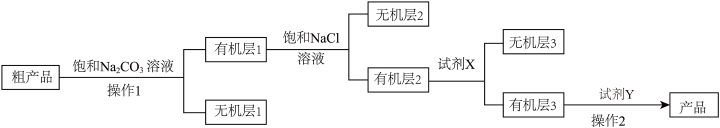
A.萃取 B.分液 C.过滤 D.蒸馏 E.浓硫酸 F.饱和氯化钙溶液 G.无水硫酸镁 H.无水氯化钙
您最近一年使用:0次
名校
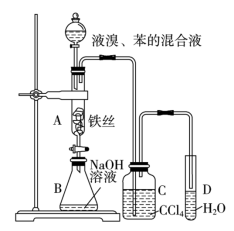
3 . 某化学课外小组用如图装置制取溴苯并探究该反应的类型。先向分液漏斗中加入苯和液溴,再将混合液滴入反应器A(A下端活塞关闭)中。___________ 。
(2)反应结束后,打开A下端的活塞,让反应液流入B中,充分振荡,目的是___________ 。
(3)C中盛放CCl4的作用是___________ 。
(4)若要证明苯和液溴发生的是取代反应,而不是加成反应,请按要求填写下表。
(2)反应结束后,打开A下端的活塞,让反应液流入B中,充分振荡,目的是
(3)C中盛放CCl4的作用是
(4)若要证明苯和液溴发生的是取代反应,而不是加成反应,请按要求填写下表。
| 向试管D中加入的试剂 | |
| 方法一 | |
| 方法二 |
您最近一年使用:0次
名校
解题方法
4 . 根据要求回答问题
(1)已知:键线式要点
a.分子中的碳氢键、碳原子及与碳原子相连的氢原子均省略
b.环形结构用相应边数的多边形来表示
c.杂原子(非碳、氢原子)不得省略,并且其上连有的氢也不省略
①一氯甲烷生成二氯甲烷___________ 。
②乙烯通入溴水中___________ 。
③苯的硝化___________ 。
④苯和氢气___________ 。
(3)已知有机物有如下转化关系,其中C的产量可用来衡量一个国家的石油化工发展水平,G的分子式为C10H14O4,试回答下列有关问题。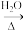 R-OH+NaX (R-表示烃基,X表示卤原子)。
R-OH+NaX (R-表示烃基,X表示卤原子)。
①A的分子式为___________ 。
②G的结构简式为___________ 。
③反应E→F的反应类型:___________ ,B+F→G的反应类型:___________ 。
④C生成D的化学方程式:___________ ;D生成E的化学方程式:___________ ;A生成B的化学方程式:___________ 。
(1)已知:键线式要点
a.分子中的碳氢键、碳原子及与碳原子相连的氢原子均省略
b.环形结构用相应边数的多边形来表示
c.杂原子(非碳、氢原子)不得省略,并且其上连有的氢也不省略
①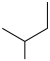 的系统命名为
的系统命名为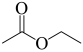 的名称为
的名称为
②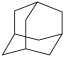 (四个等同的六元环组成)的分子式为
(四个等同的六元环组成)的分子式为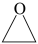 的分子式为
的分子式为
①一氯甲烷生成二氯甲烷
②乙烯通入溴水中
③苯的硝化
④苯和氢气
(3)已知有机物有如下转化关系,其中C的产量可用来衡量一个国家的石油化工发展水平,G的分子式为C10H14O4,试回答下列有关问题。
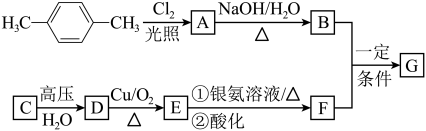
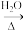 R-OH+NaX (R-表示烃基,X表示卤原子)。
R-OH+NaX (R-表示烃基,X表示卤原子)。①A的分子式为
②G的结构简式为
③反应E→F的反应类型:
④C生成D的化学方程式:
您最近一年使用:0次
名校
解题方法
5 . 某同学在用稀硫酸与锌反应制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生反应的离子方程式有___________ 。
(2)要加快上述实验中气体产生的速率,还可采取的措施有___________ (写两种)。
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间。
①请完成此实验设计,其中:V1=___________ ,V6=___________ ,V9=___________ 。
②反应一段时间后,实验A中的金属呈___________ 色,实验E中的金属呈___________ 色。
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率变化的主要原因:___________ 。
(1)上述实验中发生反应的离子方程式有
(2)要加快上述实验中气体产生的速率,还可采取的措施有
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应容器中,收集产生的气体,记录获得相同体积的气体所需的时间。
| 混合溶液 | A | B | C | D | E | F |
| 4 mol·L-1 H2SO4溶液/mL | 40 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
②反应一段时间后,实验A中的金属呈
③该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率变化的主要原因:
您最近一年使用:0次
名校
解题方法
6 . 化学电源是人类生产和生活的重要能量来源之一,回答下列问题。
(1)为了探究化学反应中的能量变化,某同学设计了如下两个实验。___________ (填序号)。
A.图1和图2的气泡均产生在锌棒表面
B.图1中温度计的示数高于图2的示数
C.图2中产生气体的速度比1快
D.图1和图2中温度计的示数相等,且均高于室温
②图②装置中,正极的电极反应方程式为___________ 。
(2)将反应2Fe3++Fe=3Fe2+设计成原电池装置,负极的电极反应方程式为___________ ,离子导体为___________ 。
(3)甲烷碱性燃料电池以KOH溶液为电解质溶液,电池反应为CH4+2O2+2OH- CO
CO +3H2O,该电池的负极电极反应方程式为
+3H2O,该电池的负极电极反应方程式为___________ ,K+向___________ 极(填正或负)移动,若电路中通过0.4mol电子,则理论上消耗甲烷的体积为(标况)___________ 。
(1)为了探究化学反应中的能量变化,某同学设计了如下两个实验。
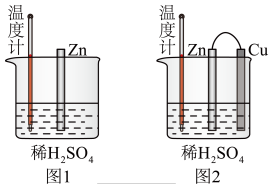
A.图1和图2的气泡均产生在锌棒表面
B.图1中温度计的示数高于图2的示数
C.图2中产生气体的速度比1快
D.图1和图2中温度计的示数相等,且均高于室温
②图②装置中,正极的电极反应方程式为
(2)将反应2Fe3++Fe=3Fe2+设计成原电池装置,负极的电极反应方程式为
(3)甲烷碱性燃料电池以KOH溶液为电解质溶液,电池反应为CH4+2O2+2OH-
 CO
CO +3H2O,该电池的负极电极反应方程式为
+3H2O,该电池的负极电极反应方程式为
您最近一年使用:0次
名校
7 . 已知X(g)和Y(g)可以相互转化:2X(g) Y(g)。现将一定量X(g)和Y(g)的混合气体通入一体积为1L的恒温密闭容器中,反应物及生成物的浓度随时间变化的关系如图所示。
Y(g)。现将一定量X(g)和Y(g)的混合气体通入一体积为1L的恒温密闭容器中,反应物及生成物的浓度随时间变化的关系如图所示。
 Y(g)。现将一定量X(g)和Y(g)的混合气体通入一体积为1L的恒温密闭容器中,反应物及生成物的浓度随时间变化的关系如图所示。
Y(g)。现将一定量X(g)和Y(g)的混合气体通入一体积为1L的恒温密闭容器中,反应物及生成物的浓度随时间变化的关系如图所示。
| A.若混合气体的总质量不变,则说明反应已达到化学平衡状态 |
| B.a、b、c、d四个点,表示化学反应处于平衡状态的只有a点 |
| C.25~30min内用X表示的平均反应速率是0.08 mol·L-1·min-1 |
| D.反应进行至25min时,曲线发生变化的原因是增大压强 |
您最近一年使用:0次
名校
解题方法
8 . 反应:2NO2(g) 2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是
2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是
 2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是
2NO(g)+O2(g),在体积固定的密闭容器中,达到平衡状态的标志是| A.单位时间内生成n mol O2的同时生成2n mol NO |
| B.用NO2、NO、O2表示的反应速率的比为2∶2∶1的状态 |
| C.混合气体的密度不再改变的状态 |
| D.混合气体的平均相对分子质量不再改变的状态 |
您最近一年使用:0次
名校
解题方法
9 . 在不同条件下,用不同物质表示反应:3A(g)+B(g)=2C(g)+2D(g)的反应速率,进行最快的是
| A.v(A)=0.6 mol·L-1·min-1 | B.v(B)=0.15 mol·L-1·min-1 |
| C.v(C)=0.015 mol·L-1·min-1 | D.v(D)=0.45 mol·L-1·min-1 |
您最近一年使用:0次
名校
解题方法
10 . 每天早上6:00起床学习会使人变得更加可爱聪明美丽帅气,而丑陋的人则会被尿憋醒,尿的主要成分是水和尿素,尿素的化学式为CO(NH2)2,陶善文博士研究出以尿素为动力的燃料电池新技术。这种电池可直接去除城市废水中的尿素,既能产、生净化的水,又能发电,电池结构如图所示,该电池描述正确的是
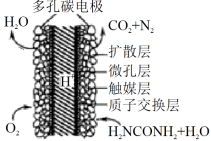
| A.电池工作时H+向右迁移 | B.该装置将电能转化成为化学能 |
| C.电池工作时负极区域酸性增强 | D.每消耗67.2LO2时,净化2mol CO(NH2)2 |
您最近一年使用:0次



