名校
1 . 碘循环工艺不仅能吸收SO2降低环境污染,同时又能制得氢气,具体流程如下:

下列说法正确的是

下列说法正确的是
| A.分离器中的物质分离操作为过滤 |
| B.膜反应器中,加入催化剂可以改变该反应的焓变 |
| C.该工艺中I2和HI的相互转化体现了“碘循环” |
D.碘循环工艺的总反应为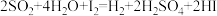 |
您最近一年使用:0次
名校
解题方法
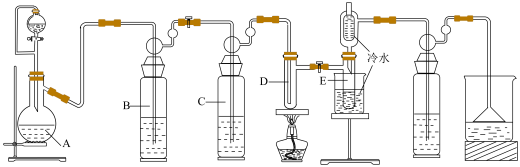
2 . 四氯化锡(SnC14)是一种重要的化工原料,主要用于有机锡化合物的制造,也可用作分析试剂、有机合成脱水剂等。已知锡单质在加热时可直接与氯气化合生成,某实验小组用如下装置对其进行合成。
【相关药品性质】
请回答下列问题:
(1)仪器A的名称是___________ 。
(2)写出SnC14水解的化学方程式___________ 。将少量SnCl4置于空气中可观察到的现象是___________ 。
(3)检验装置气密性后,向A中装入KMnO4固体,小试管D内装入Sn片,恒压滴液漏斗中加入浓盐酸,___________ (填“操作”及“现象”),点燃酒精灯开始反应;
(4)若无洗气瓶B,可能会导致的问题是___________ ;洗气瓶C中所盛放的药品是___________ 。
(5)试验结束后,小试管E内收集到的液体呈淡黄色,其原因是___________ 。

【相关药品性质】
| 药品 | 颜色、状态 | 熔点(℃) | 沸点(℃) | 其他性质 |
| Sn | 银白色固体 | 231 | 2260 | 较活泼金属能与O2、HCl等气体发生反应 |
| SnCl4 | 无色液体 | -33 | 114 | 极易水解产生SnO2∙xH2O溶胶 |
(1)仪器A的名称是
(2)写出SnC14水解的化学方程式
(3)检验装置气密性后,向A中装入KMnO4固体,小试管D内装入Sn片,恒压滴液漏斗中加入浓盐酸,
(4)若无洗气瓶B,可能会导致的问题是
(5)试验结束后,小试管E内收集到的液体呈淡黄色,其原因是
您最近一年使用:0次
名校
解题方法
3 . (I)工业合成氨的反应: 是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1mo1H-H、1mo1N-H、1mo1
是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1mo1H-H、1mo1N-H、1mo1 放出的能量分别为436kJ、391kJ、946kJ。则:
放出的能量分别为436kJ、391kJ、946kJ。则:
(1)工业上合成2mo1NH3共放出能量___________ kJ;实验室模拟工业合成氨时,在容积为2L的密闭容器内,开始投入N220mol、H230mol,反应经过10min后,生成10molNH3,则用N2表示的化学反应速率是___________ mol·L-1·min-1。
(2)如果将1mo1N2和3mo1H2混合,使之充分反应,反应放出的热量总小于上述数值,为什么?___________ 。
(II)某小组利用H2C2O4溶液和硫酸酸化的KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性KMnO4溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案,已知: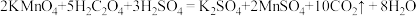
(3)表中V1=___________ mL。
ii.探究温度对化学反应速率影响的实验编号是___________ (填编号,下同),可探究反应物浓度对化学反应速率影响的实验编号是___________ 。
iii.实验①测得KMnO4溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=___________ mol·L-1·min-1。
 是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1mo1H-H、1mo1N-H、1mo1
是一个放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂。已知形成1mo1H-H、1mo1N-H、1mo1 放出的能量分别为436kJ、391kJ、946kJ。则:
放出的能量分别为436kJ、391kJ、946kJ。则:(1)工业上合成2mo1NH3共放出能量
(2)如果将1mo1N2和3mo1H2混合,使之充分反应,反应放出的热量总小于上述数值,为什么?
(II)某小组利用H2C2O4溶液和硫酸酸化的KMnO4溶液反应来探究“外界条件对化学反应速率的影响”。实验时通过测定酸性KMnO4溶液褪色所需时间来判断反应的快慢。该小组设计了如下方案,已知:
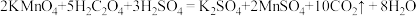
| 实验 | 0.1mol∙L-1酸性KMnO4溶液的体积/mL | 0.6mol∙L-1H2C2O4溶液的体积/mL | H2O的体积/mL | 实验温度/℃ | 溶液褪色所需时间/min |
| ① | 10 | V1 | 35 | 25 | |
| ② | 10 | 10 | 30 | 25 | |
| ③ | 10 | 10 | V2 | 50 |
ii.探究温度对化学反应速率影响的实验编号是
iii.实验①测得KMnO4溶液的褪色时间为2min,忽略混合前后溶液体积的微小变化,这段时间内平均反应速率v(H2C2O4)=
您最近一年使用:0次
名校
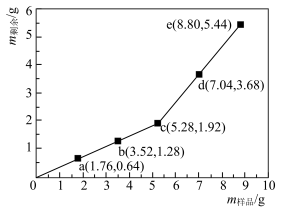
4 . 为确定Fe2O3和Cu混合物的组成(假设混合均匀),某兴趣小组称取五份不同质量的样品,分别投入30.0mL某浓度的稀硫酸中。充分反应后,每组样品剩余固体的质量与原样品质量的关系如图所示。下列说法不正确的是

A.各组样品均发生反应: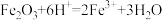 、 、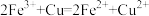 |
| B.1.76g样品充分反应后,溶液中一定存在Fe2+和Cu2+,一定不存在Fe3+ |
| C.该混合物中n(Fe2O3):n(Cu)=3:1 |
| D.稀硫酸的浓度为1.5mo1·L-1 |
您最近一年使用:0次
名校
解题方法
5 . 我国科学家在合成气直接制烯烃方面的研究获重大突破。已知:

下列说法不正确的是

下列说法不正确的是
| A.△H1-△H2<0 |
| B.反应②为吸热反应 |
C.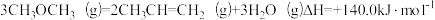 |
D.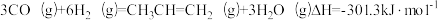 |
您最近一年使用:0次
名校
6 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.一定量的钠与8g氧气反应,若两者均无剩余,转移电子的数目为NA |
| B.等物质的量的14NO和13CO气体中所含中子数均为15NA |
| C.1mo1丙烯酸(CH2=CHCOOH)中含有双键的数目为NA |
| D.常温下,100mLpH=1的醋酸溶液中含有的氢离子数目为0.01NA |
您最近一年使用:0次
7 . 已知:A是石油裂解气的主要产物之一,其产量常用于衡量一个国家的石油化工发展水平。下列是有机物A~G之间的转化关系:
(1)A的官能团的名称是___________ ;C的结构简式是___________ ;G是一种高分子化合物,其最简式是___________ 。
(2)E是一种具有香味的液体,B+D→E的反应方程式为___________ ,该反应类型是___________ ;比赛中,当运动员肌肉挫伤或扭伤时,随队医生即对准受伤部位喷射物质F(沸点12.27℃)进行应急处理。写出由A制F的化学反应方程式___________ ;E的同分异构体能与NaHCO3溶液反应,写出该同分异构体的结构简式___________ (一种即可)。

(1)A的官能团的名称是
(2)E是一种具有香味的液体,B+D→E的反应方程式为
您最近一年使用:0次
名校
8 . 氧化铈(CeO2)是一种应用非常广泛的稀土氧化物。现以氟碳铈矿(含CeFCO3、BaO、SiO2等)为原料制备氧化铈,其工艺流程如图所示:

已知:①稀土离子易与 形成复盐沉淀,Ce3+和
形成复盐沉淀,Ce3+和 发生反应:
发生反应: ;
;
②硫脲: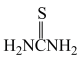 具有还原性,酸性条件下易被氧化为(SCN2H3)2;
具有还原性,酸性条件下易被氧化为(SCN2H3)2;
③Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀;
④Ce2(CO3)3为白色粉末,难溶于水。
回答下列问题:
(1)滤渣A的主要成分是___________ (填写化学式)。
(2)在另一种生产工艺中,在氟碳铈矿矿石粉中加入碳酸氢钠同时通入氧气焙烧,焙烧得到NaF和CeO2两种固体以及两种高温下的气态物质,请写出焙烧过程中相应的化学方程式___________ 。
(3)焙烧后加入稀硫酸浸出,为提高Ce的浸出率,需控制硫酸浓度不能太大的原因是______ 。
(4)加入硫脲的目的是将CeF22+还原为Ce3+,反应的离子方程式为___________ 。
(5)步骤③加入盐酸后,通常还需加入另一种化学试剂X,根据题中信息推测,加入X的作用为___________ 。
(6)下列关于步骤④的说法正确的是___________(填字母)。
(7)取所得产品7.00gCeO2溶解后配成250mL溶液。取25.00mL该溶液用0.20mol。L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定,滴定时发生反应 ,达到滴定终点时消耗硫酸亚铁铵溶液18.50mL,则该产品的纯度为
,达到滴定终点时消耗硫酸亚铁铵溶液18.50mL,则该产品的纯度为___________ 。(保留三位有效数字)。

已知:①稀土离子易与
 形成复盐沉淀,Ce3+和
形成复盐沉淀,Ce3+和 发生反应:
发生反应: ;
;②硫脲:
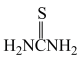 具有还原性,酸性条件下易被氧化为(SCN2H3)2;
具有还原性,酸性条件下易被氧化为(SCN2H3)2;③Ce3+在空气中易被氧化为Ce4+,两者均能形成氢氧化物沉淀;
④Ce2(CO3)3为白色粉末,难溶于水。
回答下列问题:
(1)滤渣A的主要成分是
(2)在另一种生产工艺中,在氟碳铈矿矿石粉中加入碳酸氢钠同时通入氧气焙烧,焙烧得到NaF和CeO2两种固体以及两种高温下的气态物质,请写出焙烧过程中相应的化学方程式
(3)焙烧后加入稀硫酸浸出,为提高Ce的浸出率,需控制硫酸浓度不能太大的原因是
(4)加入硫脲的目的是将CeF22+还原为Ce3+,反应的离子方程式为
(5)步骤③加入盐酸后,通常还需加入另一种化学试剂X,根据题中信息推测,加入X的作用为
(6)下列关于步骤④的说法正确的是___________(填字母)。
A.该步骤发生的反应是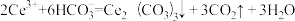 |
| B.可以用Na2CO3溶液代替NH4HCO3溶液,不影响产品纯度 |
| C.过滤时选择减压过滤能够大大提高过滤效率 |
| D.过滤后的滤液中仍含有较多Ce3+,需要将滤液循环以提高产率 |
(7)取所得产品7.00gCeO2溶解后配成250mL溶液。取25.00mL该溶液用0.20mol。L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定,滴定时发生反应
 ,达到滴定终点时消耗硫酸亚铁铵溶液18.50mL,则该产品的纯度为
,达到滴定终点时消耗硫酸亚铁铵溶液18.50mL,则该产品的纯度为
您最近一年使用:0次
名校
9 . 已知拆开1molH-H键,1molN N键分别需要吸收的能量为436kJ、946kJ;形成1molN-H键,会放出能量391kJ,在反应
N键分别需要吸收的能量为436kJ、946kJ;形成1molN-H键,会放出能量391kJ,在反应 中,每生成3mo1N-H键
中,每生成3mo1N-H键
 N键分别需要吸收的能量为436kJ、946kJ;形成1molN-H键,会放出能量391kJ,在反应
N键分别需要吸收的能量为436kJ、946kJ;形成1molN-H键,会放出能量391kJ,在反应 中,每生成3mo1N-H键
中,每生成3mo1N-H键| A.吸收92kJ热量 | B.放出46kJ热量 |
| C.放出209kJ热量 | D.吸收209kJ热量 |
您最近一年使用:0次
名校
10 . 通过实验、观察、类比、推理等方法得出正确的结论是化学学习的方法之一,下列实验操作、现象和解释或者结论正确的有几项
| 选项 | 实验操作 | 实验现象 | 实验结论 |
| ① | 将金属钠在燃烧匙中点燃,迅速伸入集满 气体的集气瓶 气体的集气瓶 | 瓶中产生大量白烟和黑色颗粒 |  具有氧化性 具有氧化性 |
| ② | 向黄色的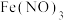 溶液中滴加氢碘酸 溶液中滴加氢碘酸 | 溶液颜色加深 | 氧化性: |
| ③ | 向某钾盐中滴加浓盐酸,产生的气体再通入品红溶液 | 品红溶液褪色 | 该钾盐为 、 、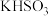 与 与 至少有一种 至少有一种 |
| ④ | 工业上用 与焦炭在高温条件下制备粗硅 与焦炭在高温条件下制备粗硅 | 生成可燃性气体,得到黑色固体粗硅 | 非金属性:C>Si |
| ⑤ | 用pH试纸测量饱和新制氯水的酸碱性 | pH试纸先变红色后褪色 | 饱和新制氯水呈酸性且具有漂白性 |
| A.2 | B.3 | C.4 | D.5 |
您最近一年使用:0次



