解题方法
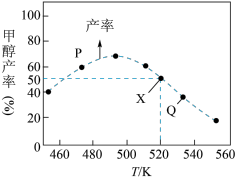
1 . 在体积为1L的恒容容器中,用CO2和H2合成甲醇CO2(g)+3H2(g) CH3OH(g)+H2O(g)。相同时间内不同的温度下,将1mol CO2和3mol H2在反应器中反应,测定CH3OH的产率与温度的关系如图所示。下列说法正确的是
CH3OH(g)+H2O(g)。相同时间内不同的温度下,将1mol CO2和3mol H2在反应器中反应,测定CH3OH的产率与温度的关系如图所示。下列说法正确的是
 CH3OH(g)+H2O(g)。相同时间内不同的温度下,将1mol CO2和3mol H2在反应器中反应,测定CH3OH的产率与温度的关系如图所示。下列说法正确的是
CH3OH(g)+H2O(g)。相同时间内不同的温度下,将1mol CO2和3mol H2在反应器中反应,测定CH3OH的产率与温度的关系如图所示。下列说法正确的是
| A.图中X点v(正)=v(逆) |
| B.该反应是吸热反应 |
| C.图中P点所示条件下,延长反应时间不能提高CH3OH的产率 |
| D.520K下,X点所对应甲醇的产率50%,则平衡常数K=1/3 |
您最近一年使用:0次
2 . 请回答下列问题:
(1)某浓度的氨水中存在平衡:NH3·H2O NH
NH +OH-。若增大NH
+OH-。若增大NH 的浓度而不增大OH-的浓度,应采取的措施是
的浓度而不增大OH-的浓度,应采取的措施是___________ (填字母)。
a.加入NH4Cl固体 b.适当升高温度 c.通入NH3 d.加入少量浓盐酸
(2)常温下,c(H+)相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
①加适量醋酸钠晶体后,醋酸溶液中c(H+)___________ (填“增大”、“减小”或“不变”,下同),盐酸中c(H+)___________ 。
②加水稀释10倍后,醋酸溶液中的c(H+)___________ (填“>”、“=”或“<”)盐酸中的c(H+)。
③加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积:醋酸___________ (填“>”“=”或“<”)盐酸。
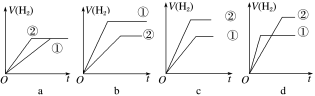
④分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是___________ (填字母)。(①表示盐酸,②表示醋酸)
(3)将0.1mol·L-1的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是___________ (填字母)。
a.电离程度增大 b.溶液中离子浓度都增大 c.Ka(乙酸)不变 d.溶液中醋酸分子减少
(1)某浓度的氨水中存在平衡:NH3·H2O
 NH
NH +OH-。若增大NH
+OH-。若增大NH 的浓度而不增大OH-的浓度,应采取的措施是
的浓度而不增大OH-的浓度,应采取的措施是a.加入NH4Cl固体 b.适当升高温度 c.通入NH3 d.加入少量浓盐酸
(2)常温下,c(H+)相同、体积相同的醋酸和盐酸两种溶液,采取以下措施:
①加适量醋酸钠晶体后,醋酸溶液中c(H+)
②加水稀释10倍后,醋酸溶液中的c(H+)
③加等浓度的NaOH溶液至恰好中和,所需NaOH溶液的体积:醋酸
④分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是

(3)将0.1mol·L-1的CH3COOH加水稀释,有关稀释后醋酸溶液的说法中,正确的是
a.电离程度增大 b.溶液中离子浓度都增大 c.Ka(乙酸)不变 d.溶液中醋酸分子减少
您最近一年使用:0次
3 . 下列各组物质中都是强电解质的是
| A.H3BO3、HCl、AgNO3 | B.NH4F、CH3COONa、BaSO4 |
| C.CO2、Ba(OH)2、CH3OH | D.NH3·H2O、NaF、KOH |
您最近一年使用:0次
解题方法
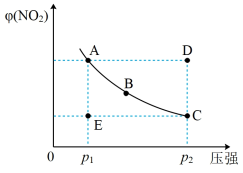
4 . 对于反应N2O4(g) 2NO2(g),在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示(实线上的每个点为对应压强下的平衡点),下列说法正确的是
2NO2(g),在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示(实线上的每个点为对应压强下的平衡点),下列说法正确的是
 2NO2(g),在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示(实线上的每个点为对应压强下的平衡点),下列说法正确的是
2NO2(g),在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示(实线上的每个点为对应压强下的平衡点),下列说法正确的是
| A.A、C两点的正反应速率的关系为A>C |
| B.A、B、C、D、E各状态中,v(正)<v(逆)的是状态E |
| C.维持p1不变,E→A所需时间为x;维持p2不变,D→C所需时间为y,则x>y |
| D.使E状态从水平方向到达C状态,再沿平衡曲线到达A状态,从理论上来讲可选用的条件是从p1缓慢加压至p2,再由p2无限突然降压至p1 |
您最近一年使用:0次
解题方法
5 . Burns和Dainton研究了反应Cl2(g)+CO(g) COCl2(g)的动力学,获得其速率方程v=k[c(Cl2)]3/2[c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。该反应可认为经过以下反应历程:下列表述错误的是
COCl2(g)的动力学,获得其速率方程v=k[c(Cl2)]3/2[c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。该反应可认为经过以下反应历程:下列表述错误的是
第一步:Cl2 2Cl 快速平衡
2Cl 快速平衡
第二步:Cl+CO COCl 快速平衡
COCl 快速平衡
第三步:COCl+Cl2→COCl2+Cl 慢反应
 COCl2(g)的动力学,获得其速率方程v=k[c(Cl2)]3/2[c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。该反应可认为经过以下反应历程:下列表述错误的是
COCl2(g)的动力学,获得其速率方程v=k[c(Cl2)]3/2[c(CO)]m,k为速率常数(只受温度影响),m为CO的反应级数。该反应可认为经过以下反应历程:下列表述错误的是第一步:Cl2
 2Cl 快速平衡
2Cl 快速平衡第二步:Cl+CO
 COCl 快速平衡
COCl 快速平衡第三步:COCl+Cl2→COCl2+Cl 慢反应
| A.COCl属于反应的中间产物 | B.第一步和第二步的活化能较低 |
| C.决定总反应快慢的是第三步 | D.第三步的有效碰撞频率较大 |
您最近一年使用:0次
6 . SO2(g)+O2(g)→SO3(g)反应过程中的能量变化如图所示(图中E1表示无催化剂时正反应的活化能,E2表示无催化剂时逆反应的活化能)。下列有关叙述正确的是


| A.该反应的逆反应为吸热反应,SO2的能量一定高于SO3的能量 |
| B.该反应中,反应物的总键能小于生成物的总键能 |
| C.ΔH=E2-E1,使用催化剂改变活化能,但不改变反应热 |
D.500℃、101kPa下,将1mol SO2(g)和0.5mol O2(g)置于密闭容器中充分反应生成SO3(g)放热akJ,其热化学方程式为2SO2(g)+O2(g) 2SO3(g) ΔH=-2akJ·mol-1 2SO3(g) ΔH=-2akJ·mol-1 |
您最近一年使用:0次
解题方法
7 . 多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时(各物质均为气态),甲醇与水在铜基催化剂上的反应机理和能量图如下图,下列说法正确的是
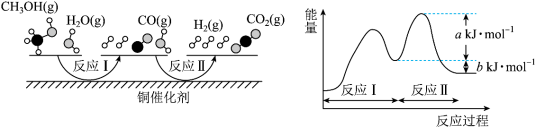

| A.反应Ⅱ的热化学方程式为:CO(g)+H2O(g)=H2(g)+CO2(g) ΔH=+bkJ/mol |
| B.在相同条件下反应Ⅰ的反应速率大于反应Ⅱ的反应速率 |
| C.选择优良的催化剂可以降低反应Ⅰ和Ⅱ的活化能,减少反应过程中的能耗和反应的焓变 |
| D.1mol CH3OH(g)和1mol H2O(g)的总能量小于1mol CO2(g)和3mol H2(g)的总能量 |
您最近一年使用:0次
8 . CO2转化为燃料甲醇是实现碳中和的途径之一,在恒温恒容密闭容器中进行反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0,下列有关说法正确的是
CH3OH(g)+H2O(g) ΔH<0,下列有关说法正确的是
 CH3OH(g)+H2O(g) ΔH<0,下列有关说法正确的是
CH3OH(g)+H2O(g) ΔH<0,下列有关说法正确的是| A.该反应的正反应为熵增过程,ΔS>0 |
| B.该反应在高温下可自发进行 |
| C.CH3OH分子中每个原子均满足8电子稳定结构 |
| D.降低温度有利于提高甲醇的产率 |
您最近一年使用:0次
解题方法
9 . 学习“化学反应的速率和化学平衡”内容后,联系工业生产实际所发表的观点,你认为正确的是
| A.化学反应速率理论可指导怎样提高原料的平衡转化率 |
| B.化学平衡理论可指导怎样使用有限原料多出产品 |
| C.温度升高,分子动能增加,反应所需活化能减少,反应速率增大 |
| D.增大压强能提高活化分子的百分率,提高单位时间内分子有效碰撞次数 |
您最近一年使用:0次
解题方法
10 . “北溪”天然气管道是俄罗斯向欧洲输气的主要管道。2022年9月26日,“北溪”天然气管道被发现有两个滑漏点,分别位于丹麦和瑞典附近水域。下列有关说法错误的是
| A.天然气的主要成分是CH4 | B.天然气是不可再生能源 |
| C.甲烷的燃烧热数值与参加反应甲烷的量有关 | D.CH4是非电解质 |
您最近一年使用:0次



