名校
解题方法
1 . 钪(Sc)是一种稀土金属元素,在国防、航天,核能等领域具有重要应用。氯化钪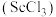 是一种可溶于水的灰白色固体,是制备钪的重要原料。从某工业废料“赤泥”(含有
是一种可溶于水的灰白色固体,是制备钪的重要原料。从某工业废料“赤泥”(含有 、
、 、
、 、
、 、
、 等)中回收
等)中回收 的工艺流程如下:
的工艺流程如下: 难溶于盐酸。
难溶于盐酸。
②常温下,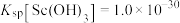 ,
, 。
。
回答下列问题:
(1)某次实验中需要使用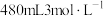 的盐酸,用浓盐酸(密度为
的盐酸,用浓盐酸(密度为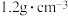 ,质量分数为
,质量分数为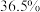 )配制实验所需要的盐酸,则需要量取浓盐酸的体积为
)配制实验所需要的盐酸,则需要量取浓盐酸的体积为___________  。
。
(2)滤渣1的主要成分是___________ (填化学式)。“酸浸”时温度过高,酸浸速率反而减慢,其原因是___________ 。
(3)常温下,“调 ”时,溶液中
”时,溶液中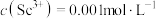 ,为除去杂质离子,应控制的
,为除去杂质离子,应控制的 范围是
范围是___________ (当溶液中某离子浓度c≤1.0×10-5mol/L时,可认为该离子沉淀完全)。
(4)“氧化”时反应的离子方程式为___________ 。
(5)实验室模拟流程中“灼烧”得到 ,用来盛放被灼烧物的仪器为
,用来盛放被灼烧物的仪器为___________ ,“加热氯化”步骤中所加入焦炭过量,写出由 制备三氯化钪反应的化学方程式:
制备三氯化钪反应的化学方程式:___________ 。
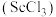 是一种可溶于水的灰白色固体,是制备钪的重要原料。从某工业废料“赤泥”(含有
是一种可溶于水的灰白色固体,是制备钪的重要原料。从某工业废料“赤泥”(含有 、
、 、
、 、
、 、
、 等)中回收
等)中回收 的工艺流程如下:
的工艺流程如下:
 难溶于盐酸。
难溶于盐酸。②常温下,
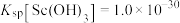 ,
, 。
。回答下列问题:
(1)某次实验中需要使用
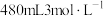 的盐酸,用浓盐酸(密度为
的盐酸,用浓盐酸(密度为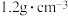 ,质量分数为
,质量分数为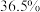 )配制实验所需要的盐酸,则需要量取浓盐酸的体积为
)配制实验所需要的盐酸,则需要量取浓盐酸的体积为 。
。(2)滤渣1的主要成分是
(3)常温下,“调
 ”时,溶液中
”时,溶液中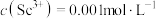 ,为除去杂质离子,应控制的
,为除去杂质离子,应控制的 范围是
范围是(4)“氧化”时反应的离子方程式为
(5)实验室模拟流程中“灼烧”得到
 ,用来盛放被灼烧物的仪器为
,用来盛放被灼烧物的仪器为 制备三氯化钪反应的化学方程式:
制备三氯化钪反应的化学方程式:
您最近一年使用:0次
名校
2 . 治理氮氧化物 的污染是化学研究的重要课题之一。
的污染是化学研究的重要课题之一。
Ⅰ. 能被灼热的铁粉还原为
能被灼热的铁粉还原为 ,同时生成
,同时生成 ,利用下列装置模拟该反应。
,利用下列装置模拟该反应。 氧化为
氧化为 ;
;
②NaOH溶液能与 反应,不与
反应,不与 反应。
反应。
(1)打开装置A分液漏斗活塞,烧瓶中观察到的实验现象:铜片表面出现无色气泡,铜片逐渐变小,___________ ,烧瓶中溶液由无色变为蓝色。
(2)上述装置接口的连接顺序:________ (按气流方向,用小写字母表示)。
a→___________→___________→___________→___________→g→h→b→c→d。
(3)装置B的作用是___________ 。
(4)装置E中反应的化学方程式为___________ 。
Ⅱ.已知: 能与
能与 反应;
反应; 和
和 都有较强氧化性。为探究
都有较强氧化性。为探究 与
与 反应的产物,提出如下假设:假设①
反应的产物,提出如下假设:假设① 氧化
氧化 ;假设②
;假设② 氧化
氧化 。
。
甲同学设计如图所示实验装置:
(5)甲、乙两同学对假设分别进行了验证:
请做出正确判断,写出 和
和 反应的化学方程式:
反应的化学方程式:___________ 。
(6)图中单向阀在实现气体单向流通的同时,还有一个作用是___________ 。
 的污染是化学研究的重要课题之一。
的污染是化学研究的重要课题之一。Ⅰ.
 能被灼热的铁粉还原为
能被灼热的铁粉还原为 ,同时生成
,同时生成 ,利用下列装置模拟该反应。
,利用下列装置模拟该反应。
 氧化为
氧化为 ;
;②NaOH溶液能与
 反应,不与
反应,不与 反应。
反应。(1)打开装置A分液漏斗活塞,烧瓶中观察到的实验现象:铜片表面出现无色气泡,铜片逐渐变小,
(2)上述装置接口的连接顺序:
a→___________→___________→___________→___________→g→h→b→c→d。
(3)装置B的作用是
(4)装置E中反应的化学方程式为
Ⅱ.已知:
 能与
能与 反应;
反应; 和
和 都有较强氧化性。为探究
都有较强氧化性。为探究 与
与 反应的产物,提出如下假设:假设①
反应的产物,提出如下假设:假设① 氧化
氧化 ;假设②
;假设② 氧化
氧化 。
。甲同学设计如图所示实验装置:
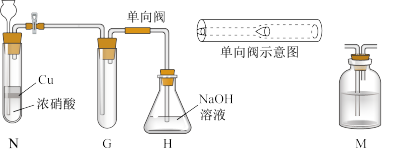
(5)甲、乙两同学对假设分别进行了验证:
| 实验操作 | 现象 | 结论 | |
| 甲同学 | 待试管G中收集满气体,向其中加入适量 粉末,塞紧塞子,轻轻振荡试管,观察现象;并将带火星的木条迅速伸进试管,观察 粉末,塞紧塞子,轻轻振荡试管,观察现象;并将带火星的木条迅速伸进试管,观察 | 红棕色气体迅速消失;木条复燃 | 假设①正确 |
| 乙同学 | 在N、G之间增加一个M洗气瓶,目的是干燥 ,重复甲同学的实验操作 ,重复甲同学的实验操作 | 红棕色气体迅速消失,带火星的木条未复燃 | 假设②正确 |
 和
和 反应的化学方程式:
反应的化学方程式:(6)图中单向阀在实现气体单向流通的同时,还有一个作用是
您最近一年使用:0次
名校
解题方法
3 . 下列根据实验方案设计及现象得出结论错误的是
| 选项 | 实验设计及现象 | 结论 |
| A | 向碘的 溶液中加入等体积浓 溶液中加入等体积浓 溶液,振荡。溶液分层,下层紫红色变浅粉红色,上层呈棕黄色 溶液,振荡。溶液分层,下层紫红色变浅粉红色,上层呈棕黄色 | 碘在浓 溶液中溶解能力大于在 溶液中溶解能力大于在 中溶解能力 中溶解能力 |
| B | 有机物A加入 乙醇溶液中,充分加热;冷却后,取混合液加足量硝酸酸化,滴加硝酸银溶液,产生白色沉淀 乙醇溶液中,充分加热;冷却后,取混合液加足量硝酸酸化,滴加硝酸银溶液,产生白色沉淀 | 有机物 可能是氯代烃 可能是氯代烃 |
| C | 向 溶液中,先加 溶液中,先加 溶液调节 溶液调节 ,有红褐色沉淀生成,再加入足量的KSCN溶液,沉淀不溶解 ,有红褐色沉淀生成,再加入足量的KSCN溶液,沉淀不溶解 | 该实验条件下, 结合 结合 的能力比 的能力比 强 强 |
| D | 常温下,用 计分别测定浓度均为 计分别测定浓度均为 的 的 溶液和 溶液和 溶液的 溶液的 ,测得 ,测得 均为7.0 均为7.0 | 两溶液中水的电离程度相同 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 下列关于物质的工业制备涉及的相关反应中错误的是
A.冶炼铝: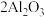 (熔融) (熔融)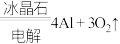 |
B.工业制硝酸: |
C.侯式制碱法: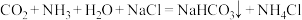 |
D.用 制备 制备 : :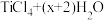 (过量) (过量)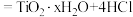 |
您最近一年使用:0次
名校
解题方法
5 . 有机化合物Ⅰ为一种杀菌抗炎药的主要成分,其中一种合成路线如图所示:
(1)D的分子式为_______ ;E的化学名称为_______ 。
(2)设计A→B、B→C的目的分别是_______ 、_______ 。
(3)写出F→G反应的化学方程式:_______ ;H→I的反应类型为_______ 。
(4)H的结构简式为_______ ;符合下列条件H的同分异构体有_______ 种。 的合成路线
的合成路线_______ (无机试剂任选)。

Ⅰ. +RCl
+RCl
 +HCl;
+HCl;
定位取代基 | 烷基 | 溴原子 | 羟基 | 烷氧基 | 氨基 | 硝基 | 磺酸基 | 羧基 |
定位效应 | 邻位、对位 | 间位 | ||||||
Ⅲ.
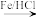
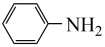 。
。
(1)D的分子式为
(2)设计A→B、B→C的目的分别是
(3)写出F→G反应的化学方程式:
(4)H的结构简式为
①分子中存在 ;②
;②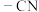 直接连在苯环上;③在核磁共振氢谱中有4组峰,面积比为3∶2∶2∶2。
直接连在苯环上;③在核磁共振氢谱中有4组峰,面积比为3∶2∶2∶2。
 的合成路线
的合成路线
您最近一年使用:0次
2024-06-07更新
|
91次组卷
|
3卷引用:黑龙江省大庆市让胡路区大庆中学2024届高三下学期5月期中化学试题
6 . 柴油汽车常用尿素(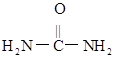 )溶液处理尾气,发生反应:
)溶液处理尾气,发生反应: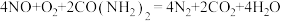 。设
。设 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
| A.上述反应涉及的元素中,基态原子第一电离能最大的为O |
B.常温下,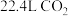 含有共用电子对数目为 含有共用电子对数目为 |
C.反应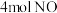 时转移的电子数目为 时转移的电子数目为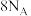 |
D.1个尿素分子中含有7个 键 键 |
您最近一年使用:0次
2024-06-04更新
|
179次组卷
|
2卷引用:黑龙江省大庆市让胡路区大庆中学2024届高三下学期5月期中化学试题
2024·辽宁沈阳·一模
名校
解题方法
7 . 以辉铜矿(主要成分为Cu2S,含Fe3O4,SiO2等杂质)为原料,合成 的流程如下。下列说法错误的是
的流程如下。下列说法错误的是
 的流程如下。下列说法错误的是
的流程如下。下列说法错误的是
| A.步骤I在足量O2中煅烧,产生气体的主要成分为SO3 |
| B.步骤Ⅱ所得溶液的溶质主要为CuSO4、Fe2(SO4)3 |
| C.步骤Ⅲ先形成难溶物,最后得到深蓝色溶液D |
| D.步骤Ⅳ的操作依次为加入乙醇、过滤、洗涤、干燥 |
您最近一年使用:0次
2024-04-13更新
|
248次组卷
|
3卷引用:黑龙江省大庆市让胡路区大庆中学2024届高三下学期5月期中化学试题
名校
解题方法
8 . 控制、治理氮氧化物对大气的污染是改善大气质量的证要方面。
(1)火力发电厂的燃煤排烟中含大量的氮氧化物( ),可利用甲烷和
),可利用甲烷和 在一条件下反应消除其污染,那么
在一条件下反应消除其污染,那么 与
与 反应的化学方程式为
反应的化学方程式为___________ 。
(2)在一密闭容器中发生反应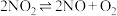 ,反应过程中
,反应过程中 的浓度随时间变化的情况如以下图所示。请回答:
的浓度随时间变化的情况如以下图所示。请回答:
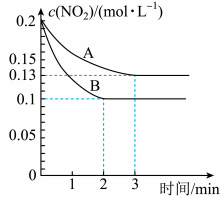
①依曲线A,反应在前3min内氧气的平均反应速率为___________ 。(保留三位有效数字)
②假设曲线A、B分别表示的是该反应在某不同条件下的反应情况,那么此条件是___________ 。(填“浓度”、“压强”、“温度”或“催化剂”)
③曲线A、B分别对应的反应平衡常数的大小关系是
___________  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
(3)一定温度下,密闭容器中 可发生以下反应:
可发生以下反应:
 I
I
 Ⅱ
Ⅱ
那么反应I的平衡常数表达式为___________ 。假设达平衡时, ,
,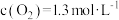 ,那么反应Ⅱ中
,那么反应Ⅱ中 的转化率为
的转化率为___________ , (g)的起始浓度不低于
(g)的起始浓度不低于___________  。
。
(1)火力发电厂的燃煤排烟中含大量的氮氧化物(
 ),可利用甲烷和
),可利用甲烷和 在一条件下反应消除其污染,那么
在一条件下反应消除其污染,那么 与
与 反应的化学方程式为
反应的化学方程式为(2)在一密闭容器中发生反应
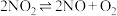 ,反应过程中
,反应过程中 的浓度随时间变化的情况如以下图所示。请回答:
的浓度随时间变化的情况如以下图所示。请回答:
①依曲线A,反应在前3min内氧气的平均反应速率为
②假设曲线A、B分别表示的是该反应在某不同条件下的反应情况,那么此条件是
③曲线A、B分别对应的反应平衡常数的大小关系是

 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)(3)一定温度下,密闭容器中
 可发生以下反应:
可发生以下反应: I
I Ⅱ
Ⅱ那么反应I的平衡常数表达式为
 ,
,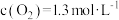 ,那么反应Ⅱ中
,那么反应Ⅱ中 的转化率为
的转化率为 (g)的起始浓度不低于
(g)的起始浓度不低于 。
。
您最近一年使用:0次
2024-04-05更新
|
69次组卷
|
2卷引用:黑龙江省鸡西市新兴实验学校2023-2024学年高三上学期11月期中考试化学试题
9 . 有机物F为某药物合成的重要中间体,F的一种合成路线如下:
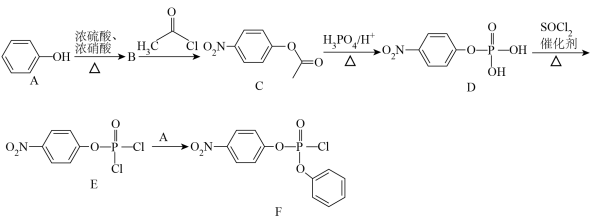
回答下列问题:
(1)B的结构简式为___________ ,其化学名称为___________ 。
(2)C中含氧官能团的名称为______________________ 。
(3)B→C的反应类型为___________ 。
(4)E→F反应的化学方程式为______________________ 。
(5)满足下列条件的C的同分异构体有___________ 种(不包括立体异构),其中核磁共振氢谱有4组峰且峰面积之比为 的结构简式为
的结构简式为______________________ 。
①硝基与苯环直接相连 ②能发生水解反应和银镜反应

回答下列问题:
(1)B的结构简式为
(2)C中含氧官能团的名称为
(3)B→C的反应类型为
(4)E→F反应的化学方程式为
(5)满足下列条件的C的同分异构体有
 的结构简式为
的结构简式为①硝基与苯环直接相连 ②能发生水解反应和银镜反应
您最近一年使用:0次
名校
10 . 常温下,0.10mol/L HCOONH4溶液中,c(HCOO-)、c(HCOOH)、 、c(NH3•H2O)四种微粒的pX[
、c(NH3•H2O)四种微粒的pX[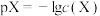 ]随pOH的变化关系如图,已知
]随pOH的变化关系如图,已知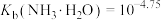 。下列说法错误的是
。下列说法错误的是
 、c(NH3•H2O)四种微粒的pX[
、c(NH3•H2O)四种微粒的pX[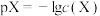 ]随pOH的变化关系如图,已知
]随pOH的变化关系如图,已知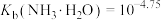 。下列说法错误的是
。下列说法错误的是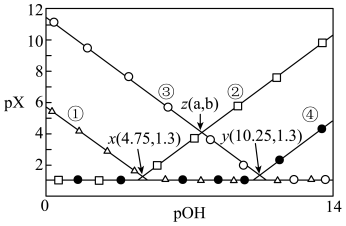
A.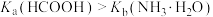 |
B.曲线③表示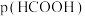 随pOH的变化关系 随pOH的变化关系 |
C.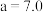 |
D.等浓度的HCOOH和HCOONH4混合液中: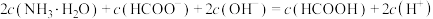 |
您最近一年使用:0次
2024-04-02更新
|
525次组卷
|
6卷引用:黑龙江省大庆市让胡路区大庆中学2024届高三下学期5月期中化学试题



