名校
解题方法
1 . X、Y、Z、W均为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子数是内层电子数的3倍,下列说法错误的是
| X | Y | |
| Z | W |
| A.四种元素的单质中,Z的单质熔点、沸点最高 |
B. 和 和 均具有漂白性,漂白原理不同 均具有漂白性,漂白原理不同 |
C.氧化物对应水化物的酸性: |
| D.X、Z的简单氢化物均能与各自某种氧化物对应的水化物发生反应 |
您最近一年使用:0次
2024-03-01更新
|
191次组卷
|
2卷引用:山东省威海市2023-2024学年高一上学期期末考试化学试题
名校
2 . 设 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是
 为阿伏加德罗常数的值,下列说法中正确的是
为阿伏加德罗常数的值,下列说法中正确的是A. 和 和 的固体混合物中含 的固体混合物中含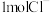 ,则混合物中质子数为 ,则混合物中质子数为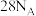 |
B.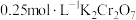 溶液中含有的 溶液中含有的 的数目为 的数目为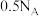 |
C.一定条件下, 与 与 充分反应,转移的电子数为 充分反应,转移的电子数为 |
D.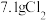 溶于水,所得溶液中 溶于水,所得溶液中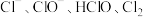 的粒子数之和为 的粒子数之和为 |
您最近一年使用:0次
2024-03-01更新
|
107次组卷
|
2卷引用:山东省威海市2023-2024学年高一上学期期末考试化学试题
名校
解题方法
3 . 某同学配制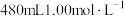 的某溶液,有关操作正确的是
的某溶液,有关操作正确的是
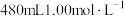 的某溶液,有关操作正确的是
的某溶液,有关操作正确的是A.配制 溶液时,将量筒、烧杯、玻璃棒洗涤2~3次,将洗涤液转入容量瓶中 溶液时,将量筒、烧杯、玻璃棒洗涤2~3次,将洗涤液转入容量瓶中 |
B.配制 溶液时,需量取 溶液时,需量取 、密度为 、密度为 的浓盐酸约 的浓盐酸约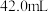 |
C.配制 溶液时,应快速溶解 溶液时,应快速溶解 固体,快速将溶液转移到容量瓶中 固体,快速将溶液转移到容量瓶中 |
D.配制 溶液定容时,摇匀后发现溶液凹液面低于刻度线,加入蒸馏水至刻度线 溶液定容时,摇匀后发现溶液凹液面低于刻度线,加入蒸馏水至刻度线 |
您最近一年使用:0次
2024-03-01更新
|
92次组卷
|
2卷引用:山东省威海市2023-2024学年高一上学期期末考试化学试题
4 . 25℃时,向三元酸 溶液中滴加NaOH溶液,溶液的pH与pX的变化关系如图所示,pX表示
溶液中滴加NaOH溶液,溶液的pH与pX的变化关系如图所示,pX表示 或
或 或
或 。下列说法错误的是
。下列说法错误的是

 溶液中滴加NaOH溶液,溶液的pH与pX的变化关系如图所示,pX表示
溶液中滴加NaOH溶液,溶液的pH与pX的变化关系如图所示,pX表示 或
或 或
或 。下列说法错误的是
。下列说法错误的是
A.曲线c表示 与pH的关系 与pH的关系 |
B.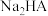 溶液中 溶液中 |
C. 时, 时, |
D.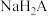 溶液中: 溶液中: |
您最近一年使用:0次
名校
5 . 为消除 对环境的影响,科研人员用
对环境的影响,科研人员用 将
将 还原为,该过程中发生的主要反应有:
还原为,该过程中发生的主要反应有:
反应Ⅰ: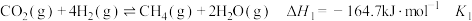
反应Ⅱ:
回答下列问题:
(1)反应
_________  ,
,
___________ (用 、
、 表示)。
表示)。
(2)在恒压密闭容器中,起始充入 、4molH2,在催化剂作用下
、4molH2,在催化剂作用下 平衡转化率、反应相同时间所测得的
平衡转化率、反应相同时间所测得的 实际转化率随温度的变化如图所示;
实际转化率随温度的变化如图所示;

 的选择性
的选择性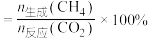 。
。
①下列措施一定能使 的平衡转化率增大的是
的平衡转化率增大的是___________ (填序号)。
A.在原容器中再充入 B.在原容器中再充入
B.在原容器中再充入
C.将水蒸气从体系中分离 D.在原容器中再充入 和
和
②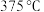 时,在催化剂催化下a点对应
时,在催化剂催化下a点对应
___________  (填“>”“<”“=”);保持温度不变,平衡时
(填“>”“<”“=”);保持温度不变,平衡时 的选择性为80%,则反应Ⅱ的
的选择性为80%,则反应Ⅱ的
___________ (保留两位有效数字)。
③ 时,为使
时,为使 的平衡转化率提高到c点,可将
的平衡转化率提高到c点,可将 的起始量增加到
的起始量增加到 。平衡时
。平衡时 的物质的量为0.2mol,则平衡体系中
的物质的量为0.2mol,则平衡体系中 的物质的量为
的物质的量为___________ ,平衡时 的选择性
的选择性
___________  (保留两位有效数字)。
(保留两位有效数字)。
④ 范围内,平衡时
范围内,平衡时 的选择性随温度的升高而变化的原因是
的选择性随温度的升高而变化的原因是___________ 。
 对环境的影响,科研人员用
对环境的影响,科研人员用 将
将 还原为,该过程中发生的主要反应有:
还原为,该过程中发生的主要反应有:反应Ⅰ:
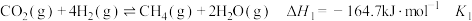
反应Ⅱ:

回答下列问题:
(1)反应

 ,
,
 、
、 表示)。
表示)。(2)在恒压密闭容器中,起始充入
 、4molH2,在催化剂作用下
、4molH2,在催化剂作用下 平衡转化率、反应相同时间所测得的
平衡转化率、反应相同时间所测得的 实际转化率随温度的变化如图所示;
实际转化率随温度的变化如图所示;
 的选择性
的选择性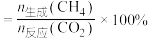 。
。①下列措施一定能使
 的平衡转化率增大的是
的平衡转化率增大的是A.在原容器中再充入
 B.在原容器中再充入
B.在原容器中再充入
C.将水蒸气从体系中分离 D.在原容器中再充入
 和
和
②
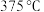 时,在催化剂催化下a点对应
时,在催化剂催化下a点对应
 (填“>”“<”“=”);保持温度不变,平衡时
(填“>”“<”“=”);保持温度不变,平衡时 的选择性为80%,则反应Ⅱ的
的选择性为80%,则反应Ⅱ的
③
 时,为使
时,为使 的平衡转化率提高到c点,可将
的平衡转化率提高到c点,可将 的起始量增加到
的起始量增加到 。平衡时
。平衡时 的物质的量为0.2mol,则平衡体系中
的物质的量为0.2mol,则平衡体系中 的物质的量为
的物质的量为 的选择性
的选择性
 (保留两位有效数字)。
(保留两位有效数字)。④
 范围内,平衡时
范围内,平衡时 的选择性随温度的升高而变化的原因是
的选择性随温度的升高而变化的原因是
您最近一年使用:0次
2024-02-27更新
|
209次组卷
|
2卷引用:山东省威海市2023-2024学年高三上学期期末考试化学试题
6 . 下列实验的设计方案、现象和结论有错误的是
| 选项 | 实验目的 | 设计方案和实验现象 | 结论 |
| A | 检验菠菜中是否含有铁元素 | 取少量菠菜叶剪碎研磨后加水搅拌,取上层清液于试管中,加入稀硝酸后,再加入 溶液,溶液变红 溶液,溶液变红 | 菠菜中含有铁元素 |
| B | 检验尿液中是否含有葡萄糖 | 取尿液适量,向其中加入 至溶液呈碱性,加入新制的 至溶液呈碱性,加入新制的 悬浊液,加热煮沸,产生砖红色沉淀 悬浊液,加热煮沸,产生砖红色沉淀 | 尿液中含有葡萄糖 |
| C | 比较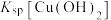 和 和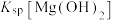 大小 大小 | 向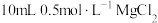 溶液中滴加 溶液中滴加 溶液,充分反应产生白色沉淀,再滴加 溶液,充分反应产生白色沉淀,再滴加 溶液,沉淀变蓝 溶液,沉淀变蓝 | 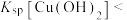 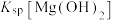 |
| D | 比较配离子 、 、 的稳定性 的稳定性 | 将 \固体溶于水,加入适量浓盐酸后,再加入少量 \固体溶于水,加入适量浓盐酸后,再加入少量 固体。溶液先由粉红色变为蓝色,再由蓝色变成粉红色(已知: 固体。溶液先由粉红色变为蓝色,再由蓝色变成粉红色(已知: 呈粉红色, 呈粉红色, 呈蓝色, 呈蓝色, 呈无色) 呈无色) | 稳定性: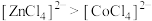 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-27更新
|
226次组卷
|
3卷引用:山东省威海市2023-2024学年高三上学期期末考试化学试题
7 . 黄连素具有清热解毒等功效。实验室从黄连中提取黄连素的操作流程如图所示:

已知:黄连素为黄色针状结晶,属于生物碱,微溶于水和乙醇,易溶于热水及热醇;黄连素的含氧酸盐在水中溶解度较大,不含氧酸盐难溶于水。下列说法错误的是

已知:黄连素为黄色针状结晶,属于生物碱,微溶于水和乙醇,易溶于热水及热醇;黄连素的含氧酸盐在水中溶解度较大,不含氧酸盐难溶于水。下列说法错误的是
| A.加热回流时,将黄连切成碎片的目的是增大接触面积,加快提取速率 |
| B.加热溶解时,加入乙酸的作用是将黄连素转变成含氧酸盐,增大在水中的溶解度 |
| C.试剂a和b可分别选用冰水和热水 |
| D.抽滤③和抽滤④均需要冷却后进行 |
您最近一年使用:0次
2024-02-24更新
|
215次组卷
|
2卷引用:山东省威海市2023-2024学年高三上学期期末考试化学试题
8 . 含硫化合物在生产、科研中应用广泛。回答下列问题:
Ⅰ.常温向 溶液中加入适量的NaOH,溶液中
溶液中加入适量的NaOH,溶液中 、
、 、
、 的分布系数
的分布系数 随pOH的变化如图。
随pOH的变化如图。

(1)下列说法正确的是___________ 。
A.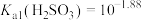
B.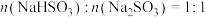 时,溶液显酸性
时,溶液显酸性
C.N点对应的溶液,对水的电离起到抑制作用
(2)M点对应的溶液中,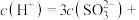
___________ 。(用含离子浓度的关系式表示)
Ⅱ.工业上用NaOH溶液吸收烟气中的 ,再将所得的
,再将所得的 溶液进行电解(装置如图),可实现NaOH的循环再生,同时得到
溶液进行电解(装置如图),可实现NaOH的循环再生,同时得到 。
。

(3)c为___________ (填“阴”“阳”)离子交换膜,b极的电极反应式为___________ 。
Ⅲ.硫代硫酸钠(Na2S2O3)常用作还原剂、脱氯剂等。
利用“化学放大”反应测定少量的碘化物:
①准确移取 含KI的试液,在中性或弱酸性介质中用
含KI的试液,在中性或弱酸性介质中用 氧化为
氧化为 ;
;
②加入过量的KI,用 萃取生成的
萃取生成的 ;
;
③分去水相后,用肼(N2H4)的水溶液将 反萃至水相;
反萃至水相;
④再用过量的 将
将 氧化为
氧化为 ,并除去剩余的
,并除去剩余的 ;
;
⑤加入过量的KI,酸化,加入指示剂,用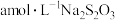 标准溶液滴定,滴定终点消耗
标准溶液滴定,滴定终点消耗 溶液
溶液 。(已知:
。(已知: ;
;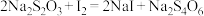 )
)
(4)步骤⑤中指示剂可以选用___________ ;
(5)测定过程中,原试液1mol 消耗
消耗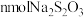 ,即相当于“放大”n倍。本实验中相当于“放大”
,即相当于“放大”n倍。本实验中相当于“放大”___________ 倍;
(6)原试液中KI的浓度为___________  (用含a、
(用含a、 、
、 的字母表示)。
的字母表示)。
Ⅰ.常温向
 溶液中加入适量的NaOH,溶液中
溶液中加入适量的NaOH,溶液中 、
、 、
、 的分布系数
的分布系数 随pOH的变化如图。
随pOH的变化如图。
(1)下列说法正确的是
A.
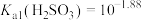
B.
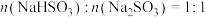 时,溶液显酸性
时,溶液显酸性C.N点对应的溶液,对水的电离起到抑制作用
(2)M点对应的溶液中,
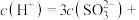
Ⅱ.工业上用NaOH溶液吸收烟气中的
 ,再将所得的
,再将所得的 溶液进行电解(装置如图),可实现NaOH的循环再生,同时得到
溶液进行电解(装置如图),可实现NaOH的循环再生,同时得到 。
。
(3)c为
Ⅲ.硫代硫酸钠(Na2S2O3)常用作还原剂、脱氯剂等。
利用“化学放大”反应测定少量的碘化物:
①准确移取
 含KI的试液,在中性或弱酸性介质中用
含KI的试液,在中性或弱酸性介质中用 氧化为
氧化为 ;
;②加入过量的KI,用
 萃取生成的
萃取生成的 ;
;③分去水相后,用肼(N2H4)的水溶液将
 反萃至水相;
反萃至水相;④再用过量的
 将
将 氧化为
氧化为 ,并除去剩余的
,并除去剩余的 ;
;⑤加入过量的KI,酸化,加入指示剂,用
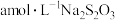 标准溶液滴定,滴定终点消耗
标准溶液滴定,滴定终点消耗 溶液
溶液 。(已知:
。(已知: ;
;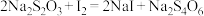 )
)(4)步骤⑤中指示剂可以选用
(5)测定过程中,原试液1mol
 消耗
消耗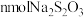 ,即相当于“放大”n倍。本实验中相当于“放大”
,即相当于“放大”n倍。本实验中相当于“放大”(6)原试液中KI的浓度为
 (用含a、
(用含a、 、
、 的字母表示)。
的字母表示)。
您最近一年使用:0次
解题方法
9 . 双氧水在工业、医药等领域应用广泛。某小组采用如下方法制备 并探究
并探究 的分解反应机理。回答下列问题:
的分解反应机理。回答下列问题:
Ⅰ.电解-水解法制备 制备步骤:
制备步骤:
(1)①电解硫酸氢钾饱和溶液,制取 ;
;
②将电解所得 酸化水解制取
酸化水解制取 。电解时阳极反应式为
。电解时阳极反应式为___________ 。

Ⅱ.探究的分解反应机理
①按图1连接装置,检查装置气密性;
②向a中加入60mL15%H2O2,观察现象,通过pH传感器测pH;
③20s时,打开双通阀,向a中加入1滴管 溶液,搅拌,观察现象。反应部分实验数据结果和反应历程见图2和图3(忽略温度的影响)。
溶液,搅拌,观察现象。反应部分实验数据结果和反应历程见图2和图3(忽略温度的影响)。

回答下列问题:
(2)仪器a的名称是___________ ,已知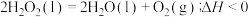 ,据此分析并说明常温常压下
,据此分析并说明常温常压下 能否分解
能否分解___________ ,前20s测得溶液pH为3.47,其原因是___________ (用电离方程式表示)。
(3)步骤③中加入 溶液后的现象为
溶液后的现象为___________ 、溶液颜色由黄色变深,又变回黄色。20~23s pH变化的原因是___________ 。结合图2和图3,23~150s pH变化对应的历程为___________ (用序号表示),150s后pH变化的原因是___________ (用反应式表示)。
(4)加入 溶液后,150s时收集到19.5mL
溶液后,150s时收集到19.5mL ,则用
,则用 的体积变化表示该反应的速率为
的体积变化表示该反应的速率为___________ 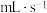 。该实验证明催化剂通过改变反应历程,从而加快反应速率。
。该实验证明催化剂通过改变反应历程,从而加快反应速率。
 并探究
并探究 的分解反应机理。回答下列问题:
的分解反应机理。回答下列问题:Ⅰ.电解-水解法制备
 制备步骤:
制备步骤:(1)①电解硫酸氢钾饱和溶液,制取
 ;
;②将电解所得
 酸化水解制取
酸化水解制取 。电解时阳极反应式为
。电解时阳极反应式为
Ⅱ.探究的分解反应机理
①按图1连接装置,检查装置气密性;
②向a中加入60mL15%H2O2,观察现象,通过pH传感器测pH;
③20s时,打开双通阀,向a中加入1滴管
 溶液,搅拌,观察现象。反应部分实验数据结果和反应历程见图2和图3(忽略温度的影响)。
溶液,搅拌,观察现象。反应部分实验数据结果和反应历程见图2和图3(忽略温度的影响)。
回答下列问题:
(2)仪器a的名称是
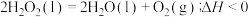 ,据此分析并说明常温常压下
,据此分析并说明常温常压下 能否分解
能否分解(3)步骤③中加入
 溶液后的现象为
溶液后的现象为(4)加入
 溶液后,150s时收集到19.5mL
溶液后,150s时收集到19.5mL ,则用
,则用 的体积变化表示该反应的速率为
的体积变化表示该反应的速率为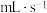 。该实验证明催化剂通过改变反应历程,从而加快反应速率。
。该实验证明催化剂通过改变反应历程,从而加快反应速率。
您最近一年使用:0次
10 . 氨是化肥工业的主要原料,其在国防、涂料等领域应用广泛。回答下列问题:
(1)合成氨反应 的活化能
的活化能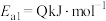 ,则氨分解反应
,则氨分解反应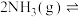
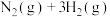 的活化能
的活化能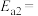
___________  (用含Q、a、b、c的关系式表示)。(已知相关化学键的键能数据如表所示)
(用含Q、a、b、c的关系式表示)。(已知相关化学键的键能数据如表所示)
(2)在体积为2L的密闭容器中充入1mol 和3mol
和3mol ,发生反应
,发生反应 。
。 、
、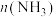 在
在 和
和 温度下的变化曲线如图所示。
温度下的变化曲线如图所示。
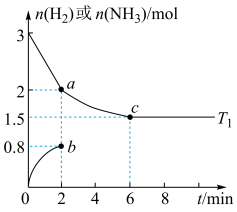
①在___________ (填“ ”“
”“ ”)温度下先达到平衡状态,判断的依据是
”)温度下先达到平衡状态,判断的依据是___________ 。
②a、b、c三点, 的转化率由大到小的顺序为
的转化率由大到小的顺序为___________ ,已知c点之后容器内的压强为P,且保持不变。合成氨反应在 温度下的
温度下的
___________ 。
(3)清华大学科研团队在电催化氮还原合成氨方面取得重大进展。两种条件下的反应历程如图甲所示。

①图乙对应的是图甲中的电催化___________ (填“Ⅰ”“Ⅱ”)。
②由图甲可见,不同历程中 的活化均为决速步骤,理由是
的活化均为决速步骤,理由是___________ 。
③碱性水溶液中,该电催化氮还原合成氨的电极反应式为___________ 。
(1)合成氨反应
 的活化能
的活化能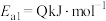 ,则氨分解反应
,则氨分解反应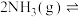
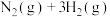 的活化能
的活化能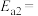
 (用含Q、a、b、c的关系式表示)。(已知相关化学键的键能数据如表所示)
(用含Q、a、b、c的关系式表示)。(已知相关化学键的键能数据如表所示)| 化学键 |  |  |  |
 | a | b | c |
(2)在体积为2L的密闭容器中充入1mol
 和3mol
和3mol ,发生反应
,发生反应 。
。 、
、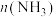 在
在 和
和 温度下的变化曲线如图所示。
温度下的变化曲线如图所示。
①在
 ”“
”“ ”)温度下先达到平衡状态,判断的依据是
”)温度下先达到平衡状态,判断的依据是②a、b、c三点,
 的转化率由大到小的顺序为
的转化率由大到小的顺序为 温度下的
温度下的
(3)清华大学科研团队在电催化氮还原合成氨方面取得重大进展。两种条件下的反应历程如图甲所示。

①图乙对应的是图甲中的电催化
②由图甲可见,不同历程中
 的活化均为决速步骤,理由是
的活化均为决速步骤,理由是③碱性水溶液中,该电催化氮还原合成氨的电极反应式为
您最近一年使用:0次



