1 . 用铁泥(主要成分为Fe2O3,还含有少量FeO和Fe)制备纳米Fe3O4的流程如下。下列说法正确的是

| A.步骤②④发生的反应均为氧化还原反应 |
| B.步骤②中发生的反应为2Fe3++Fe = 3Fe2+、Fe+2H+ = Fe2++H2↑ |
| C.步骤④中使用过量的H2O2有利于提高纳米Fe3O4产率 |
| D.纳米Fe3O4能产生丁达尔效应 |
您最近一年使用:0次
2 . 回答下列问题。
(1)现有6种物质①MgCl2 ②HCl ③SO2 ④K2CO3 ⑤CaO ⑥NaHSO4 ⑦N2。请根据下列标准,对上述物质进行分类(填序号):
①属于共价化合物是___________ 。
②只含离子键的化合物是___________ 。
③含共价键的离子化合物是___________ 。
④如果将NaHSO4溶于水,破坏了NaHSO4中化学键的类型为___________ 。
(2)现有下列9种微粒: 、
、 、
、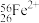 、
、 、
、 、
、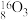 。
。
形成上述6种微粒的核素有___________ 种、元素有___________ 种。
(3)已知有下列物质:①Al ②HCl气体 ③ ④KCl ⑤熔融NaOH,其中能导电的是
④KCl ⑤熔融NaOH,其中能导电的是___________ (填标号,下同);属于电解质的是___________ ;
(1)现有6种物质①MgCl2 ②HCl ③SO2 ④K2CO3 ⑤CaO ⑥NaHSO4 ⑦N2。请根据下列标准,对上述物质进行分类(填序号):
①属于共价化合物是
②只含离子键的化合物是
③含共价键的离子化合物是
④如果将NaHSO4溶于水,破坏了NaHSO4中化学键的类型为
(2)现有下列9种微粒:
 、
、 、
、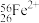 、
、 、
、 、
、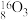 。
。形成上述6种微粒的核素有
(3)已知有下列物质:①Al ②HCl气体 ③
 ④KCl ⑤熔融NaOH,其中能导电的是
④KCl ⑤熔融NaOH,其中能导电的是
您最近一年使用:0次
3 . 已知① ②C2H5OH(g)=C2H5OH(l)
②C2H5OH(g)=C2H5OH(l) 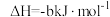 ,③
,③ (a、b、c均>0)。若使
(a、b、c均>0)。若使 酒精液体完全燃烧,最后恢复到室温,则放出的热量为(单位:
酒精液体完全燃烧,最后恢复到室温,则放出的热量为(单位: )
)
 ②C2H5OH(g)=C2H5OH(l)
②C2H5OH(g)=C2H5OH(l) 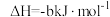 ,③
,③ (a、b、c均>0)。若使
(a、b、c均>0)。若使 酒精液体完全燃烧,最后恢复到室温,则放出的热量为(单位:
酒精液体完全燃烧,最后恢复到室温,则放出的热量为(单位: )
)A.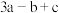 | B.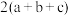 | C.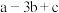 | D.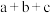 |
您最近一年使用:0次
名校
解题方法
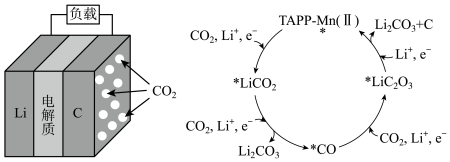
4 .  可充电电池的结构和在催化剂TAPP-Mn(Ⅱ)作用下正极反应可能的历程如图所示。下列说法错误的是
可充电电池的结构和在催化剂TAPP-Mn(Ⅱ)作用下正极反应可能的历程如图所示。下列说法错误的是
 可充电电池的结构和在催化剂TAPP-Mn(Ⅱ)作用下正极反应可能的历程如图所示。下列说法错误的是
可充电电池的结构和在催化剂TAPP-Mn(Ⅱ)作用下正极反应可能的历程如图所示。下列说法错误的是
| A.放电时,电流由C电极流出,经负载流入Li电极 |
B. 电池可以使用 电池可以使用 水溶液做离子导体 水溶液做离子导体 |
C.放电时, 由Li电极向C电极迁移 由Li电极向C电极迁移 |
D.充电时,阳极反应为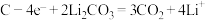 |
您最近一年使用:0次
2024-01-26更新
|
514次组卷
|
4卷引用:2023—2024学年高二上学期化学期末考试模拟试题(一)
名校
解题方法
5 . 常温下,用0.100mol/L盐酸滴定20.00 mL0.100mol/LNH3·H2O溶液,溶液的pH与所加盐酸体积的关系如图所示(不考虑溶液的体积和温度变化)。已知:Kb(NH3·H2O)≈1.6×10-5,1g2.5≈0.4。下列说法错误的是
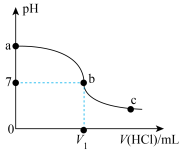

| A.a点对应的pH约为11.1 |
B.b点溶液中, <1 <1 |
| C.曲线包含的全过程中,水的电离程度最大的点在b点 |
D.当溶液中NH4Cl与NH3·H2O浓度比为2:1时,有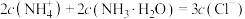 |
您最近一年使用:0次
2024-01-21更新
|
648次组卷
|
3卷引用:2023—2024学年高二上学期化学期末考试模拟试题(一)
23-24高一上·山东聊城·期末
解题方法
6 . X、Y、Z三种主族元素的单质在常温下都是常见的无色气体,在适当条件下,三者之间可以两两发生反应生成分别是双核、三核和四核的甲、乙、丙三种分子,且乙、丙分子中含有X元素的原子个数比为 。请回答下列问题:
。请回答下列问题:
(1)元素X的名称是___________ ,丙分子的电子式为___________ 。
(2)乙在常温下为无色液体,则乙的化学式为___________ 。
(3)化合物丁含X、Y、Z三种元素,丁是一种常见的强酸,将丁与丙按物质的量之比1:1混合后所得物质戊的晶体结构中含有的化学键为___________ (选填序号)。
a.只含共价键 b.只含离子键 c.既含离子键,又含共价键
 。请回答下列问题:
。请回答下列问题:(1)元素X的名称是
(2)乙在常温下为无色液体,则乙的化学式为
(3)化合物丁含X、Y、Z三种元素,丁是一种常见的强酸,将丁与丙按物质的量之比1:1混合后所得物质戊的晶体结构中含有的化学键为
a.只含共价键 b.只含离子键 c.既含离子键,又含共价键
您最近一年使用:0次
名校
解题方法
7 . X、Y、Z、W为四种短周期主族元素,且原子序数依次增大,已知X原子的最外层电子数是其电子层数的2倍,Y是地壳中含量最高的元素,Y原子的最外层电子数是W原子最外层电子数的2倍,Z原子的最外层上只有一个电子,下列说法正确的是
| A.最高价氧化物对应水化物的碱性:Z<W |
| B.Y与Z两种元素只能形成一种化合物 |
| C.X的简单气态氢化物的溶沸点比Y的低 |
| D.X的简单气态氢化物的热稳定性比Y的强 |
您最近一年使用:0次
2024-01-09更新
|
625次组卷
|
3卷引用:2023—2024学年高二上学期化学期末考试模拟试题(一)
2023—2024学年高二上学期化学期末考试模拟试题(一) 江苏省马坝高级中学2023-2024学年高三上学期期中考试化学试卷(已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
名校
8 . 研究电解质在水溶液中的离子反应与平衡有重要的意义。
(1)常温下,用 溶液滴定
溶液滴定 溶液的滴定曲线如下图所示。
溶液的滴定曲线如下图所示。
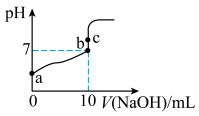
①a点溶液的 pH___________ 1(填“>”、“<”或“=”),请用化学用语解释其原因___________ 。
② b 点溶液中的溶质为___________ (填化学式)。
③c点溶液中,
___________ 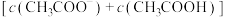 。c点
。c点
___________  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
④a、b、c三点中,水的电离程度最大的点为___________ 。
(2)用电位滴定法模拟测定某醋酸溶液样品中醋酸的含量,操作如下:
已知:该条件下,醋酸和 以物质的量1:1反应时得到的溶液
以物质的量1:1反应时得到的溶液 为8.7。
为8.7。
i.准确量取 醋酸溶液样品,加入蒸馏水至总体积为
醋酸溶液样品,加入蒸馏水至总体积为 ,取其中
,取其中 进行滴定实验,用酸度计检测
进行滴定实验,用酸度计检测 变化;
变化;
ii.逐滴滴入 的
的 溶液,酸度计显示
溶液,酸度计显示 停止滴定,记录消耗的
停止滴定,记录消耗的 溶液的体积V(NaOH);
溶液的体积V(NaOH);
iii.平行测定多次(数据见表1);
iv.分析处理数据。
表1实验数据记录表格
①在滴定过程中,在滴定过程中,若出现下列情况,测定结果偏低的是___________ 。
A.滴定前用待滴定的醋酸溶液润洗锥形瓶
B.在振荡锥形瓶时不慎将瓶内溶液浅出
C.若在滴定过程中不慎将数滴碱液滴锥形瓶外
D.用蒸馏水洗涤碱式滴定管后即使用,没有用碱液润洗
②根据表1中的有效数据,计算消耗的 溶液的平均体积V(NaOH)=
溶液的平均体积V(NaOH)=___________  。该醋酸溶液样品中醋酸的含量是
。该醋酸溶液样品中醋酸的含量是___________  。
。
(3)已知:25℃时 、
、 和
和 的电离平衡常数:
的电离平衡常数:
① 的电离平衡常数表达式
的电离平衡常数表达式
___________ 。
②25℃时,浓度均为 的
的 溶液、
溶液、 溶液、
溶液、 溶液的碱性由大到小的排序是
溶液的碱性由大到小的排序是___________ 。
③25℃时,若初始时次氯酸溶液中 的物质的量浓度为
的物质的量浓度为 ,达到电离平衡时溶液中
,达到电离平衡时溶液中
___________  。
。
④下列化学反应可能发生的是___________ 。
A.
B.
C.
D.
(1)常温下,用
 溶液滴定
溶液滴定 溶液的滴定曲线如下图所示。
溶液的滴定曲线如下图所示。
①a点溶液的 pH
② b 点溶液中的溶质为
③c点溶液中,

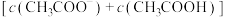 。c点
。c点
 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)④a、b、c三点中,水的电离程度最大的点为
(2)用电位滴定法模拟测定某醋酸溶液样品中醋酸的含量,操作如下:
已知:该条件下,醋酸和
 以物质的量1:1反应时得到的溶液
以物质的量1:1反应时得到的溶液 为8.7。
为8.7。i.准确量取
 醋酸溶液样品,加入蒸馏水至总体积为
醋酸溶液样品,加入蒸馏水至总体积为 ,取其中
,取其中 进行滴定实验,用酸度计检测
进行滴定实验,用酸度计检测 变化;
变化;ii.逐滴滴入
 的
的 溶液,酸度计显示
溶液,酸度计显示 停止滴定,记录消耗的
停止滴定,记录消耗的 溶液的体积V(NaOH);
溶液的体积V(NaOH);iii.平行测定多次(数据见表1);
iv.分析处理数据。
表1实验数据记录表格
| 编号 | 1 | 2 | 3 |
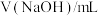 | 23.99 | 24.01 | 24.00 |
A.滴定前用待滴定的醋酸溶液润洗锥形瓶
B.在振荡锥形瓶时不慎将瓶内溶液浅出
C.若在滴定过程中不慎将数滴碱液滴锥形瓶外
D.用蒸馏水洗涤碱式滴定管后即使用,没有用碱液润洗
②根据表1中的有效数据,计算消耗的
 溶液的平均体积V(NaOH)=
溶液的平均体积V(NaOH)= 。该醋酸溶液样品中醋酸的含量是
。该醋酸溶液样品中醋酸的含量是 。
。
(3)已知:25℃时
 、
、 和
和 的电离平衡常数:
的电离平衡常数:| 化学式 |  |  |  |
电离平衡常数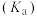 |  |   |  |
 的电离平衡常数表达式
的电离平衡常数表达式
②25℃时,浓度均为
 的
的 溶液、
溶液、 溶液、
溶液、 溶液的碱性由大到小的排序是
溶液的碱性由大到小的排序是③25℃时,若初始时次氯酸溶液中
 的物质的量浓度为
的物质的量浓度为 ,达到电离平衡时溶液中
,达到电离平衡时溶液中
 。
。④下列化学反应可能发生的是
A.

B.

C.

D.

您最近一年使用:0次
2024-01-08更新
|
529次组卷
|
4卷引用:2023—2024学年高二上学期化学期末考试模拟试题(一)
名校
9 . 瑞典化学家舍勒最先用软锰矿和浓盐酸制出了一种黄绿色气体,并且知道了这种气体的某些性质,但他却认为,该气体是一种化合物。直到1810年,英国化学家戴维才确认这种气体是一种单质——氯气。
(1)下列关于氯气的叙述错误的是___________。
(2)下列氯化物中,既能由金属和氯气直接制取,又能由金属和盐酸直接制取的是___________。
(3)氯气可以用来给自来水消毒。某学生用自来水配制下列物质的溶液,不会产生明显药品变质的是___________。
(4)今有 、
、 混合气560mL(标准状况),其中一种气体体积为224mL。光照使两种气体发生反应后恢复到标况,气体体积为
混合气560mL(标准状况),其中一种气体体积为224mL。光照使两种气体发生反应后恢复到标况,气体体积为___________ mL。为了确认剩余的气体是 还是
还是 ,使气体通过水洗气,并使剩余气体干燥后恢复到标况,可能的情况有以下两种:
,使气体通过水洗气,并使剩余气体干燥后恢复到标况,可能的情况有以下两种:
①测量剩佘气体的体积,如果剩余112mL,证明有 剩余;理由是
剩余;理由是___________ 。测量过程进行到末读数环节,忘记调节左右液面相平了,液面左高右低(具体如图所示),测得的气体体积___________ (填“偏大”、“偏小”或“不变”)。
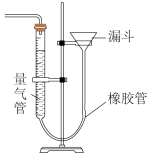
②如果上述水洗液有漂白性,证明有 剩余;理由是
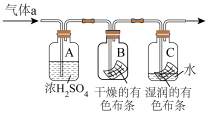
剩余;理由是___________ 。干燥的 没有漂白性,具体验证如下:剩余气体连续通过A、B、C、D装置。B瓶中的现象是
没有漂白性,具体验证如下:剩余气体连续通过A、B、C、D装置。B瓶中的现象是___________ 。不过这一装置设计有缺陷,体现在___________ 。
(5)①一定量的氢气在氯气中燃烧,火焰为___________ 色。
②所得混合物用100mL 的NaOH溶液(密度为
的NaOH溶液(密度为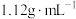 )恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。原NaOH溶液中溶质的物质的量是
)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。原NaOH溶液中溶质的物质的量是___________ mol;
③把NaCl和NaClO统一为通式 (
(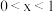 )。根据元素守恒,可知所得溶液中
)。根据元素守恒,可知所得溶液中 的物质的量为
的物质的量为___________ mol。
(1)下列关于氯气的叙述错误的是___________。
| A.氯气能溶于水 | B.氯气是黄绿色气体 |
| C.液氯是氯气的水溶液 | D.单质氯有气、液、固三种状态 |
(2)下列氯化物中,既能由金属和氯气直接制取,又能由金属和盐酸直接制取的是___________。
A. | B. | C. | D. |
(3)氯气可以用来给自来水消毒。某学生用自来水配制下列物质的溶液,不会产生明显药品变质的是___________。
| A.石蕊 | B. | C.NaOH | D.NaCl |
(4)今有
 、
、 混合气560mL(标准状况),其中一种气体体积为224mL。光照使两种气体发生反应后恢复到标况,气体体积为
混合气560mL(标准状况),其中一种气体体积为224mL。光照使两种气体发生反应后恢复到标况,气体体积为 还是
还是 ,使气体通过水洗气,并使剩余气体干燥后恢复到标况,可能的情况有以下两种:
,使气体通过水洗气,并使剩余气体干燥后恢复到标况,可能的情况有以下两种:①测量剩佘气体的体积,如果剩余112mL,证明有
 剩余;理由是
剩余;理由是
②如果上述水洗液有漂白性,证明有
 剩余;理由是
剩余;理由是 没有漂白性,具体验证如下:剩余气体连续通过A、B、C、D装置。B瓶中的现象是
没有漂白性,具体验证如下:剩余气体连续通过A、B、C、D装置。B瓶中的现象是
(5)①一定量的氢气在氯气中燃烧,火焰为
②所得混合物用100mL
 的NaOH溶液(密度为
的NaOH溶液(密度为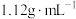 )恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。原NaOH溶液中溶质的物质的量是
)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500mol。原NaOH溶液中溶质的物质的量是③把NaCl和NaClO统一为通式
 (
(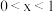 )。根据元素守恒,可知所得溶液中
)。根据元素守恒,可知所得溶液中 的物质的量为
的物质的量为
您最近一年使用:0次
名校
10 . I.利用铁元素“价﹣类”二维图可以从不同角度研究含铁物质的性质及其转化关系,请据此图回答问题:
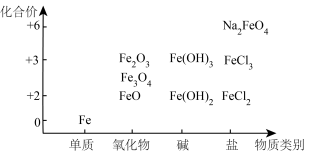
(1)从物质类别和元素价态视角,下列说法中错误的一项是___________
(2)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,从而制造印刷电路板,写出此过程的离子方程式___________ 。某研究人员向上述印刷电路板的废液中加入一定量铁粉,充分反应后,准备过滤并收集滤渣。此时,滤渣的成分不可能是___________ 。
A.没有滤渣 B.有Cu也有Fe C.只有Fe D.只有Cu
II.某学习小组设计了一系列实验,研究FeCl2与FeCl3溶液的性质。
(3)请补充空缺的实验现象:
(4)请写出实验1中第一步所发生反应的离子方程式___________ 。

(1)从物质类别和元素价态视角,下列说法中错误的一项是___________
| A.Na2FeO4具有强氧化性,可以用作水体消毒剂 |
| B.FeO和Fe2O3可分别与水发生反应生成Fe(OH)2和Fe(OH)3 |
| C.可以在FeCl2溶液中放入少量Fe粉,以防止溶液变质 |
| D.可以将Al单质作为还原剂和Fe2O3冶炼Fe单质 |
(2)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,从而制造印刷电路板,写出此过程的离子方程式
A.没有滤渣 B.有Cu也有Fe C.只有Fe D.只有Cu
II.某学习小组设计了一系列实验,研究FeCl2与FeCl3溶液的性质。
(3)请补充空缺的实验现象:
| 序号 | 实验 | 操作现象 |
| 实验1 | 第一步:取2mL酸化的FeCl2溶液于试管中,加入5滴5%H2O2溶液 | 溶液立即变为棕黄色,稍后产生气泡 |
| 第二步:向反应后的溶液中滴入 | 溶液变为血红色 | |
| 实验2 | 取5mLKI﹣淀粉溶液于试管中,加入2mL酸化的FeCl3溶液 |
(4)请写出实验1中第一步所发生反应的离子方程式
您最近一年使用:0次



