解题方法
1 . 燃料电池的种类很多,氢氧燃料电池是目前最成熟的燃料电池,电解质可以是酸性的,也可以是碱性的。回答下列问题:
(1)氢氧燃料电池中,负极上通入的气体是______ ,电池总反应为______ 。
(2)若以稀硫酸作电解质溶液,电池工作时的负极反应为______ 。
(3)若以氢氧化钠溶液作电解质溶液,电池工作时的正极反应为______ 。
(1)氢氧燃料电池中,负极上通入的气体是
(2)若以稀硫酸作电解质溶液,电池工作时的负极反应为
(3)若以氢氧化钠溶液作电解质溶液,电池工作时的正极反应为
您最近一年使用:0次
2 . 海洋是个巨大的资源宝库,利用海水可以获得淡水、食盐、单质溴、单质镁等多种化学物质。结合有关过程回答下列问题:
(1)利用海水制备下列物质,不用通过化学反应过程就可以得到的是______。
(2)氯碱工业中电解饱和食盐水可以得到氢氧化钠、氯气和氢气,写出电解反应的化学方程式______ 。
(3)实验室中通常用浓盐酸和二氧化锰加热制备氯气,反应的化学方程式为______ 。用该种方法制备的氯气中含有杂质,为获得纯净干燥的氯气,可将气体依次通入盛有______ 和浓硫酸的洗气瓶中。
(4)海水中提取镁,先制备MgCl2再进一步获得单质镁,由MgCl2得到单质镁的化学方程式为______ 。
(1)利用海水制备下列物质,不用通过化学反应过程就可以得到的是______。
| A.氢氧化钠 | B.单质镁 | C.淡水 | D.单质溴 |
(3)实验室中通常用浓盐酸和二氧化锰加热制备氯气,反应的化学方程式为
(4)海水中提取镁,先制备MgCl2再进一步获得单质镁,由MgCl2得到单质镁的化学方程式为
您最近一年使用:0次
3 . 实验室欲用98%的浓硫酸(密度为1.84 g·cm-3)配制1.5 mol·L-1的稀硫酸90 mL。
(1)仪器的选择:配制溶液时,下列仪器不需要用到的是___________ (填字母)。
A.天平 B.100 mL容量瓶 C.玻璃棒
D.烧杯 E.量筒 F.250 mL容量瓶
还需要补充的仪器是___________ 。
(2)通过计算,用量筒量取浓硫酸的体积为___________ mL。
(3)稀释浓硫酸,冷却后移液,再进行定容、摇匀等一系列操作。从配制好的溶液中取出10 mL,加水稀释至100 mL,稀释后硫酸的物质的量浓度为___________ mol·L-1。
(1)仪器的选择:配制溶液时,下列仪器不需要用到的是
A.天平 B.100 mL容量瓶 C.玻璃棒
D.烧杯 E.量筒 F.250 mL容量瓶
还需要补充的仪器是
(2)通过计算,用量筒量取浓硫酸的体积为
(3)稀释浓硫酸,冷却后移液,再进行定容、摇匀等一系列操作。从配制好的溶液中取出10 mL,加水稀释至100 mL,稀释后硫酸的物质的量浓度为
您最近一年使用:0次
4 . 现有下列几种物质:
①Al2O3、②CuO、③NaHSO4、④FeCl3、⑤Cl2、⑥NaOH、⑦稀硫酸。回答下列问题:
(1)上述物质中属于碱性氧化物的是___________ (填序号,下同),属于两性氧化物的是___________ ,属于混合物的是___________ 。
(2)上述物质在水中能电离出三种离子的是___________ (填序号);写出④的电离方程式:___________ 。
(3)写出①与⑦反应的离子方程式:___________ 。
①Al2O3、②CuO、③NaHSO4、④FeCl3、⑤Cl2、⑥NaOH、⑦稀硫酸。回答下列问题:
(1)上述物质中属于碱性氧化物的是
(2)上述物质在水中能电离出三种离子的是
(3)写出①与⑦反应的离子方程式:
您最近一年使用:0次
5 . 四种短周期主族元素W、X、Y、Z的原子序数依次增大。W与Y同族,且Y的原子序数是W的2倍;X的原子核外电子层数是其最外层电子数的3倍。回答下列问题:
(1)W在周期表中的位置为___________ 。
(2)W、X、Y的简单离子半径由大到小的顺序为___________ (用离子符号表示)。
(3)W、X形成的两种化合物的化学式为___________ 。
(4)元素Y、Z中非金属性较强的是___________ (用元素符号表示),下列说法能说明这一事实的是___________ (填字母)。
a.常温时两种元素的单质状态不同
b.气态氢化物的稳定性:Z>Y
c.氧化物对应水化物的酸性:Z>Y
d.简单离子的还原性:Y>Z
(1)W在周期表中的位置为
(2)W、X、Y的简单离子半径由大到小的顺序为
(3)W、X形成的两种化合物的化学式为
(4)元素Y、Z中非金属性较强的是
a.常温时两种元素的单质状态不同
b.气态氢化物的稳定性:Z>Y
c.氧化物对应水化物的酸性:Z>Y
d.简单离子的还原性:Y>Z
您最近一年使用:0次
6 . 回答下列问题。
(1)Na、Fe、Cl、Al是中学化学常见的元素。
①含上述某一种元素的常见化合物中,呈淡黄色的是___________ (填化学式)。
②焰色试验中,Na元素燃烧时的焰色为___________ 色,观察K元素燃烧时的焰色需要透过___________ 。
③实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是___________ ,反应的化学方程式为___________ 。
(2)饮用水质量是关系人类健康的重要问题。
氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为___________ 。
(1)Na、Fe、Cl、Al是中学化学常见的元素。
①含上述某一种元素的常见化合物中,呈淡黄色的是
②焰色试验中,Na元素燃烧时的焰色为
③实验室在制备Fe(OH)2时必须隔绝空气,否则发生的现象是
(2)饮用水质量是关系人类健康的重要问题。
氯气是最早用于饮用水消毒的物质,其消毒作用主要是氯气溶于水后生成了次氯酸,该反应的离子方程式为
您最近一年使用:0次
7 . 下列各组离子能在溶液中大量共存的是
| A.钠离子、二价铁离子、硝酸根离子、氢离子 | B.钠离子、氢离子、碳酸氢根离子、硝酸根 |
| C.钾离子、铵根离子、硫酸根离子、钡离子 | D.氢离子、铜离子、硝酸根、硫酸根 |
您最近一年使用:0次
名校
解题方法
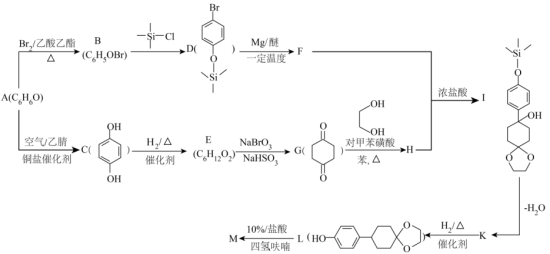
8 . 有机物M是一种制备液晶材料的重要中间体,其合成路线如图:
已知:Ⅰ.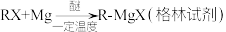
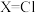 、Br、I
、Br、I
Ⅱ.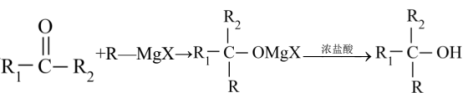
Ⅲ.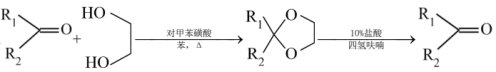
(1)A→B的反应方程式为_______ ,反应类型为_______ 。
(2)反应中使用三甲基氯硅烷( )的作用是
)的作用是_______ ,在本流程中起类似作用的有机物还有_______ (填名称)。
(3)L中的官能团有_______ (填名称)。
(4)符合下列条件的E的同分异构体有种_______ (不考虑立体异构)。
①能与金属钠反应产生氢气②含两个甲基③能发生银镜反应;
其中核磁共振氢谱中显示的六组峰的面积比为 ,且含有1个手性碳原子的有机物结构简式为
,且含有1个手性碳原子的有机物结构简式为_______ (只写一种)。
(5)已知: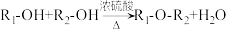 。写出以苯、丙酮和格林试剂为原料合成
。写出以苯、丙酮和格林试剂为原料合成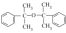 的路线(其他试剂任选)
的路线(其他试剂任选)_______ 。

已知:Ⅰ.
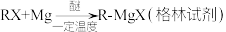
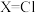 、Br、I
、Br、IⅡ.

Ⅲ.

(1)A→B的反应方程式为
(2)反应中使用三甲基氯硅烷(
 )的作用是
)的作用是(3)L中的官能团有
(4)符合下列条件的E的同分异构体有种
①能与金属钠反应产生氢气②含两个甲基③能发生银镜反应;
其中核磁共振氢谱中显示的六组峰的面积比为
 ,且含有1个手性碳原子的有机物结构简式为
,且含有1个手性碳原子的有机物结构简式为(5)已知:
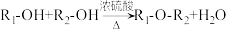 。写出以苯、丙酮和格林试剂为原料合成
。写出以苯、丙酮和格林试剂为原料合成 的路线(其他试剂任选)
的路线(其他试剂任选)
您最近一年使用:0次
名校
解题方法
9 . 硼、砷、铁等元素可形成结构、性质各异的物质,在生产、科研中发挥着重要用途。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是_______ (填标号,下同),用光谱仪可捕捉到发射光谱的是_______ 。
A.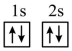 B.
B.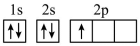
C.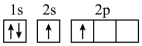 D.
D.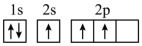
(2)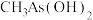 与
与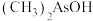 两种含砷有机酸中沸点较高的是
两种含砷有机酸中沸点较高的是_______ (填化学式),原因为_______ 。
(3)LiZnAs晶体的立方晶胞结构如下图1所示,N点原子分数坐标为 ;LiZnAs晶体部分Zn原子被Mn原子代替后可以形成一种新型稀磁半导体
;LiZnAs晶体部分Zn原子被Mn原子代替后可以形成一种新型稀磁半导体 ,其立方晶胞结构如下图2所示。
,其立方晶胞结构如下图2所示。
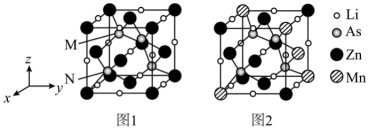
①M点原子分数坐标为_______ 。
②m=_______ 。
③已知 为阿伏加德罗常数的值,
为阿伏加德罗常数的值, 的摩尔质量为
的摩尔质量为 ,晶体密度为
,晶体密度为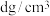 。晶胞中As原子与Mn原子之间的最短距离为
。晶胞中As原子与Mn原子之间的最短距离为_______ nm(列出计算式)。
(4) 的结构如下图所示。
的结构如下图所示。
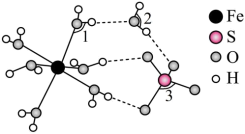
图示 结构中键角1、2、3由大到小的顺序是
结构中键角1、2、3由大到小的顺序是_______ (填序号)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是
A.
 B.
B.
C.
 D.
D.
(2)
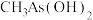 与
与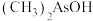 两种含砷有机酸中沸点较高的是
两种含砷有机酸中沸点较高的是(3)LiZnAs晶体的立方晶胞结构如下图1所示,N点原子分数坐标为
 ;LiZnAs晶体部分Zn原子被Mn原子代替后可以形成一种新型稀磁半导体
;LiZnAs晶体部分Zn原子被Mn原子代替后可以形成一种新型稀磁半导体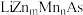 ,其立方晶胞结构如下图2所示。
,其立方晶胞结构如下图2所示。
①M点原子分数坐标为
②m=
③已知
 为阿伏加德罗常数的值,
为阿伏加德罗常数的值,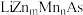 的摩尔质量为
的摩尔质量为 ,晶体密度为
,晶体密度为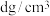 。晶胞中As原子与Mn原子之间的最短距离为
。晶胞中As原子与Mn原子之间的最短距离为(4)
 的结构如下图所示。
的结构如下图所示。
图示
 结构中键角1、2、3由大到小的顺序是
结构中键角1、2、3由大到小的顺序是
您最近一年使用:0次
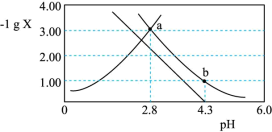
10 . 常温下,向一定浓度 溶液中加入
溶液中加入 ,保持溶液体积和温度不变,测得pH与
,保持溶液体积和温度不变,测得pH与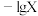 [X为
[X为 、
、 、
、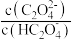 ]变化如下图所示。下列说法错误的是
]变化如下图所示。下列说法错误的是
 溶液中加入
溶液中加入 ,保持溶液体积和温度不变,测得pH与
,保持溶液体积和温度不变,测得pH与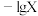 [X为
[X为 、
、 、
、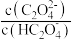 ]变化如下图所示。下列说法错误的是
]变化如下图所示。下列说法错误的是
A.常温下, 的 的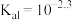 |
B.a点溶液中: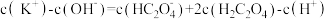 |
| C.从a点到b点溶液中水的电离程度逐渐减小 |
D. 溶液中: 溶液中: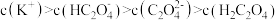 |
您最近一年使用:0次



