名校
解题方法
1 . 下列装置能达到实验目的的是
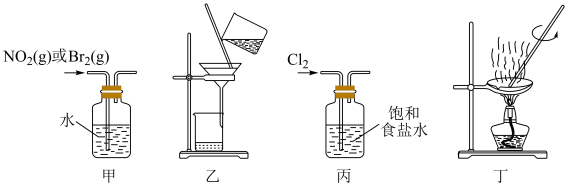

| A.用甲装置鉴别Br2(g)和NO2(g) | B.用乙装置除去水中的苯酚 |
| C.用丙装置收集Cl2 | D.用丁装置灼烧Fe(OH)3固体制得Fe2O3 |
您最近一年使用:0次
2024-03-15更新
|
441次组卷
|
3卷引用:山东省烟台市2023-2024学年高三上学期期末考试化学试题
名校
解题方法
2 . 酞菁和酞菁钴可制得光动力学中的光敏剂,分子结构如图,其中酞菁分子中所有原子共平面,下列说法正确的是
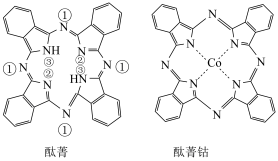
| A.酞菁钴中钴的化合价为+4 |
| B.直径为1.5×10–9 m的酞菁钴分子能透过半透膜 |
| C.酞菁钴中元素的电负性由大到小的顺序为N>C>H>Co |
| D.标注①②的N原子的杂化方式是sp2,③的N原子的杂化方式是sp3 |
您最近一年使用:0次
2024-03-13更新
|
532次组卷
|
3卷引用:山东省烟台市2023-2024学年高三上学期期末考试化学试题
名校
解题方法
3 . 根据下列实验操作和现象能得到相应结论的是
选项 | 操作和现象 | 结论 |
A | 向漂白粉溶液中通入SO2,产生白色沉淀 | 酸性:H2SO3>HClO |
B | 常温下,分别测定1 mol·L–1CH3COONH4溶液和0.1 mol·L–1 CH3COONH4溶液的pH,测得pH都等于7 | 同温下,不同浓度CH3COONH4溶液中水的电离程度相同 |
C | 10 mL 0.1 mol·L–1FeCl3溶液和10 mL 0.1 mol·L–1KI溶液充分反应后分成两等份,一份加入2滴KSCN溶液,溶液变红;另一份加入2滴淀粉溶液,溶液变蓝 | FeCl3和KI的反应存在限度 |
D | 向露置在空气中的Na2O2固体中加入稀盐酸,产生气泡 | Na2O2固体已经变质 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-03-09更新
|
326次组卷
|
2卷引用:山东省烟台市2023-2024学年高三上学期期末考试化学试题
4 . X、Y、Z、W、Q为原子序数依次增大的短周期主族元素,X的原子半径小于Y的原子半径,Z基态原子核外有3个未成对电子,Y的核外电子数与Z的价层电子数相等,Q2是氧化性最强的单质,下列说法正确的是
| A.键能:Z2<W2<Q2 | B.YQ3、ZQ3 均为非极性分子 |
| C.沸点:X2W<XQ | D.同周期中第一电离能介于Y和Z之间的元素有3种 |
您最近一年使用:0次
2024-03-09更新
|
369次组卷
|
4卷引用:山东省烟台市2023-2024学年高三上学期期末考试化学试题
解题方法
5 . 某锂电池的负极材料由锂原子嵌入石墨烯层间形成,其晶胞结构如图甲,下列说法错误的是
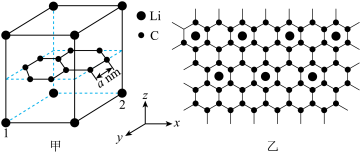

| A.该晶体的化学式为LiC6 |
B.1号、2号Li之间的距离为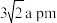 |
| C.图乙可表示该化合物沿z轴的局部投影图 |
| D.利用X射线衍射实验可测得晶胞参数α、β、γ |
您最近一年使用:0次
解题方法
6 . 根据物质及结构分析,下列推断错误的是
| 选项 | 物质及结构 | 推断 |
| A | N-甲基咪唑: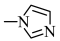 | N-甲基咪唑中σ键的数目为6 |
| B | 邻羟基苯甲酸: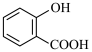 | 邻羟基苯甲酸可形成分子内氢键和分子间氢键 |
| C | 肉桂酸乙酯: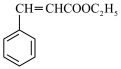 | 肉桂酸乙酯存在顺反异构 |
| D | CrO5: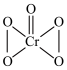 | CrO5中Cr为+6价 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 利用1-甲基萘(1-MN)制备四氢萘类物质(MTLs,包括1-MTL和5-MTL)。反应过程中伴有生成1-甲基十氢萘(1-MD)的副反应,涉及反应如下。各反应的平衡常数K与温度T的关系如图所示。
(1)温度为T1时,反应Ⅱ的平衡常数与反应Ⅲ、Ⅳ的平衡常数之间的关系是K2=___________ (用含K3、K4的代数式表示),曲线a、b中,表示反应Ⅳ的平衡常数随温度变化的曲线为___________ (填代号)。已知1-MTL比5-MTL稳定,则 的数值范围是
的数值范围是___________ (填标号)。
A.< -1 B.-1~0 C.0~1 D.>1
(2)以1mol 1-MN为原料,在1×103 kPa的高压H2氛围下反应(H2的压强近似等于总压),测得不同温度下达平衡时各产物的选择性Si(某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数xi(xi表示物种i物质的量与除H2外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图所示。___________ ,m=___________ ,反应Ⅱ的分压平衡常数Kp=___________ kPa–2。
(3)同温同压下,向温度为T2时的平衡体系中再充入H2,过程中保持H2的浓度不变,反应Ⅰ的化学平衡___________ (填“正向移动”“逆向移动”或“不移动”)。平衡时,1-MTL与5-MTL物质的量浓度之比c(1-MTL):c(5-MTL)=___________ 。
反应Ⅰ: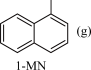 +2H2(g)
+2H2(g)
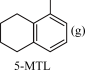 ;ΔH1
;ΔH1
反应Ⅱ: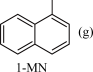 +2H2(g)
+2H2(g)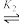
 ;ΔH2
;ΔH2
反应Ⅲ: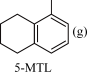 +3H2(g)
+3H2(g)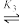
 ;ΔH3
;ΔH3
反应Ⅳ: +3H2(g)
+3H2(g)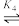
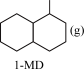 ;ΔH4
;ΔH4

(1)温度为T1时,反应Ⅱ的平衡常数与反应Ⅲ、Ⅳ的平衡常数之间的关系是K2=
 的数值范围是
的数值范围是A.< -1 B.-1~0 C.0~1 D.>1
(2)以1mol 1-MN为原料,在1×103 kPa的高压H2氛围下反应(H2的压强近似等于总压),测得不同温度下达平衡时各产物的选择性Si(某生成物i的物质的量与消耗1-MN的物质的量之比)和物质的量分数xi(xi表示物种i物质的量与除H2外其他各物种总物质的量之比)随1-MN平衡转化率y的变化关系如图所示。
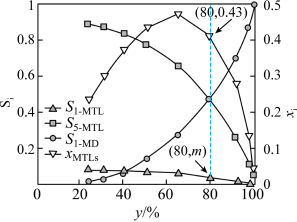
(3)同温同压下,向温度为T2时的平衡体系中再充入H2,过程中保持H2的浓度不变,反应Ⅰ的化学平衡
您最近一年使用:0次
8 . 环烷酸钴[(C5H9)(CH2)3COO]2Co可作合成橡胶的催化剂,实验室以CoCl2、环烷酸[C5H9(CH2)3COOH]等为原料制备环烷酸钴。回答下列问题:
Ⅰ.CoCl2的制备
实验室用如图实验装置制备纯净的CoCl2(CoCl2易潮解)。
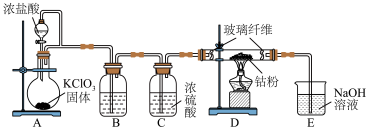
(1)A中发生反应的离子方程式为___________ 。
(2)B中盛放的试剂为___________ ;图示装置存在一处缺陷会导致产品不纯,改进的措施是___________ 。
(3)SOCl2遇水极易反应生成两种酸性气体,常作吸水剂。某实验小组设计用CoCl2·6H2O和SOCl2反应制备无水CoCl2,反应的化学方程式为___________ 。
Ⅱ.环烷酸钴的制备
控制温度90~95 ℃,向环烷酸中滴入一定浓度NaOH溶液,反应约2 h后,再加入一定浓度CoCl2溶液,得到含有环烷酸钴的水溶液,分离提纯得环烷酸钴粗产品。
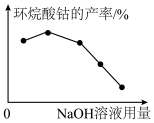
(4)实验中NaOH溶液的用量对环烷酸钴产率的影响如图所示,NaOH溶液过量导致环烷酸钴产率降低的原因是___________ 。
Ⅲ.环烷酸钴纯度的测定
步骤①:准确称取m g环烷酸钴产品,加入少量稀硫酸使其溶解,将溶液转移至250 mL容量瓶,定容。
步骤②:移取25.00 mL上述溶液于锥形瓶中,加入0.0500 mol∙L–1EDTA标准溶液25.00 mL。充分反应后,以铬黑T为指示剂,用0.0500 mol∙L–1锌标准溶液滴定过量的EDTA,消耗锌标准溶液5.00 mL。
已知:环烷酸钴摩尔质量为M g∙mol–1;EDTA与金属离子以1:1形成稳定配合物。
(5)产品中环烷酸钴的纯度为___________ (用含字母的式子表示)。下列情况会导致产品纯度测定值偏低的是___________ 。
A.产品中存在[(C5H9)(CH2)3COO]3Co B.步骤①中定容时俯视刻度线
C.步骤①中转移溶液时未洗涤烧杯 D.步骤②中滴定管未用锌标准溶液润洗
Ⅰ.CoCl2的制备
实验室用如图实验装置制备纯净的CoCl2(CoCl2易潮解)。

(1)A中发生反应的离子方程式为
(2)B中盛放的试剂为
(3)SOCl2遇水极易反应生成两种酸性气体,常作吸水剂。某实验小组设计用CoCl2·6H2O和SOCl2反应制备无水CoCl2,反应的化学方程式为
Ⅱ.环烷酸钴的制备
控制温度90~95 ℃,向环烷酸中滴入一定浓度NaOH溶液,反应约2 h后,再加入一定浓度CoCl2溶液,得到含有环烷酸钴的水溶液,分离提纯得环烷酸钴粗产品。
(4)实验中NaOH溶液的用量对环烷酸钴产率的影响如图所示,NaOH溶液过量导致环烷酸钴产率降低的原因是

Ⅲ.环烷酸钴纯度的测定
步骤①:准确称取m g环烷酸钴产品,加入少量稀硫酸使其溶解,将溶液转移至250 mL容量瓶,定容。
步骤②:移取25.00 mL上述溶液于锥形瓶中,加入0.0500 mol∙L–1EDTA标准溶液25.00 mL。充分反应后,以铬黑T为指示剂,用0.0500 mol∙L–1锌标准溶液滴定过量的EDTA,消耗锌标准溶液5.00 mL。
已知:环烷酸钴摩尔质量为M g∙mol–1;EDTA与金属离子以1:1形成稳定配合物。
(5)产品中环烷酸钴的纯度为
A.产品中存在[(C5H9)(CH2)3COO]3Co B.步骤①中定容时俯视刻度线
C.步骤①中转移溶液时未洗涤烧杯 D.步骤②中滴定管未用锌标准溶液润洗
您最近一年使用:0次
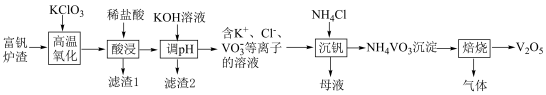
9 . 工业上以富钒炉渣(主要含FeO·V2O3、V2O5和少量的SiO2、Al2O3等)为原料制备V2O5的工艺流程如下:
已知:①+ 5价钒元素在溶液中的存在形式与溶液pH的关系:
②Ksp[Fe(OH)3]=2.6×10–39;Ksp[Al(OH)3]=1.0×10–33;Ksp(NH4VO3)=1.6×10–3
回答下列问题:
(1)“高温氧化”前将富钒炉渣研磨粉碎的目的是___________ ;“高温氧化”过程中发生主要反应的化学方程式为___________ 。
(2)滤渣1的主要成分为___________ ;“调pH”时需将Fe3+、Al3+除尽(浓度≤1×10–5 mol∙L–1时,可认为已除尽),需调节pH的范围为___________ 。
(3)若“沉钒”前溶液中c(VO )=0.2 mol∙L–1,忽略溶液体积变化,为使钒元素的沉降率达到99%,至少应调节c(NH
)=0.2 mol∙L–1,忽略溶液体积变化,为使钒元素的沉降率达到99%,至少应调节c(NH )为
)为___________ mol·L–1。过滤、洗涤、干燥得到NH4VO3沉淀,检验NH4VO3沉淀是否洗净的操作是___________ 。
(4)“焙烧”时生成两种参与大气循环的无毒物质,则该反应的化学方程式为___________ 。

已知:①+ 5价钒元素在溶液中的存在形式与溶液pH的关系:
| 溶液pH | <1.0 | 1.0~4.0 | 4.0~6.0 | 6.0~8.5 | 8.5~13.0 | >13.0 |
| 钒元素存在形式 | VO | V2O5 | 多矾酸根 | VO | 多矾酸根 | VO |
| 备注 | 多矾酸盐在水中溶解度较小 | |||||
回答下列问题:
(1)“高温氧化”前将富钒炉渣研磨粉碎的目的是
(2)滤渣1的主要成分为
(3)若“沉钒”前溶液中c(VO
 )=0.2 mol∙L–1,忽略溶液体积变化,为使钒元素的沉降率达到99%,至少应调节c(NH
)=0.2 mol∙L–1,忽略溶液体积变化,为使钒元素的沉降率达到99%,至少应调节c(NH )为
)为(4)“焙烧”时生成两种参与大气循环的无毒物质,则该反应的化学方程式为
您最近一年使用:0次
10 . 硫是组成生命的重要元素。回答下列问题:
(1)基态硫原子的价电子轨道表示式为___________ 。
(2)广谱杀虫剂硫酰氟(SO2F2)常温常压下为无色气体,固态SO2F2的晶体类型为___________ ,S原子的轨道杂化方式为___________ ,其F-S-F键角___________ 硫酰氯(SO2Cl2)中的Cl-S-Cl键角(填“>”或“<”),原因是___________ 。
(3)硫代硫酸根(S2O )可看作是SO
)可看作是SO 中的一个O原子被S原子取代的产物,S2O
中的一个O原子被S原子取代的产物,S2O 的空间结构是
的空间结构是___________ ;工业上,S2O 常作为配体与金属阳离子形成配合物,除O原子外可做配位原子的是
常作为配体与金属阳离子形成配合物,除O原子外可做配位原子的是___________ (填“中心”或“端基”)S原子。
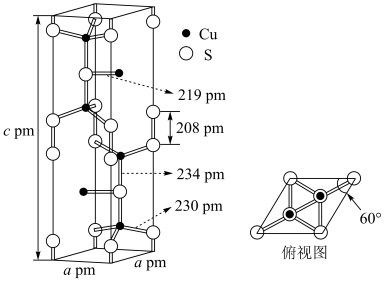
(4)天然硫化铜俗称铜蓝,其晶胞结构如图。已知晶胞中含S ,则一个晶胞中含有
,则一个晶胞中含有___________ 个Cu2+,若阿伏加德罗常数的值为NA,则该晶体的密度ρ=___________ g·cm–3(用含NA的代数式表示)。
(1)基态硫原子的价电子轨道表示式为
(2)广谱杀虫剂硫酰氟(SO2F2)常温常压下为无色气体,固态SO2F2的晶体类型为
(3)硫代硫酸根(S2O
 )可看作是SO
)可看作是SO 中的一个O原子被S原子取代的产物,S2O
中的一个O原子被S原子取代的产物,S2O 的空间结构是
的空间结构是 常作为配体与金属阳离子形成配合物,除O原子外可做配位原子的是
常作为配体与金属阳离子形成配合物,除O原子外可做配位原子的是(4)天然硫化铜俗称铜蓝,其晶胞结构如图。已知晶胞中含S
 ,则一个晶胞中含有
,则一个晶胞中含有
您最近一年使用:0次



