名校
解题方法
1 . 沿海电厂采用海水为冷却水,但在排水管中生物的附着和滋生会阻碍冷却水排放并降低冷却效率,为解决这一问题,通常在管道口设置一对惰性电极(如图所示),通入一定的电流。
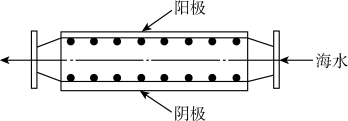
| A.阳极发生反应是Cl-被氧化 |
| B.管道中可以生成氧化灭杀附着生物的NaClO |
| C.阴极生成的电极反应:2H2O+2e-=2OH-+H2↑ |
| D.阳极表面形成的Mg(OH)2等积垢需要定期清理 |
您最近一年使用:0次
名校
解题方法
2 . [W10Ox]y的结构如图所示,下列说法不正确的是

A.结构中基本单元化学式为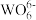 |
| B.[W10Ox]y中,x=32,y=4- |
| C.它属于同多酸类离子 |
| D.基本单元结构为八面体,其中有6个氧原子共顶点 |
您最近一年使用:0次
名校
解题方法
3 . XSO4(aq)与NaOH(aq)反应,定量生成X3(OH)4SO4(s)和Na2SO4(aq)。1.0mol/L的XSO4和1.0mol/LNaOH混合,总体积为50mL(体积可加合)。为了得到最大的沉淀量,这两种溶液的体积应取
| A.29mLNaOH+21mLXSO4 | B.21mLNaOH+29mLXSO4 |
| C.15mLNaOH+35mLXSO4 | D.20mLNaOH+30mLXSO4 |
您最近一年使用:0次
名校
4 . 已知: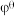 (Fe3+/Fe2+)=+0.77V,
(Fe3+/Fe2+)=+0.77V,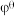 (Br2/Br-)=+1.07V,
(Br2/Br-)=+1.07V,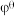 (H2O2/H2O)=+1.78V,
(H2O2/H2O)=+1.78V,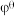 (Sn4+/Sn2+)=+0.15V,则下列各组物质在标准态下能共存的是
(Sn4+/Sn2+)=+0.15V,则下列各组物质在标准态下能共存的是
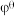 (Fe3+/Fe2+)=+0.77V,
(Fe3+/Fe2+)=+0.77V,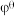 (Br2/Br-)=+1.07V,
(Br2/Br-)=+1.07V,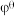 (H2O2/H2O)=+1.78V,
(H2O2/H2O)=+1.78V,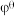 (Sn4+/Sn2+)=+0.15V,则下列各组物质在标准态下能共存的是
(Sn4+/Sn2+)=+0.15V,则下列各组物质在标准态下能共存的是| A.Fe3+,Sn2+ | B.Sn4+,Fe2+ | C. Sn2+,Br2 | D.H2O2,Fe2+ |
您最近一年使用:0次
名校
5 . 已知铁元素的电势图为:FeO
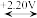 Fe3+
Fe3+ Fe2+
Fe2+ Fe,
Fe,
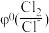 =+1.36V。下列有关说法正确的是
=+1.36V。下列有关说法正确的是

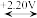 Fe3+
Fe3+ Fe2+
Fe2+ Fe,
Fe,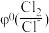 =+1.36V。下列有关说法正确的是
=+1.36V。下列有关说法正确的是| A.Fe2+在水溶液中可发生歧化反应 |
| B.无论在酸性或碱性条件下,Fe均可还原水 |
C. 在水溶液中可稳定存在 在水溶液中可稳定存在 |
D.Cl2无论在何条件下均不能氧化Fe3+生成 |
您最近一年使用:0次
名校
6 . 同温同浓度的下列水溶液中,使溶液沸点升高最多的溶质是
| A.CuSO4 | B.K2SO4 | C.Al2(SO4)3 | D.KAl(SO4)2 |
您最近一年使用:0次
7 . 已知银氨溶液配离子的1gβ1、lgβ2分别为3.4和7.4,则AgCl在0.01mol/LNH3水中存在的溶解度为mol·L-1[Ksp(AgCl)=1.8×10-10]
| A.8.0×10-6 | B.9.6×10-5 | C.6.7×10-4 | D.8.4×10-7 |
您最近一年使用:0次
名校
8 . 黄色固体X,可能含有漂白粉、FeSO4、Fe2(SO4)3、CuCl2、KI之中的几种或全部。将X与足量的水作用,得到深棕色固体混合物Y和无色碱性溶液Z。下列结论合理的是
| A.X中必有CuCl2,可能含有KI、FeSO4 |
| B.X中必有漂白粉和CuCl2而Fe2(SO4)3和FeSO4至少有一种 |
| C.Y中必有Cu(OH)2和Fe(OH)3,可能有I2 |
| D.用H2SO4酸化溶液Z,若有黄绿色气体放出,说明X中含有CuCl2 |
您最近一年使用:0次
名校
9 . 已知22℃下水的蒸气压为2.7kPa,在该温度和100.0kPa下,用排水集气法收集到H2(g)0.05mol,则干燥后H2(g)的体积应为
| A.1.26L | B.2.45L | C.12.6L | D.24.5L |
您最近一年使用:0次
10 . 一块铜板被等分成两块,Cu(a)和Cu(b);锤打Cu(a),Cu(b)不动。再由Cu(a)、Cu(b)及CuSO4溶液组成电池:Cu(a)|CuSO4(cmol·L-1)|Cu(b),测得电动势E>0,因为Cu(a)的
| A.△S>0,△H=0 | B.△S>0,△H<0 |
| C.△S<0,△H=0 | D.△S<0,△H<0 |
您最近一年使用:0次



