1 . 化学计量是研究化学的重要工具。回答下列有关问题:
(1)28g氮气中含有的原子数约为_______ 个,标准状况下的体积为_______ L。
(2)7.8g 固体中含有离子的总物质的量为
固体中含有离子的总物质的量为_______ mol。
(3)在含有 、
、 、
、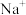 、
、 、
、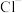 的溶液中,
的溶液中, ,若
,若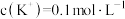 ,则
,则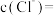
_______  。
。
(4)某气体纯净物在标准状况下的密度为1.25 ,且每个气体分子中含有两个相同原子,则该气体的名称是
,且每个气体分子中含有两个相同原子,则该气体的名称是_______ 。
(5)27g某二价金属氯化物中含有0.4mol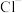 ,则该物质的化学式为
,则该物质的化学式为_______ 。
(6)标准状况下,由CO与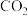 组成的混合气体密度为
组成的混合气体密度为 ,则该混合气体中
,则该混合气体中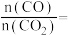
_______ (用含 的分式表示,不需要化简)。
的分式表示,不需要化简)。
(1)28g氮气中含有的原子数约为
(2)7.8g
 固体中含有离子的总物质的量为
固体中含有离子的总物质的量为(3)在含有
 、
、 、
、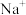 、
、 、
、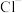 的溶液中,
的溶液中, ,若
,若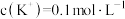 ,则
,则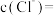
 。
。(4)某气体纯净物在标准状况下的密度为1.25
 ,且每个气体分子中含有两个相同原子,则该气体的名称是
,且每个气体分子中含有两个相同原子,则该气体的名称是(5)27g某二价金属氯化物中含有0.4mol
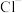 ,则该物质的化学式为
,则该物质的化学式为(6)标准状况下,由CO与
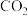 组成的混合气体密度为
组成的混合气体密度为 ,则该混合气体中
,则该混合气体中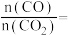
 的分式表示,不需要化简)。
的分式表示,不需要化简)。
您最近一年使用:0次
名校
解题方法
2 . 将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+2D(g)反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6mol,C的物质的量为0.8 mol。
2C(g)+2D(g)反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为________ 。
(2)反应前A的物质的量浓度是________ mol·L-1 。
(3)10 s末,生成物D的物质的量浓度为____ mol·L-1。
(4)A与B的平衡转化率之比为________ 。
(5)反应过程中容器内气体的平均相对分子质量变化是________ (填“增大”、“减小”或“不变”)。
 2C(g)+2D(g)反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6mol,C的物质的量为0.8 mol。
2C(g)+2D(g)反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6mol,C的物质的量为0.8 mol。(1)用C表示10 s内反应的平均反应速率为
(2)反应前A的物质的量浓度是
(3)10 s末,生成物D的物质的量浓度为
(4)A与B的平衡转化率之比为
(5)反应过程中容器内气体的平均相对分子质量变化是
您最近一年使用:0次
名校
3 . 将NaOH、MgCl2、AlCl3三种固体组成的混合物溶于足量水后,产生1.16 g白色沉淀,再向所得浊液中逐渐加入1.00 mol/L HCl溶液,加入HCl溶液的体积与生成沉淀的关系如下图所示。

试回答:
(1)A点的沉淀的化学式为________ ,理由是_______________________________________ ;
(2)写出A点至B点发生反应的离子方程式:_____________________________________ ;
(3)原混合物中AlCl3的质量是________ g,NaOH的物质的量是________ mol。

试回答:
(1)A点的沉淀的化学式为
(2)写出A点至B点发生反应的离子方程式:
(3)原混合物中AlCl3的质量是
您最近一年使用:0次
2018-01-16更新
|
804次组卷
|
2卷引用:安徽省淮南市第二中学2017-2018学年高一上学期第二次月考化学试题



