解题方法
1 . 已知H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
(1)计算H2S的平衡转化率a=_____ (写出计算过程)。
(2)计算浓度平衡常数K=_____ 。(写出计算过程)。
 COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。
COS(g)+H2O(g),在610K时,将0.10molCO2与0.40molH2S充入1L的空钢瓶中,反应平衡后水的物质的量分数为0.02。(1)计算H2S的平衡转化率a=
(2)计算浓度平衡常数K=
您最近一年使用:0次
2 . 将标准状况下 溶于
溶于 水中,计算生成的硝酸浓度
水中,计算生成的硝酸浓度_____ (忽略溶液体积的变化)。
 溶于
溶于 水中,计算生成的硝酸浓度
水中,计算生成的硝酸浓度
您最近一年使用:0次
解题方法
3 . 为测定某种铝镁合金中铝的质量分数,探究小组进行了实验:称取质量为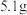 的合金,加入的稀盐酸,恰好完全反应,并产生了
的合金,加入的稀盐酸,恰好完全反应,并产生了 的氢气。计算铝镁合金中铝的质量分数是多少
的氢气。计算铝镁合金中铝的质量分数是多少_____ 。
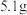 的合金,加入的稀盐酸,恰好完全反应,并产生了
的合金,加入的稀盐酸,恰好完全反应,并产生了 的氢气。计算铝镁合金中铝的质量分数是多少
的氢气。计算铝镁合金中铝的质量分数是多少
您最近一年使用:0次
解题方法
4 . 100mL6.0mol•L-1稀硝酸,恰好使铜和氧化铜完全溶解,同时收集到标准状况下NO2.24L。请回答以下问题:
(1)铜和稀硝酸反应的化学方程式_______ ,该反应中氧化剂和还原剂的物质的量之比为______ 。
(2)原混合物中铜的物质的量为多少_______ ?氧化铜的质量为多少_______ ?(写出计算过程)
(1)铜和稀硝酸反应的化学方程式
(2)原混合物中铜的物质的量为多少
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题:
(1)某化工厂用氯气与石灰乳生产漂白粉,该厂出厂产品说明书如下:

漂白粉的主要成分是CaCl2和Ca(ClO)2,其中有效成分为Ca(ClO)2,长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式_______ ,_______ 。
(2)若用43.50g二氧化锰与足量浓盐酸(质量分数为63.50%)完全反应,制取氯气。求:
①所得气体的质量为_______ 。
②若将所得气体全部用石灰乳吸收,所制得的漂白粉中所含有效成分的质量为_______ 。
(已知MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O ,本题要求写出计算步骤,答案保留2位小数)
MnCl2+Cl2↑+2H2O ,本题要求写出计算步骤,答案保留2位小数)
(1)某化工厂用氯气与石灰乳生产漂白粉,该厂出厂产品说明书如下:

漂白粉的主要成分是CaCl2和Ca(ClO)2,其中有效成分为Ca(ClO)2,长期露置在空气中会变质,写出漂白粉变质过程中涉及的化学方程式
(2)若用43.50g二氧化锰与足量浓盐酸(质量分数为63.50%)完全反应,制取氯气。求:
①所得气体的质量为
②若将所得气体全部用石灰乳吸收,所制得的漂白粉中所含有效成分的质量为
(已知MnO2+4HCl(浓)
 MnCl2+Cl2↑+2H2O ,本题要求写出计算步骤,答案保留2位小数)
MnCl2+Cl2↑+2H2O ,本题要求写出计算步骤,答案保留2位小数)
您最近一年使用:0次
解题方法
6 . 一定温度下,在某体积为2L的密闭容器中充入1.5molNO2和2molCO,在一定条件下发生反应:NO2(g)+CO(g) CO2(g)+NO(g),2min时,测得容器中NO的物质的量为0.5mol。
CO2(g)+NO(g),2min时,测得容器中NO的物质的量为0.5mol。
(1)此段时间内,用CO2表示的平均反应速率_______ 。
(2)2min时,CO的转化率_______ 。
(3)平衡时,CO为1mol,求CO2的体积分数_______ 。
 CO2(g)+NO(g),2min时,测得容器中NO的物质的量为0.5mol。
CO2(g)+NO(g),2min时,测得容器中NO的物质的量为0.5mol。(1)此段时间内,用CO2表示的平均反应速率
(2)2min时,CO的转化率
(3)平衡时,CO为1mol,求CO2的体积分数
您最近一年使用:0次
7 . 在真空密闭容器内加入amolPH4I固体,在一定温度下发生如下反应:
PH4I(s) PH3(g)+HI(g)
PH3(g)+HI(g)
4PH3(g) P4(g)+6H2(g)
P4(g)+6H2(g)
2HI(g) H2(g)+I2(g)
H2(g)+I2(g)
以上三个反应建立平衡后,测得HI为bmol,I2为cmol,H2为dmol。
(1)平衡后,增大压强,容器内n(I2)将___ (填“增加”、“减小”或“不变”)。
(2)计算平衡后容器内P4(g)和PH3(g)的物质的量(列出计算过程)___ 。
PH4I(s)
 PH3(g)+HI(g)
PH3(g)+HI(g)4PH3(g)
 P4(g)+6H2(g)
P4(g)+6H2(g)2HI(g)
 H2(g)+I2(g)
H2(g)+I2(g)以上三个反应建立平衡后,测得HI为bmol,I2为cmol,H2为dmol。
(1)平衡后,增大压强,容器内n(I2)将
(2)计算平衡后容器内P4(g)和PH3(g)的物质的量(列出计算过程)
您最近一年使用:0次
解题方法
8 . 燃烧法是测定有机物分子式的一种重要方法。将0.1mol某烃在氧气中完全燃烧,得到二氧化碳在标准状况下体积为11.2L,生成水为10.8g,求:
(1)该烃的分子式___________ 。
(2)写出可能的结构简式___________ 。
(1)该烃的分子式
(2)写出可能的结构简式
您最近一年使用:0次
2021-07-09更新
|
410次组卷
|
2卷引用:安徽省蚌埠市2020-2021学年高一下学期期末考试化学试题
解题方法
9 . 某化学兴趣小组同学在盛有 20g石灰石的烧杯中加入 200mL稀盐酸,恰好完全反应,生成 3.36L CO2(标准状况下)。(假设石灰石中其他成分不与稀盐酸反应) 计算:
(1)石灰石中 CaCO3的质量分数_____ 。
(2)所加稀盐酸的物质的量浓度_____ 。
(1)石灰石中 CaCO3的质量分数
(2)所加稀盐酸的物质的量浓度
您最近一年使用:0次
名校
解题方法
10 . 物质的量是高中化学常用的物理量,请完成以下有关计算:
(1)标准状况下,0.5molO2的体积约为___________ L。
(2)标准状况下,含有相同氧原子数的CO和CO2的体积之比为___________ 。
(3)5.85gNaCl溶于水配成200mL溶液,该溶液溶质的物质的量浓度为___________ mol/L。
(4)将21.2g碳酸氢钠粉末与足量盐酸完全反应后,产生标准状况下气体的体积为___________ L。
(5)钠有两种氧化物,其中能用于呼吸面具和潜水艇中作为氧气来源的氧化物是:___________ (填化学式)。
(6)固体碳酸钠中含有碳酸氢钠杂质,除去此杂质的简单方法是___________ (填“萃取”或“加热”或“蒸馏”)。
(1)标准状况下,0.5molO2的体积约为
(2)标准状况下,含有相同氧原子数的CO和CO2的体积之比为
(3)5.85gNaCl溶于水配成200mL溶液,该溶液溶质的物质的量浓度为
(4)将21.2g碳酸氢钠粉末与足量盐酸完全反应后,产生标准状况下气体的体积为
(5)钠有两种氧化物,其中能用于呼吸面具和潜水艇中作为氧气来源的氧化物是:
(6)固体碳酸钠中含有碳酸氢钠杂质,除去此杂质的简单方法是
您最近一年使用:0次



