名校
1 . 一定温度下,在容积为VL的密闭容器中进行反应,M、N两种气体的物质的量随时间的变化曲线如图所示:
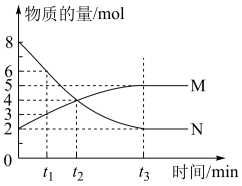
(1)该反应的化学反应方程式是___________ ;
(2) t 1到t 2时刻,以M的浓度变化表示的平均反应速率为:___________ ;
(3)若达到平衡状态的时间是4 min,N物质在该4 min内的平均反应速率为1.5mol⋅L−1⋅min−1,则此容器的容积为V=___________ L;
(4)反应A(g)+B(g) ⇌2C(g),当改变下列条件时,会加快反应速率的是___________ (填序号)
①降低温度 ②保持容器的体积不变,充入氦气
③加入催化剂 ④保持容器的体积不变,增加A(g)的物质的量
(5)用 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图:
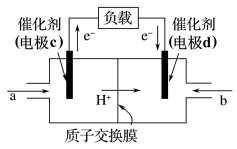
①则电极d是___________  填“正极”或“负极”),电极d的电极反应式为
填“正极”或“负极”),电极d的电极反应式为___________ ;
②若线路中转移2mol电子,则该燃料电池理论上消耗的 在标准状况下的体积为
在标准状况下的体积为___________ L。

(1)该反应的化学反应方程式是
(2) t 1到t 2时刻,以M的浓度变化表示的平均反应速率为:
(3)若达到平衡状态的时间是4 min,N物质在该4 min内的平均反应速率为1.5mol⋅L−1⋅min−1,则此容器的容积为V=
(4)反应A(g)+B(g) ⇌2C(g),当改变下列条件时,会加快反应速率的是
①降低温度 ②保持容器的体积不变,充入氦气
③加入催化剂 ④保持容器的体积不变,增加A(g)的物质的量
(5)用
 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图:
①则电极d是
 填“正极”或“负极”),电极d的电极反应式为
填“正极”或“负极”),电极d的电极反应式为②若线路中转移2mol电子,则该燃料电池理论上消耗的
 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
2021-07-09更新
|
840次组卷
|
4卷引用:安徽省安庆市2020-2021学年高一下学期期末考试化学试题
名校
解题方法
2 . (1)常温下,已知0.1mol·L-1一元酸HA溶液中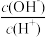 =1×108。
=1×108。
①常温下,0.1mol·L-1HA溶液的pH=___ ;写出该酸(HA)与NaOH溶液反应的离子方程式:___ 。
②0.2mol·L1HA溶液与0.1mol·L1NaOH溶液等体积混合后所得溶液中:c(H+)+c(HA)-c(OH-)=___ mol·L1。(溶液体积变化忽略不计)
(2)t℃时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数Kw=___ 。
①该温度下(t℃),将100mL0.1mol·L1的稀H2SO4溶液与100mL0.4mol·L1的NaOH溶液混合后(溶液体积变化忽略不计),溶液的pH=___ 。
②该温度下(t℃),1体积的稀硫酸和10体积的NaOH溶液混合后溶液呈中性,则稀硫酸的pH(pHa)与NaOH溶液的pH(pHb)的关系是:___ 。
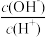 =1×108。
=1×108。①常温下,0.1mol·L-1HA溶液的pH=
②0.2mol·L1HA溶液与0.1mol·L1NaOH溶液等体积混合后所得溶液中:c(H+)+c(HA)-c(OH-)=
(2)t℃时,有pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数Kw=
①该温度下(t℃),将100mL0.1mol·L1的稀H2SO4溶液与100mL0.4mol·L1的NaOH溶液混合后(溶液体积变化忽略不计),溶液的pH=
②该温度下(t℃),1体积的稀硫酸和10体积的NaOH溶液混合后溶液呈中性,则稀硫酸的pH(pHa)与NaOH溶液的pH(pHb)的关系是:
您最近一年使用:0次
解题方法
3 . (1)25 ℃时,0.05mol·L-1H2SO4溶液的pH=_______ ,0.01 mol·L-1NaOH溶液的pH=_______ 。
(2)某温度下纯水中的c(H+)=2×10-7 mol·L-1,则此时溶液中的c(OH-)=_______ ;若温度不变,滴入稀盐酸,使c(H+)=5×10-4 mol·L-1,则此时溶液中由水电离产生的c(H+)=_______ 。
(2)某温度下纯水中的c(H+)=2×10-7 mol·L-1,则此时溶液中的c(OH-)=
您最近一年使用:0次
名校
4 . 在10L容器中,加入4mol的SO2(g)和4mol的NO2(g),保持温度恒定,发生反应:SO2(g)+NO2(g) SO3(g)+NO(g)。5分钟时达到平衡状态,测得容器中SO2(g)的转化率为50%。
SO3(g)+NO(g)。5分钟时达到平衡状态,测得容器中SO2(g)的转化率为50%。
(1)化学平衡时化学平衡常数___________ ,5分钟内NO2的反应速率为___________ ;
(2)当达到的平衡状态时,继续向容器中充入2mol的SO2(g)、1mol的NO2(g)、2molSO3(g)和2molNO(g),则v正___________ v逆(填“>”“<”或“=”)
(3)该温度下、该容器中,再继续加入2mol的SO2(g),则整个过程中,SO2的转化率由50%变为___________ %,NO2的转化率为___________ %
 SO3(g)+NO(g)。5分钟时达到平衡状态,测得容器中SO2(g)的转化率为50%。
SO3(g)+NO(g)。5分钟时达到平衡状态,测得容器中SO2(g)的转化率为50%。(1)化学平衡时化学平衡常数
(2)当达到的平衡状态时,继续向容器中充入2mol的SO2(g)、1mol的NO2(g)、2molSO3(g)和2molNO(g),则v正
(3)该温度下、该容器中,再继续加入2mol的SO2(g),则整个过程中,SO2的转化率由50%变为
您最近一年使用:0次
名校
解题方法
5 . I.将200mLH2SO4 和Fe2(SO4)3的混合溶液分成两等份。向其中一份中加入足量铁粉,充分反应后测的固体质量减少4.48g;向另一份中加入足量BaCl2溶液,经过滤、洗涤、干 燥、称量,得到46.6g 白色沉淀。则:
(1)原溶液中c( )=
)=_______ ;
(2)原溶液中H2SO4和Fe2(SO4)3的物质的量浓度之比为_______ 。
(3)实验室中的FeSO4溶液常因氧化而变质。除杂的方法是______________________ ,检验是否变质的方法是_______
II.准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4 g,则这种铁的氧化物为_______
(1)原溶液中c(
 )=
)=(2)原溶液中H2SO4和Fe2(SO4)3的物质的量浓度之比为
(3)实验室中的FeSO4溶液常因氧化而变质。除杂的方法是
II.准确称取某种铁的氧化物2.88 g,用足量的CO进行还原,将生成的CO2全部用足量的澄清石灰水吸收,得到沉淀4 g,则这种铁的氧化物为
您最近一年使用:0次
名校
解题方法
6 . 计算下列溶液的pH。
(1)常温下,pH=1的HCl与pH=4的H2SO4溶液等体积混合后,溶液的pH=___ 。
(2)常温下,将0.006mol•L-1的H2SO4与0.01mol•L-1的NaOH溶液等体积混合后,溶液的pH=___ 。
(3)常温下,pH=4的盐酸与pH=10的NaOH溶液以体积比11:9混合后,溶液的pH=___ 。
(1)常温下,pH=1的HCl与pH=4的H2SO4溶液等体积混合后,溶液的pH=
(2)常温下,将0.006mol•L-1的H2SO4与0.01mol•L-1的NaOH溶液等体积混合后,溶液的pH=
(3)常温下,pH=4的盐酸与pH=10的NaOH溶液以体积比11:9混合后,溶液的pH=
您最近一年使用:0次
名校
解题方法
7 . 在2 L的密闭容器中放入4 mol N2O5,发生如下反应:2N2O5(g) 4NO2(g)+O2(g)。反应至5 min时,测得N2O5转化了20%,则v(NO2)为
4NO2(g)+O2(g)。反应至5 min时,测得N2O5转化了20%,则v(NO2)为___ ;c(N2O5)为___ ;O2的物质的量浓度为___ 。
 4NO2(g)+O2(g)。反应至5 min时,测得N2O5转化了20%,则v(NO2)为
4NO2(g)+O2(g)。反应至5 min时,测得N2O5转化了20%,则v(NO2)为
您最近一年使用:0次
2021-01-05更新
|
190次组卷
|
2卷引用:安徽省桐城中学2020-2021学年高一上学期12月月考化学试题
名校
8 . 某研究性学习小组同学为了探究“在相同的温度和压强下、相同体积的任何气体都含有相同数目的分子”,他们设计了如下实验装置并记录相关实验数据。实验装置:

部分实验数据:
请回答下列问题:
(1)4分钟时H2物质的量是______ mol。
(2)该温度下,气体摩尔体积是________ 。
(3)假设电解H2O速率相同,2分钟时试管内收集到的H2的体积是________ mL。
(4)根据以上实验得出如下结论,其中不正确的是________ 。
A. 气体摩尔体积与气体的温度相关
B. 在该实验条件下,3 mol O2的气体摩尔体积为74.58 L/mol
C. 同温、同压下,2 mol O2和2 mol CO和CO2混合气体的体积相同
D. 该实验条件下,O2的密度为1.287 g/L

部分实验数据:
| 温度 | 压强 | 时间 | 水槽中H2O的质量 | H2体积 | O2体积 |
| 30℃ | 101 kPa | 0 | 300g | 0 | 0 |
| 30℃ | 101 kPa | 4分钟 | 298.2g | 1.243 L |
请回答下列问题:
(1)4分钟时H2物质的量是
(2)该温度下,气体摩尔体积是
(3)假设电解H2O速率相同,2分钟时试管内收集到的H2的体积是
(4)根据以上实验得出如下结论,其中不正确的是
A. 气体摩尔体积与气体的温度相关
B. 在该实验条件下,3 mol O2的气体摩尔体积为74.58 L/mol
C. 同温、同压下,2 mol O2和2 mol CO和CO2混合气体的体积相同
D. 该实验条件下,O2的密度为1.287 g/L
您最近一年使用:0次
9 . 向2 L密闭容器中通入a mol气体A和b mol气体B,在一定条件下发生反应:xA(g)+yB(g)=pC(g)+qD(g)
已知:平均反应速率vC= vA;反应2 min时,A的浓度减少了
vA;反应2 min时,A的浓度减少了 ,B的物质的量减少了
,B的物质的量减少了 mol,有a mol D生成。回答下列问题:
mol,有a mol D生成。回答下列问题:
(1)反应2 min内,vA=________ ,vB=________ ;
(2)化学方程式中,x=________ 、y=________ 、p=________ 、q=________ ;
已知:平均反应速率vC=
 vA;反应2 min时,A的浓度减少了
vA;反应2 min时,A的浓度减少了 ,B的物质的量减少了
,B的物质的量减少了 mol,有a mol D生成。回答下列问题:
mol,有a mol D生成。回答下列问题:(1)反应2 min内,vA=
(2)化学方程式中,x=
您最近一年使用:0次
2020-10-18更新
|
188次组卷
|
2卷引用:安徽省安庆市宜秀区白泽湖中学2020-2021学年高二上学期第一次月考化学试题
10 . (1)已知某温度时,KW=1.0×10-12 ,Na2CO3溶液的水解常数Kh=2.0×10-3,则当溶液中c(HCO )∶c(CO
)∶c(CO )=2∶1时,试求该溶液的pH=
)=2∶1时,试求该溶液的pH=______ 。
(2)已知25 ℃时,NH3·H2O的电离平衡常数Kb=1.8×10-5,该温度下1 mol·L-1的NH4Cl溶液中c(H+)=____________ mol·L-1。(已知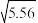 ≈2.36)
≈2.36)
(3)25 ℃时,H2SO3 HSO
HSO +H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=
+H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=________________ ,若向NaHSO3溶液中加入少量的I2,则溶液中 将
将________ (填“增大”“减小”或“不变”)。
(4)已知常温下CN-的水解常数Kh=1.61×10-5。
①常温下,含等物质的量浓度的HCN与NaCN的混合溶液显_____ (填“酸”“碱”或“中”)性,c(CN-)________ (填“>”“<”或“=”)c(HCN)。该溶液中各离子浓度由大到小的顺序为____________ 。
②常温下,若将c mol·L-1盐酸与0.62 mol·L-1KCN溶液等体积混合后恰好得到中性溶液,则c=________ (小数点后保留4位数字)。
 )∶c(CO
)∶c(CO )=2∶1时,试求该溶液的pH=
)=2∶1时,试求该溶液的pH=(2)已知25 ℃时,NH3·H2O的电离平衡常数Kb=1.8×10-5,该温度下1 mol·L-1的NH4Cl溶液中c(H+)=
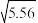 ≈2.36)
≈2.36)(3)25 ℃时,H2SO3
 HSO
HSO +H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=
+H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh= 将
将(4)已知常温下CN-的水解常数Kh=1.61×10-5。
①常温下,含等物质的量浓度的HCN与NaCN的混合溶液显
②常温下,若将c mol·L-1盐酸与0.62 mol·L-1KCN溶液等体积混合后恰好得到中性溶液,则c=
您最近一年使用:0次
2020-10-15更新
|
981次组卷
|
3卷引用:安徽省桐城中学2020-2021学年高二上学期12月月考化学试题
安徽省桐城中学2020-2021学年高二上学期12月月考化学试题安徽省阜阳市太和第一中学2020-2021学年高二上学期10月月考化学试题(已下线)全册综合检测(一)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)



