名校
解题方法
1 . 填空。
(1)CH4、CO2和碳酸都是碳的重要化合物,实现碳及其化合物的相互转化。对开发新能源和降低碳排放意义重大。
已知:①
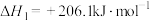
②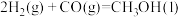
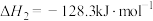
③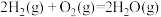
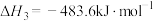
写出由甲烷和氧气合成液态甲醇的热化学方程式:_______ 。
(2)已知: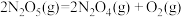
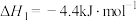
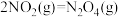
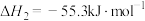
则反应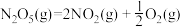 的△H=
的△H=_______ kJ∙mol-1。
(3)若将NaHSO4与Ba(OH)2在溶液中按物质的量之比为1:1混合,化学反应的离子方程式是_______ 。
(4)实验室现欲用质量分数为98%,密度为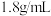 包的浓H2SO4溶液配制450 mL浓度为
包的浓H2SO4溶液配制450 mL浓度为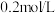 的稀H2SO4溶液,用量筒量取所需浓H2SO4溶液的体积是
的稀H2SO4溶液,用量筒量取所需浓H2SO4溶液的体积是_______ mL。
(1)CH4、CO2和碳酸都是碳的重要化合物,实现碳及其化合物的相互转化。对开发新能源和降低碳排放意义重大。
已知:①

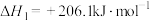
②
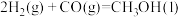
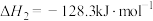
③
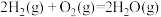
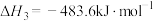
写出由甲烷和氧气合成液态甲醇的热化学方程式:
(2)已知:
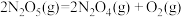
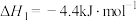
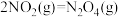
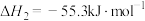
则反应
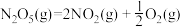 的△H=
的△H=(3)若将NaHSO4与Ba(OH)2在溶液中按物质的量之比为1:1混合,化学反应的离子方程式是
(4)实验室现欲用质量分数为98%,密度为
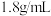 包的浓H2SO4溶液配制450 mL浓度为
包的浓H2SO4溶液配制450 mL浓度为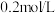 的稀H2SO4溶液,用量筒量取所需浓H2SO4溶液的体积是
的稀H2SO4溶液,用量筒量取所需浓H2SO4溶液的体积是
您最近一年使用:0次
解题方法
2 . 某抗酸药的有效成分为碳酸钙。取0.2克药片研碎后加入30 ml 某浓度稀盐酸,恰好完全反应,生成33.6 mL CO2气体(标准状况下)。(假设药片中其他成分不与盐酸反应)。计算:
(1)药片中CaCO3的质量分数_______ 。
(2)所加稀盐酸的物质的量浓度_______ 。
(1)药片中CaCO3的质量分数
(2)所加稀盐酸的物质的量浓度
您最近一年使用:0次
解题方法
3 . 36g H2O气体的物质的量是___________ ,分子个数是___________ ,氢原子的物质的量是___________ 。
您最近一年使用:0次
名校
解题方法
4 . 将64g铜与160mL一定浓度的硝酸反应,铜完全溶解产生的NO和NO2混合气体在标准状况下的体积为22.4L。请回答:
(1)在标准状况下,NO的体积为___________ L,NO2的体积为___________ L。
(2)参加反应的HNO3的物质的量是___________ 。
(1)在标准状况下,NO的体积为
(2)参加反应的HNO3的物质的量是
您最近一年使用:0次
解题方法
5 . 将等物质的量的A、B混合于2L的密闭容器中,发生反应3A(g)+B(g)⇌xC(g)+2D(g),经5s后,测得D的浓度为0.5mol/L,c(A):c(B)=3:5,v(C)为0.1mol/(L·s)
求:(1)x的值;___________
(2)以B表示的该反应的平均反应速率;___________
(3)此时A的浓度及反应开始前放入容器中的A、B的物质的量。___________
求:(1)x的值;
(2)以B表示的该反应的平均反应速率;
(3)此时A的浓度及反应开始前放入容器中的A、B的物质的量。
您最近一年使用:0次
解题方法
6 . 含0.6 mol NH 的(NH4)2CO3固体中,CO
的(NH4)2CO3固体中,CO 的质量是多少g?
的质量是多少g?
 的(NH4)2CO3固体中,CO
的(NH4)2CO3固体中,CO 的质量是多少g?
的质量是多少g?
您最近一年使用:0次
解题方法
7 . 将含有一定杂质的硅10g(杂质不与氢氧化钠反应)加入到足量的氢氧化钠溶液中,在标准状况下得到气体的体积为4.48L,求混合物中硅的质量分数?
您最近一年使用:0次
2014高三·全国·专题练习
名校
解题方法
8 . (1)北京奥运会祥云火炬将中国传统文化、奥运精神以及现代高科技融为一体。火炬内熊熊大火来源于丙烷的燃烧,丙烷是一种优良的燃料。试回答下列问题:
①如图是一定量丙烷完全燃烧生成CO2和1molH2O(l)过程中的能量变化图,请在图中的括号内填入“+”或“−”___ 。

②写出表示丙烷燃烧热的热化学方程式:___ 。
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1mol二甲醚完全燃烧生成CO2和液态水放出1455kJ热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为___ 。
(2)盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总热效应相同。试运用盖斯定律回答下列问题:
①已知:H2O(g)═H2O (l) △H1=−Q1kJ/mol
C2H5OH(g)═C2H5OH (l) △H2=−Q2kJ/mol
C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g) △H3=−Q3kJ/mol
若使23g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为___ kJ。
②碳(s)在氧气供应不充分时,生成CO同时还部分生成CO2,因此无法通过实验直接测得反应:C(s)+ O2(g)═CO(g)的△H.但可设计实验、利用盖斯定律计算出该反应的△H,计算时需要测得的实验数据有
O2(g)═CO(g)的△H.但可设计实验、利用盖斯定律计算出该反应的△H,计算时需要测得的实验数据有___ 。
①如图是一定量丙烷完全燃烧生成CO2和1molH2O(l)过程中的能量变化图,请在图中的括号内填入“+”或“−”

②写出表示丙烷燃烧热的热化学方程式:
③二甲醚(CH3OCH3)是一种新型燃料,应用前景广阔。1mol二甲醚完全燃烧生成CO2和液态水放出1455kJ热量。若1mol丙烷和二甲醚的混合气体完全燃烧生成CO2和液态水共放出1645kJ热量,则混合气体中,丙烷和二甲醚的物质的量之比为
(2)盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总热效应相同。试运用盖斯定律回答下列问题:
①已知:H2O(g)═H2O (l) △H1=−Q1kJ/mol
C2H5OH(g)═C2H5OH (l) △H2=−Q2kJ/mol
C2H5OH(g)+3O2(g)═2CO2(g)+3H2O(g) △H3=−Q3kJ/mol
若使23g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为
②碳(s)在氧气供应不充分时,生成CO同时还部分生成CO2,因此无法通过实验直接测得反应:C(s)+
 O2(g)═CO(g)的△H.但可设计实验、利用盖斯定律计算出该反应的△H,计算时需要测得的实验数据有
O2(g)═CO(g)的△H.但可设计实验、利用盖斯定律计算出该反应的△H,计算时需要测得的实验数据有
您最近一年使用:0次
2020-06-05更新
|
118次组卷
|
11卷引用:安徽省亳州市涡阳县第九中学2019-2020学年高一下学期期末考试化学试题
安徽省亳州市涡阳县第九中学2019-2020学年高一下学期期末考试化学试题(已下线)2014届高考化学二轮专题冲刺第5讲 化学反应与能量练习卷黑龙江省鹤岗第一中学2016-2017学年高一下学期期中考试化学试卷湖北省天门、仙桃、潜江三市2016-2017学年高一下学期期末考试化学试题【市级联考】内蒙古自治区鄂尔多斯市2018-2019学年高二上学期期中考试化学试题甘肃省张掖市临泽县第一中学2019-2020学年高二上学期9月月考化学试题甘肃省兰州大学附属中学(33中)2019-2020学年高二上学期期中考试化学试题河南省安阳市林州市第一中学2020-2021学年高二上学期开学考试(实验班)化学试题(已下线)1.3.2+反应热的计算-2020-2021学年高二化学同步课堂帮帮帮(人教版选修4)江西省赣州市南康中学2020-2021学年高二上学期第一次月考化学试题安徽省淮北市孙疃中学2020-2021学年高二上学期第一次月考化学(实验班)试题
名校
解题方法
9 . “信阳毛尖”是一种绿茶,绿茶中含有的单宁酸(化学式为C76XnO46)具有抑制血压上升、清热解毒等功效。回答下列问题:
(1)已知单宁酸完全燃烧时得到CO2、H2O,则X代表______ 元素,单宁酸的摩尔质量是1700g·L-1,则n=______ ,170g单宁酸完全燃烧时可得到______ gH2O。
(2)若170g单宁酸某次燃烧时生成了3.6molCO2,则生成的CO最多______ g,此种情况下恢复到常温,所得混合气体的平均摩尔质量为______ (保留1位小数)。
(1)已知单宁酸完全燃烧时得到CO2、H2O,则X代表
(2)若170g单宁酸某次燃烧时生成了3.6molCO2,则生成的CO最多
您最近一年使用:0次
名校
解题方法
10 . T1温度时在容积为2L的恒容密闭容器中只充入1.00molNO2气体发生反应:2NO(g)+O2(g) 2NO2(g) ∆H<0。实验测得:v正=k正c2(NO)·c(O2),v逆=k逆c2(NO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(NO2)如下表:
2NO2(g) ∆H<0。实验测得:v正=k正c2(NO)·c(O2),v逆=k逆c2(NO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(NO2)如下表:
(1)从0~2s该反应的平均速率v(NO2)=__ 。
(2)T1温度时化学平衡常数K=__ L·mol-1。
(3)化学平衡常数K与速率常数k正、k逆的数学关系是K=__ 。若将容器的温度改变为T2时其k正=k逆,则T2__ T1(填“>”、“<”或“=”)。
 2NO2(g) ∆H<0。实验测得:v正=k正c2(NO)·c(O2),v逆=k逆c2(NO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(NO2)如下表:
2NO2(g) ∆H<0。实验测得:v正=k正c2(NO)·c(O2),v逆=k逆c2(NO2),k正、k逆为速率常数只受温度影响。不同时刻测得容器中n(NO2)如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO2)/mol | 1.00 | 0.80 | 0.65 | 0.55 | 0.50 | 0.50 |
(1)从0~2s该反应的平均速率v(NO2)=
(2)T1温度时化学平衡常数K=
(3)化学平衡常数K与速率常数k正、k逆的数学关系是K=
您最近一年使用:0次



