名校
解题方法
1 . 某实验小组用氯酸钾和二氧化锰为原料制取氧气,在试管中加入少量二氧化锰和适量氯酸钾,反应过程中测量的有关数据记录如下:
(1)反应到___________ min时,氯酸钾就完全分解。
(2)计算反应前氯酸钾的质量是多少?__________ (写出解题步骤)
| 反应时间(min) | 0 | 1 | 2 | 3 | 4 |
| 试管中固体质量(g) | 14.25 | 12.65 | 11.05 | 9.45 | 9.45 |
(2)计算反应前氯酸钾的质量是多少?
您最近一年使用:0次
2 . 硫氧粉(Na2SO3)可用作染漂脱氧剂,常因氧化变质生成Na2SO4。向18.4 g可能被氧化的样品中,加入质量分数为10%的稀硫酸至恰好不再产生气泡(假设气体全部逸出),消耗稀硫酸98 g。
已知: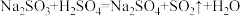 。
。
(1)三种钠盐:①Na2SO4、②Na2SO3、③Na2S2O3,其中含钠量由大到小的顺序是_______ (填序号)。
(2)求反应后溶液中溶质的质量分数(结果精确到0.1%)_______ 。(写出计算过程)
已知:
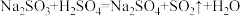 。
。(1)三种钠盐:①Na2SO4、②Na2SO3、③Na2S2O3,其中含钠量由大到小的顺序是
(2)求反应后溶液中溶质的质量分数(结果精确到0.1%)
您最近一年使用:0次
解题方法
3 . 质量、物质的量、气体摩尔体积等是用于化学计算的常见物理量,请完成下列计算:
(1)约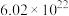 个
个 的物质的量是
的物质的量是___________ ;与___________ g  含有的氧原子数相等。
含有的氧原子数相等。
(2)42g 的体积(标准状况下)为
的体积(标准状况下)为___________ 。
(3)15.6g 中含有0.4mol
中含有0.4mol  ,则X的相对原子质量为
,则X的相对原子质量为___________ 。
(4)在相同温度和压强下,相同体积的氨气和硫化氢气体的质量之比为___________ ,其中含有的氢原子数目之比为___________ 。
(1)约
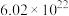 个
个 的物质的量是
的物质的量是 含有的氧原子数相等。
含有的氧原子数相等。(2)42g
 的体积(标准状况下)为
的体积(标准状况下)为(3)15.6g
 中含有0.4mol
中含有0.4mol  ,则X的相对原子质量为
,则X的相对原子质量为(4)在相同温度和压强下,相同体积的氨气和硫化氢气体的质量之比为
您最近一年使用:0次
解题方法
4 . 用 溶液滴定体积均为
溶液滴定体积均为 、浓度均为
、浓度均为 盐酸和醋酸溶液得到如图所示的滴定曲线:
盐酸和醋酸溶液得到如图所示的滴定曲线:
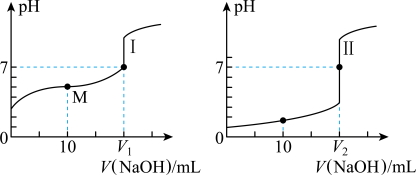
(1)用 溶液滴定醋酸溶液通常所选择的指示剂为
溶液滴定醋酸溶液通常所选择的指示剂为______ (选填“酚酞”、“甲基橙”或“石蕊”),符合其滴定曲线的是______ (选填“Ⅰ”或“Ⅱ”)。
(2) 盐酸中,由水电离出的
盐酸中,由水电离出的
______  。
。
(3)图中 和
和 大小的比较:
大小的比较:
______ (选填“<”或“=”或“>”) 。
。
(4)在 时,有
时,有 为
为 的盐酸和
的盐酸和 为
为 的
的 溶液,
溶液, 该盐酸恰好中和
该盐酸恰好中和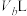 该
该 溶液。
溶液。
①若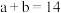 ,则
,则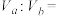
______ (填数字)。
②若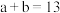 ,则
,则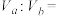
______ (填数字)。
 溶液滴定体积均为
溶液滴定体积均为 、浓度均为
、浓度均为 盐酸和醋酸溶液得到如图所示的滴定曲线:
盐酸和醋酸溶液得到如图所示的滴定曲线:
(1)用
 溶液滴定醋酸溶液通常所选择的指示剂为
溶液滴定醋酸溶液通常所选择的指示剂为(2)
 盐酸中,由水电离出的
盐酸中,由水电离出的
 。
。(3)图中
 和
和 大小的比较:
大小的比较:
 。
。(4)在
 时,有
时,有 为
为 的盐酸和
的盐酸和 为
为 的
的 溶液,
溶液, 该盐酸恰好中和
该盐酸恰好中和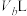 该
该 溶液。
溶液。①若
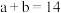 ,则
,则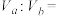
②若
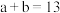 ,则
,则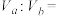
您最近一年使用:0次
5 . 正常体温下,人体动脉血液的 在
在 之间,之所以能够控制在该范围内,主要是因为血液中
之间,之所以能够控制在该范围内,主要是因为血液中 分子与
分子与 共存形成“缓冲溶液”[正常体温下
共存形成“缓冲溶液”[正常体温下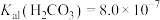 ,
,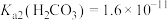 ],若血液
],若血液 超出正常范围,则可能导致酸中毒或碱中毒。
超出正常范围,则可能导致酸中毒或碱中毒。
(1)正常体温下,若某人动脉血 为
为 ,则属于
,则属于______ 中毒(选填“酸”或“碱”),他的血液中
______ 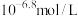 (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。
(2)已知: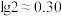 。正常体温下,某人动脉血液中
。正常体温下,某人动脉血液中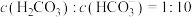 ,试通过计算判断属于酸中毒或碱中毒。
,试通过计算判断属于酸中毒或碱中毒。_____________________
 在
在 之间,之所以能够控制在该范围内,主要是因为血液中
之间,之所以能够控制在该范围内,主要是因为血液中 分子与
分子与 共存形成“缓冲溶液”[正常体温下
共存形成“缓冲溶液”[正常体温下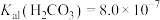 ,
,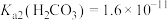 ],若血液
],若血液 超出正常范围,则可能导致酸中毒或碱中毒。
超出正常范围,则可能导致酸中毒或碱中毒。(1)正常体温下,若某人动脉血
 为
为 ,则属于
,则属于
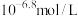 (选填“>”、“<”或“=”)。
(选填“>”、“<”或“=”)。(2)已知:
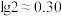 。正常体温下,某人动脉血液中
。正常体温下,某人动脉血液中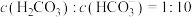 ,试通过计算判断属于酸中毒或碱中毒。
,试通过计算判断属于酸中毒或碱中毒。
您最近一年使用:0次
名校
6 . 250mL 2mol/L 的H2SO4 与足量铁屑完全反应。写出必要的计算过程。计算:
(1)参加反应的铁屑的物质的量_____ 。
(2)生成的H2在标准状况下的体积_____ 。
(1)参加反应的铁屑的物质的量
(2)生成的H2在标准状况下的体积
您最近一年使用:0次
2024-01-28更新
|
95次组卷
|
2卷引用:四川省成都市成华区某校2023-2024学年高一上学期12月月考化学试题
名校
7 . 向100mL含 、
、 、HCl的溶液中滴加一定浓度的NaOH溶液至过量,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。
、HCl的溶液中滴加一定浓度的NaOH溶液至过量,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。___________ ;
(2)依据表格中信息,计算滴加氢氧化钠溶液的物质的量浓度为___________ :(保留一位小数)
(3)原溶液中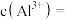
___________ ,
___________ ;
(4)将最终生成的沉淀过滤、洗涤、干燥后,放入坩埚中灼烧,得到的固体质量为4.9克。若灼烧后的固体为 ,则x的值为多少?
,则x的值为多少?___________ (无计算过程不给分)。
 、
、 、HCl的溶液中滴加一定浓度的NaOH溶液至过量,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。
、HCl的溶液中滴加一定浓度的NaOH溶液至过量,生成沉淀的质量与所加NaOH溶液的体积关系如图所示。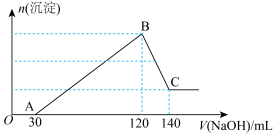
(2)依据表格中信息,计算滴加氢氧化钠溶液的物质的量浓度为
| 分子式:NaOH 相对分子质量:40 密度:  NaOH的质量分数:16.7% |
(3)原溶液中
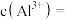

(4)将最终生成的沉淀过滤、洗涤、干燥后,放入坩埚中灼烧,得到的固体质量为4.9克。若灼烧后的固体为
 ,则x的值为多少?
,则x的值为多少?
您最近一年使用:0次
名校
解题方法
8 . Fe和 的混合物38.4g,加入
的混合物38.4g,加入 的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色。
的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色。
(1)发生反应的离子方程式有:___________ 。
(2)所得溶液中 的物质的量浓度为
的物质的量浓度为___________  (假设反应后溶液体积仍为200mL)。
(假设反应后溶液体积仍为200mL)。
(3) 的质量为多少克?
的质量为多少克?___________ (列出计算过程,此问无过程就无分)
(4)收集到气体在标准状况下的体积为___________ L。
 的混合物38.4g,加入
的混合物38.4g,加入 的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色。
的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色。(1)发生反应的离子方程式有:
(2)所得溶液中
 的物质的量浓度为
的物质的量浓度为 (假设反应后溶液体积仍为200mL)。
(假设反应后溶液体积仍为200mL)。(3)
 的质量为多少克?
的质量为多少克?(4)收集到气体在标准状况下的体积为
您最近一年使用:0次
9 . 把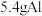 放入
放入 足量氢氧化钠溶液中完全反应,忽略溶液体积变化,试计算:
足量氢氧化钠溶液中完全反应,忽略溶液体积变化,试计算:
(1)生成氢气在标准状况下的体积______________ 。
(2)反应后溶液中四羟基合铝酸钠的物质的量浓度______________ 。
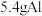 放入
放入 足量氢氧化钠溶液中完全反应,忽略溶液体积变化,试计算:
足量氢氧化钠溶液中完全反应,忽略溶液体积变化,试计算:(1)生成氢气在标准状况下的体积
(2)反应后溶液中四羟基合铝酸钠的物质的量浓度
您最近一年使用:0次
名校
10 . 研究钠及其化合物的性质有重要的意义。
(1)金属钠非常活泼,通常保存在___________ 中,以隔绝空气。
(2)汽车安全气囊内装有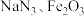 和
和 等物质。
等物质。
①当汽车发生严重碰撞时,引发 分解:
分解: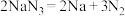 ,
, 中存在的化学键为
中存在的化学键为___________ ;若安全气囊内有 ,其完全分解所释放的
,其完全分解所释放的 在标准状况下的体积为
在标准状况下的体积为___________ L。
②产生的Na立即与 发生置换反应生成
发生置换反应生成 ,其中还原产物是
,其中还原产物是___________ 。
(3)某同学向 和
和 的混合液中逐滴加入一定浓度的盐酸,生成CO2的体积(标准状况)与加入盐酸的体积的关系如图所示。
的混合液中逐滴加入一定浓度的盐酸,生成CO2的体积(标准状况)与加入盐酸的体积的关系如图所示。
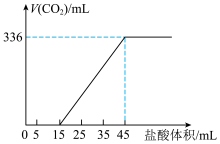
①混合液中
___________ 。
②盐酸的物质的量浓度为___________ 。
(1)金属钠非常活泼,通常保存在
(2)汽车安全气囊内装有
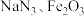 和
和 等物质。
等物质。①当汽车发生严重碰撞时,引发
 分解:
分解: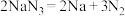 ,
, 中存在的化学键为
中存在的化学键为 ,其完全分解所释放的
,其完全分解所释放的 在标准状况下的体积为
在标准状况下的体积为②产生的Na立即与
 发生置换反应生成
发生置换反应生成 ,其中还原产物是
,其中还原产物是(3)某同学向
 和
和 的混合液中逐滴加入一定浓度的盐酸,生成CO2的体积(标准状况)与加入盐酸的体积的关系如图所示。
的混合液中逐滴加入一定浓度的盐酸,生成CO2的体积(标准状况)与加入盐酸的体积的关系如图所示。
①混合液中

②盐酸的物质的量浓度为
您最近一年使用:0次



