1 . 下列实验现象描述正确的是
| A.碘水中加入少量裂化汽油振荡,静置后上层颜色变浅,下层颜色变为紫红色 |
| B.红热的铜丝在氯气中燃烧,产生了棕黄色的雾 |
| C.电解氯化钠饱和溶液,将阳极气体产物通入碘化钾淀粉溶液中,溶液变蓝 |
| D.溴化钠溶液中加入少量新制的氯水振荡,再加入少量四氯化碳溶液振荡,静置后上层颜色变浅,下层颜色变为橙红色 |
您最近一年使用:0次
2 . 根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计与结论都正确的是
| 实验目的 | 方案设计 | 现象 | 结论 | |
| A | 检验固体样品中是否含有 | 将固体样品加水溶解,滴入浓NaOH溶液并加热,试管口放一张湿润的红色石蕊试纸 | 湿润的红色石蕊试纸变蓝色 | 样品中含有 |
| B | 探究铝与浓硫酸的钝化现象 | 常温下,将铝片直接放入浓硫酸中,一段时间后取出并用水洗净,放入 溶液 溶液 | 铝片表面未见紫红色固体生成 | 室温下浓硫酸能将铝片钝化 |
| C | 探究Si、Cl元素的非金属性的强弱 | 向 溶液中滴加1滴酚酞,然后逐滴加入盐酸至红色褪去 溶液中滴加1滴酚酞,然后逐滴加入盐酸至红色褪去 | 混合液逐渐变成白色凝胶 | 非金属性:Si<Cl |
| D | 探究 的化学性质 的化学性质 | 将镁条引燃后,迅速伸入集满 的集气瓶 的集气瓶 | 镁条剧烈燃烧,产生大量白烟,瓶口有淡黄色颗粒 |  具有氧化性 具有氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
3 . 已知配合物中心M与配体L之间存在平衡关系: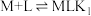 ,
,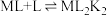 ,
,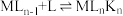 。
。 与
与 具有很强的亲和性,当
具有很强的亲和性,当 的浓度过大时,还会形成
的浓度过大时,还会形成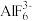 。常温下向某浓度的
。常温下向某浓度的 溶液中加入
溶液中加入 ,实验测定
,实验测定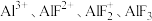 在所有含铝元素微粒中的百分含量随
在所有含铝元素微粒中的百分含量随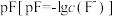 的变化如图所示,下列说法正确的是
的变化如图所示,下列说法正确的是
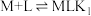 ,
,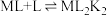 ,
,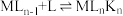 。
。 与
与 具有很强的亲和性,当
具有很强的亲和性,当 的浓度过大时,还会形成
的浓度过大时,还会形成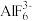 。常温下向某浓度的
。常温下向某浓度的 溶液中加入
溶液中加入 ,实验测定
,实验测定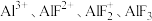 在所有含铝元素微粒中的百分含量随
在所有含铝元素微粒中的百分含量随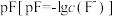 的变化如图所示,下列说法正确的是
的变化如图所示,下列说法正确的是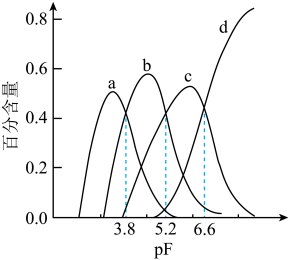
A.曲线d表示 的变化情况 的变化情况 |
B.反应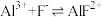 的平衡常数数量级为 的平衡常数数量级为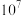 |
C. 时, 时,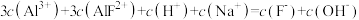 |
D.溶液中可能存在 |
您最近一年使用:0次
4 . 以钢铁厂锌灰(主要成分为 ,含少量的
,含少量的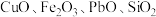 等)为原料制备高纯氧化锌的工艺流程如下:
等)为原料制备高纯氧化锌的工艺流程如下:
 ,含少量的
,含少量的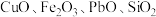 等)为原料制备高纯氧化锌的工艺流程如下:
等)为原料制备高纯氧化锌的工艺流程如下: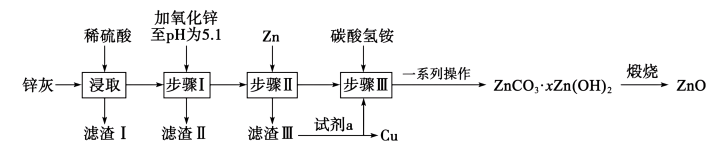
A.滤渣I的主要成分是 |
| B.加入试剂a的目的是提取铜中的锌 |
C.氢氧化铁的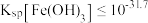 |
D.若取步骤III后的固体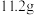 煅烧,得到产品 煅烧,得到产品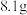 ,则 ,则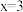 |
您最近一年使用:0次
解题方法
5 . 一定电压条件下,NiCo-LDHs电极材料上5-羟甲基-2-呋喃甲醛(HMF)可能的物质转化过程如图1所示,各物质含量的动态变化如图2所示。下列说法错误的是
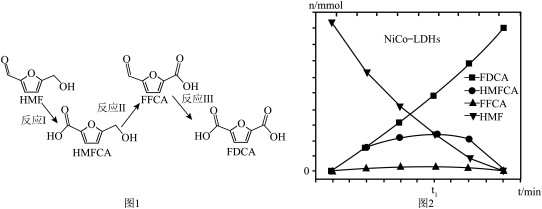
| A.NiCo-LDHs电极连接外接电源的正极 |
B.NiCo-LDHs电极上发生反应: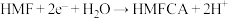 |
| C.基元反应Ⅲ活化能最小 |
| D.FFCA的沸点比FDCA低的主要原因是FDCA的相对分子质量大 |
您最近一年使用:0次
解题方法
6 . 常温下 水溶液体系中存在反应:
水溶液体系中存在反应: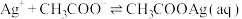 ,平衡常数为
,平衡常数为 。已知初始浓度
。已知初始浓度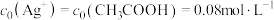 ,所有含碳物种的摩尔分数与pH变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
,所有含碳物种的摩尔分数与pH变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
 水溶液体系中存在反应:
水溶液体系中存在反应: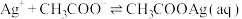 ,平衡常数为
,平衡常数为 。已知初始浓度
。已知初始浓度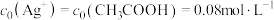 ,所有含碳物种的摩尔分数与pH变化关系如图所示(忽略溶液体积变化)。下列说法正确的是
,所有含碳物种的摩尔分数与pH变化关系如图所示(忽略溶液体积变化)。下列说法正确的是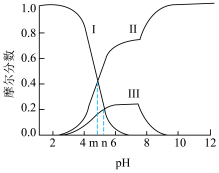
A.曲线Ⅱ表示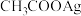 的变化情况 的变化情况 |
B. 的电离平衡常数 的电离平衡常数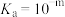 |
C.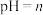 时, 时,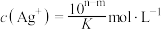 |
D. 时, 时,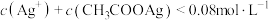 |
您最近一年使用:0次
解题方法
7 . 逆水气变换反应: 。一定压力下,按
。一定压力下,按 、
、 物质的量之比
物质的量之比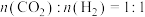 投料,
投料, 、
、 温度时反应物摩尔分数随时间变化关系如图所示。已知该反应的速率方程为
温度时反应物摩尔分数随时间变化关系如图所示。已知该反应的速率方程为 ,
, 、
、 温度时反应速率常数
温度时反应速率常数 分别为
分别为 、
、 。下列说法正确的是
。下列说法正确的是
 。一定压力下,按
。一定压力下,按 、
、 物质的量之比
物质的量之比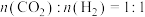 投料,
投料, 、
、 温度时反应物摩尔分数随时间变化关系如图所示。已知该反应的速率方程为
温度时反应物摩尔分数随时间变化关系如图所示。已知该反应的速率方程为 ,
, 、
、 温度时反应速率常数
温度时反应速率常数 分别为
分别为 、
、 。下列说法正确的是
。下列说法正确的是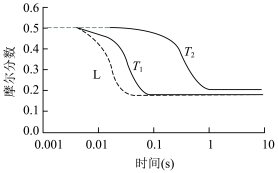
A. |
B.逆水煤气变换反应 |
C. 温度下,仅增大体系初始压力,反应物摩尔分数随时间的变化曲线可能为L 温度下,仅增大体系初始压力,反应物摩尔分数随时间的变化曲线可能为L |
D. 温度下,改变初始投料比例,可使平衡时各组分摩尔分数与 温度下,改变初始投料比例,可使平衡时各组分摩尔分数与 温度时相同 温度时相同 |
您最近一年使用:0次
8 . 298K时,向 溶液中滴加
溶液中滴加 溶液,滴定曲线如图所示。下列说法不正确的是
溶液,滴定曲线如图所示。下列说法不正确的是
 溶液中滴加
溶液中滴加 溶液,滴定曲线如图所示。下列说法不正确的是
溶液,滴定曲线如图所示。下列说法不正确的是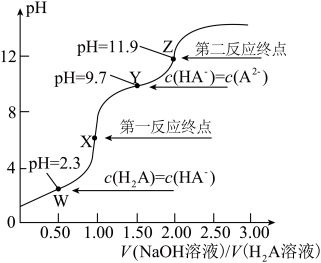
| A.该滴定过程应该选择酚酞溶液作指示剂 |
B.W点到X点发生的主要反应的离子方程式为 |
C.Y点对应的溶液中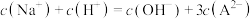 |
D.反应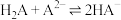 的平衡常数 的平衡常数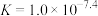 |
您最近一年使用:0次
9 . 蔗糖遇浓硫酸会变成“黑面包”状,下列说法正确的是
| A.蔗糖属于多糖 |
| B.在水浴条件下,蔗糖能与银氨溶液反应产生“银镜” |
| C.浓硫酸表现出脱水性、氧化性 |
| D.产生的气体通入品红溶液,溶液会褪色 |
您最近一年使用:0次
解题方法
10 . 关于SO2的说法正确的是
| A.中心原子的杂化类型为sp2 | B.电负性:O<S |
| C.属于非极性分子 | D.价层电子对的空间结构为平面三角形 |
您最近一年使用:0次



