名校
1 . A、B、C、D、E为中学化学常见物质,它们按如图所示关系相互转化,已知A为金属单质,C的焰色呈黄色。
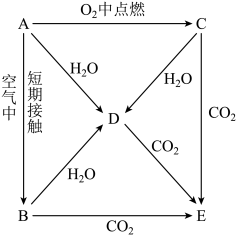
(1)写出下列物质的化学式:C_________ ,D__________ ,E________ 。
(2)写出C→D的离子方程式:___________ 。
(3)将盐酸逐滴滴入E的溶液中至过量的实验现象是___________ 。
(4)D与过量的CO2反应的离子方程式:___________ 。
(5)C与CO2反应被氧化的物质是___________ ,当生成2.24L(标准状况)O2转移的电子数目为___________ 。

(1)写出下列物质的化学式:C
(2)写出C→D的离子方程式:
(3)将盐酸逐滴滴入E的溶液中至过量的实验现象是
(4)D与过量的CO2反应的离子方程式:
(5)C与CO2反应被氧化的物质是
您最近一年使用:0次
名校
解题方法
2 . 工业上以 和
和 为原料可制备合成气(CO、
为原料可制备合成气(CO、 ),该反应的化学方程式为
),该反应的化学方程式为 。回答下列问题:
。回答下列问题:
(1)已知: 、
、 、CO的燃烧热分别为
、CO的燃烧热分别为 ,
, ,
, ,则
,则 的
的
_______ 。
(2)在1L恒温恒容密闭容器中充入 和
和 发生上述反应。900℃,反应达到平衡时混合体系中甲烷体积分数为10%,此时压强为2MPa,则平衡常数
发生上述反应。900℃,反应达到平衡时混合体系中甲烷体积分数为10%,此时压强为2MPa,则平衡常数
_______  (用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
(3)已知在高温条件下,会发生如下副反应:
 ,且温度越高副反应的转化率越高。投料比
,且温度越高副反应的转化率越高。投料比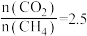 时温度变化对平衡时
时温度变化对平衡时 配比的影响如图所示。
配比的影响如图所示。
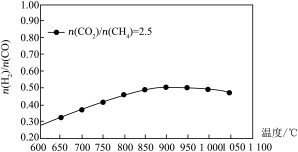
按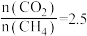 的配比进料,900℃以后,随温度升高,合成气
的配比进料,900℃以后,随温度升高,合成气 配比的变化规律是
配比的变化规律是_______ ;其原因可能是_______ 。
(4)工业上常利用生成的合成气制备甲醇( ),将CO和
),将CO和 通入某密闭容器中,只发生反应
通入某密闭容器中,只发生反应 ,有甲、乙两容器,甲容器容积固定。一定温度下,在甲容器中通入1mol CO、
,有甲、乙两容器,甲容器容积固定。一定温度下,在甲容器中通入1mol CO、 ,达到平衡时生成
,达到平衡时生成 。相同温度下,在乙容器中通入2mol CO、
。相同温度下,在乙容器中通入2mol CO、 ,若乙的压强始终与甲的压强相等,乙中反应达到平衡时,生成
,若乙的压强始终与甲的压强相等,乙中反应达到平衡时,生成 的物质的量为
的物质的量为_______ ;若乙的容积与甲的容积相等,乙中反应达到平衡时,生成 的物质的量
的物质的量_______ (填“大于”“小于”或“等于”) 。
。
 和
和 为原料可制备合成气(CO、
为原料可制备合成气(CO、 ),该反应的化学方程式为
),该反应的化学方程式为 。回答下列问题:
。回答下列问题:(1)已知:
 、
、 、CO的燃烧热分别为
、CO的燃烧热分别为 ,
, ,
, ,则
,则 的
的
(2)在1L恒温恒容密闭容器中充入
 和
和 发生上述反应。900℃,反应达到平衡时混合体系中甲烷体积分数为10%,此时压强为2MPa,则平衡常数
发生上述反应。900℃,反应达到平衡时混合体系中甲烷体积分数为10%,此时压强为2MPa,则平衡常数
 (用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度,分压=总压×物质的量分数)。(3)已知在高温条件下,会发生如下副反应:

 ,且温度越高副反应的转化率越高。投料比
,且温度越高副反应的转化率越高。投料比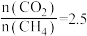 时温度变化对平衡时
时温度变化对平衡时 配比的影响如图所示。
配比的影响如图所示。
按
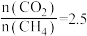 的配比进料,900℃以后,随温度升高,合成气
的配比进料,900℃以后,随温度升高,合成气 配比的变化规律是
配比的变化规律是(4)工业上常利用生成的合成气制备甲醇(
 ),将CO和
),将CO和 通入某密闭容器中,只发生反应
通入某密闭容器中,只发生反应 ,有甲、乙两容器,甲容器容积固定。一定温度下,在甲容器中通入1mol CO、
,有甲、乙两容器,甲容器容积固定。一定温度下,在甲容器中通入1mol CO、 ,达到平衡时生成
,达到平衡时生成 。相同温度下,在乙容器中通入2mol CO、
。相同温度下,在乙容器中通入2mol CO、 ,若乙的压强始终与甲的压强相等,乙中反应达到平衡时,生成
,若乙的压强始终与甲的压强相等,乙中反应达到平衡时,生成 的物质的量为
的物质的量为 的物质的量
的物质的量 。
。
您最近一年使用:0次
3 . 联氨(又称肼,N2H4,无色液体)是一种应用广泛的化工原料,回答下列问题:
I、
(1)联氨的结构式为___________ 。
(2)火箭发射时可以用联氨作燃料,NO2作氧化剂,二者反应生成N2和水蒸气。已知:
①2O2(g)+N2(g)=2NO2(g) △H1=+66.4kJ/mol
②N2H4(l)+O2(g)=N2(g)+2H2O(l) △H2=-622.0kJ/mol
③H2O(l)=H2O(g) △H3=+44.0kJ/mol
请写出N2H4(l)与NO2(g)反应的热化学方程式___________ 。
II、肼(N2H4)─空气燃料电池是一种理想的电池,具有容量大、能量转化率高、产物无污染等特点,某学习小组利用该电池来探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。
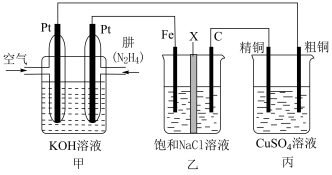
(3)乙装置中石墨电极为___________ 极(填“正”或“负”、“阴”或“阳”),Fe电极反应式为___________ 。
(4)丙装置模拟工业中的粗铜精炼原理,电解后精铜质量增加3.2g,则理论上甲装置中肼消耗质量为___________ g。
(5)如果将丙中的粗铜电极换为Pt电极,该溶液中pH___________ (填“变大”“变小”“不变”),电解一段时间后溶液蓝色变浅,但并未消失,要想把此时的溶液恢复至原状态,需加入适量的___________ (填化学式)。
I、
(1)联氨的结构式为
(2)火箭发射时可以用联氨作燃料,NO2作氧化剂,二者反应生成N2和水蒸气。已知:
①2O2(g)+N2(g)=2NO2(g) △H1=+66.4kJ/mol
②N2H4(l)+O2(g)=N2(g)+2H2O(l) △H2=-622.0kJ/mol
③H2O(l)=H2O(g) △H3=+44.0kJ/mol
请写出N2H4(l)与NO2(g)反应的热化学方程式
II、肼(N2H4)─空气燃料电池是一种理想的电池,具有容量大、能量转化率高、产物无污染等特点,某学习小组利用该电池来探究某些工业原理,其中乙装置中X为阳离子交换膜(即只允许阳离子通过)。

(3)乙装置中石墨电极为
(4)丙装置模拟工业中的粗铜精炼原理,电解后精铜质量增加3.2g,则理论上甲装置中肼消耗质量为
(5)如果将丙中的粗铜电极换为Pt电极,该溶液中pH
您最近一年使用:0次
4 . 某研究小组欲从含少量 、
、 、
、 、
、 的
的 溶液中制纯净的无水
溶液中制纯净的无水 固体,设计的流程如下:
固体,设计的流程如下:

常温下,几种金属离子沉淀完全(离子浓度小于 )时的
)时的 如表所示:
如表所示:
回答下列问题:
(1)实验室用 配制
配制 溶液的方法是
溶液的方法是___________
(2)加入 ,发生反应的离子方程式为
,发生反应的离子方程式为___________ ;“过滤2”得到的沉淀是___________ (填化学式)。
(3)常温时,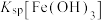 、
、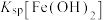 、
、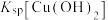 、
、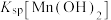 中数值最大的为
中数值最大的为___________ ;第一次“调pH”的最小值为___________ ,第二次“调pH”的最小值为___________ 。已知常温下, 的
的 ,
, 的氨水的pH=
的氨水的pH=___________ (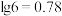 )。
)。
(4)“一系列操作”包括___________ 、洗涤、干燥;由 制无水
制无水 的操作是
的操作是___________ 。
 、
、 、
、 、
、 的
的 溶液中制纯净的无水
溶液中制纯净的无水 固体,设计的流程如下:
固体,设计的流程如下:
常温下,几种金属离子沉淀完全(离子浓度小于
 )时的
)时的 如表所示:
如表所示:| 金属离子 |  |  |  |  |
沉淀完全时的 | 2.8 | 8.3 | 10.1 | 6.7 |
(1)实验室用
 配制
配制 溶液的方法是
溶液的方法是(2)加入
 ,发生反应的离子方程式为
,发生反应的离子方程式为(3)常温时,
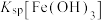 、
、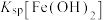 、
、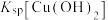 、
、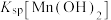 中数值最大的为
中数值最大的为 的
的 ,
, 的氨水的pH=
的氨水的pH=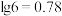 )。
)。(4)“一系列操作”包括
 制无水
制无水 的操作是
的操作是
您最近一年使用:0次
解题方法
5 . 现代生活离不开化学电源,各种各样的化学电源都是依据原电池的原理制造的,学会设计原电池有重要的意义。请回答下列问题:

I.某化学兴趣小组根据反应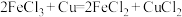 设计原电池,装置如图所示。
设计原电池,装置如图所示。
(1)负极的电极材料为___________ ,正极的电极材料可采用___________ 。
(2)X溶液为___________ ,电池工作时, 向
向___________ (填“正极”或“负极”)移动。
II.燃料电池能抵转换效率高、对环境污染小,是一种很有前途的能源利用方式。根据反应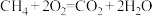 设计的甲烷燃料电池如图所示。
设计的甲烷燃料电池如图所示。

(3)M极为___________ (填“正极”或“负极”),应通入的气体为___________ ,该电极发生的电极反应为___________ 。
(4)该电池工作一段时间后,溶液的
___________ (填“增大”、“减小”或“不变”),当消耗 (标准状况下)
(标准状况下) 时,电路中转移了
时,电路中转移了___________  。
。

I.某化学兴趣小组根据反应
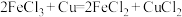 设计原电池,装置如图所示。
设计原电池,装置如图所示。(1)负极的电极材料为
(2)X溶液为
 向
向II.燃料电池能抵转换效率高、对环境污染小,是一种很有前途的能源利用方式。根据反应
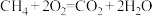 设计的甲烷燃料电池如图所示。
设计的甲烷燃料电池如图所示。
(3)M极为
(4)该电池工作一段时间后,溶液的

 (标准状况下)
(标准状况下) 时,电路中转移了
时,电路中转移了 。
。
您最近一年使用:0次
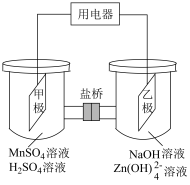
6 . 水系 电池是一种具有较高工作电压和能量密度的储能电池,其工作原理如图所示(甲极附有
电池是一种具有较高工作电压和能量密度的储能电池,其工作原理如图所示(甲极附有 ,乙极为锌片,盐桥中含有可自由移动的
,乙极为锌片,盐桥中含有可自由移动的 、
、 ),下列说法正确的是
),下列说法正确的是
 电池是一种具有较高工作电压和能量密度的储能电池,其工作原理如图所示(甲极附有
电池是一种具有较高工作电压和能量密度的储能电池,其工作原理如图所示(甲极附有 ,乙极为锌片,盐桥中含有可自由移动的
,乙极为锌片,盐桥中含有可自由移动的 、
、 ),下列说法正确的是
),下列说法正确的是
| A.甲极为正极,发生氧化反应 |
B.乙极上发生的电极反应为 |
C.工作一段时间后,左侧电解液的 减小 减小 |
D.该电池工作时,盐桥中的 向甲极方向移动 向甲极方向移动 |
您最近一年使用:0次
7 . 在25℃时,不同浓度的一元酸HA、HB和HC溶液的pH如表所示,下列说法正确的是
浓度 | HA | HB | HC |
| 0.1000 | 2.9 | 4.2 | 1.0 |
| 0.0100 | 3.4 | 4.7 | 2.0 |
| 0.0010 | 3.9 | 5.2 | 3.0 |
A.酸性: |
B.25℃时, |
C.可以发生反应: |
| D.25℃时,向10mLHB溶液中加入5mL等浓度的NaOH溶液后,溶液呈酸性 |
您最近一年使用:0次
解题方法
8 . 下列说法正确的是
| A.铅酸蓄电池放电工作一段时间后,负极质量减小,正极质量增大 |
B.由 、 、 、 、 溶液组成的原电池,其负极发生的电极反应为 溶液组成的原电池,其负极发生的电极反应为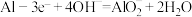 |
| C.锂离子电池具有质量小、储存能量大等优点,以水溶液为电解质溶液时的放电效率高 |
D.反应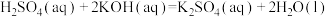  在理论上可以设计为原电池 在理论上可以设计为原电池 |
您最近一年使用:0次
9 . 下列说法正确的是
| A.构成原电池的正极和负极必须是两种不同的金属 |
| B.将铜片插入三氯化铁溶液中,铜片表面会生成一层铁 |
| C.工业上常采用电解KOH溶液制备单质钾 |
| D.钢铁在水膜酸度较高的特殊环境中发生的电化学腐蚀,称为析氢腐蚀 |
您最近一年使用:0次
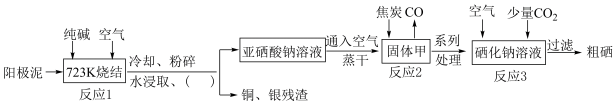
10 . 硒元素是人和动物的抗氧化酶,在体内起到平衡氧化还原作用,可以提高免疫力。同时硒是人体必需的微量元素,具有极大的作用。某化学科研小组以精炼铜的阳极泥为主要原料(主要成分是Se,含有CuSe、Ag2Se等杂质),提炼粗硒的工艺流程如下:
请回答下列问题:
(1)把阳极泥烧结后进行粉碎的目的是___________ ;上述流程图中的括号内的操作方法是___________ ,该操作在实验室中所使用的玻璃仪器有___________ 。
(2)亚硒酸钠溶液中滴入几滴酚酞,溶液显___________ 色,原因是___________ (用离子方程式表示)。
(3)写出反应2的化学方程式___________ 。
(4)写出反应3的离子方程式___________ 。
(5)工艺流程中可以循环使用的物质是___________ (填化学式)。

请回答下列问题:
(1)把阳极泥烧结后进行粉碎的目的是
(2)亚硒酸钠溶液中滴入几滴酚酞,溶液显
(3)写出反应2的化学方程式
(4)写出反应3的离子方程式
(5)工艺流程中可以循环使用的物质是
您最近一年使用:0次



