1 . 已知植物光合作用发生的反应如下: ,
,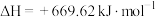 该反应达到化学平衡后,下列说法正确的是
该反应达到化学平衡后,下列说法正确的是
 ,
,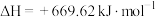 该反应达到化学平衡后,下列说法正确的是
该反应达到化学平衡后,下列说法正确的是A.取走一半 , , 转化率增大 转化率增大 |
B.适当升高温度,既提高了反应速率,又增大了 的转化率增大 的转化率增大 |
C.加入催化剂, 的体积分数增大 的体积分数增大 |
D.增大 的浓度,平衡右移,化学平衡常数增大 的浓度,平衡右移,化学平衡常数增大 |
您最近一年使用:0次
解题方法
2 . 下列说法正确的是
A.已知 ,该反应为熵减小的反应 ,该反应为熵减小的反应 |
| B.氢氧化钠固体溶于水体系温度升高,是因为发生了放热反应 |
| C.甲烷燃烧放热,是因为破坏反应物化学键所需的能量特别大 |
D.已知乙醚的摩尔燃烧焓为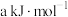 ,则表示乙醚摩尔燃烧焓的热化学方程式为: ,则表示乙醚摩尔燃烧焓的热化学方程式为: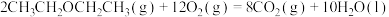 , , |
您最近一年使用:0次
名校
3 . Ⅰ.已知下列热化学方程式:
①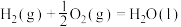
 ;
;
②
 ;
;
③
 ;
;
④
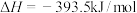 。
。
回答下列问题:
(1)碳的燃烧热的热化学方程式为___________ (填序号)。
(2)燃烧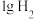 生成气态水,放出的热量为
生成气态水,放出的热量为___________ 。
II.已知强酸稀溶液与强碱稀溶液发生中和反应的热化学方程式为:
 。
。
(3)若稀硫酸与氢氧化钠固体反应生成 ,则反应放出的热量
,则反应放出的热量___________ (填“大于”、“等于”或“小于”) ,原因是
,原因是___________ 。
Ⅲ.氮及其化合物与人类生产、生活密切相关。氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。
(4)已知:



若用CO还原 至
至 ,当消耗标准状况下
,当消耗标准状况下 时,放出的热量为
时,放出的热量为___________ kJ(用含有a和b的代数式表示)。
Ⅳ.请回答:
(5)CO、 可用于合成甲醇和甲醚,其反应为(m、n均大于0):
可用于合成甲醇和甲醚,其反应为(m、n均大于0):
反应①:

反应②:

反应③:

则m与n的关系为___________ 。
(6)已知 和
和 反应时放热,且断裂
反应时放热,且断裂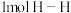 键、
键、 键、
键、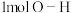 键需要吸收的能量分别为
键需要吸收的能量分别为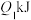 、
、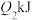 、
、 。下列关系一定正确的是___________。
。下列关系一定正确的是___________。
①
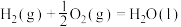
 ;
;②

 ;
;③

 ;
;④

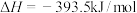 。
。回答下列问题:
(1)碳的燃烧热的热化学方程式为
(2)燃烧
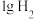 生成气态水,放出的热量为
生成气态水,放出的热量为II.已知强酸稀溶液与强碱稀溶液发生中和反应的热化学方程式为:

 。
。(3)若稀硫酸与氢氧化钠固体反应生成
 ,则反应放出的热量
,则反应放出的热量 ,原因是
,原因是Ⅲ.氮及其化合物与人类生产、生活密切相关。氮氧化物是造成光化学烟雾和臭氧层损耗的主要气体。
(4)已知:




若用CO还原
 至
至 ,当消耗标准状况下
,当消耗标准状况下 时,放出的热量为
时,放出的热量为Ⅳ.请回答:
(5)CO、
 可用于合成甲醇和甲醚,其反应为(m、n均大于0):
可用于合成甲醇和甲醚,其反应为(m、n均大于0):反应①:


反应②:


反应③:


则m与n的关系为
(6)已知
 和
和 反应时放热,且断裂
反应时放热,且断裂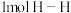 键、
键、 键、
键、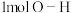 键需要吸收的能量分别为
键需要吸收的能量分别为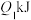 、
、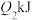 、
、 。下列关系一定正确的是___________。
。下列关系一定正确的是___________。A.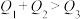 | B.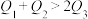 |
C.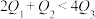 | D. |
您最近一年使用:0次
2023-10-02更新
|
108次组卷
|
2卷引用:安徽省马鞍山市第二中学2022-2023学年高二上学期11月期中考试化学试题
名校
解题方法
4 . 氮元素是构成生命体必不可少的元素,对人类生命和生活具有重要意义。
(1)氨的人工合成使大幅度增加粮食产量的愿望变成了现实。
已知:①
②
③
则 的燃烧热
的燃烧热
___________  (填“<”“>”或“=”),写出工业合成氨的热化学方程式:
(填“<”“>”或“=”),写出工业合成氨的热化学方程式:___________ 。
(2)向某密闭容器中加入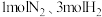 使其发生反应
使其发生反应 ,达到平衡后分别在
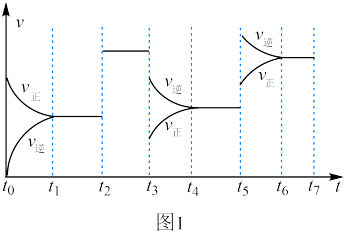
,达到平衡后分别在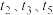 时均只改变某一个条件,相应反应速率的变化如图1所示。
时均只改变某一个条件,相应反应速率的变化如图1所示。 时改变的条件是
时改变的条件是___________ ,四个平衡状态中, 的平衡转化率最小的是
的平衡转化率最小的是___________ (填字母)。
a. b.
b. c.
c. d.
d.
(3)将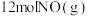 和
和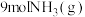 充入某一恒压(
充入某一恒压( )密闭容器内,控制不同温度使其发生反应:
)密闭容器内,控制不同温度使其发生反应: ,测得第
,测得第 时容器中
时容器中 转化率与温度的关系如图2所示。
转化率与温度的关系如图2所示。
___________ 0(填“<”或“>”);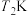 下,该反应的平衡常数
下,该反应的平衡常数
___________  (以分压表示,分压=总压
(以分压表示,分压=总压 物质的量分数)。
物质的量分数)。

(1)氨的人工合成使大幅度增加粮食产量的愿望变成了现实。
已知:①

②

③

则
 的燃烧热
的燃烧热
 (填“<”“>”或“=”),写出工业合成氨的热化学方程式:
(填“<”“>”或“=”),写出工业合成氨的热化学方程式:(2)向某密闭容器中加入
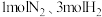 使其发生反应
使其发生反应 ,达到平衡后分别在
,达到平衡后分别在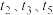 时均只改变某一个条件,相应反应速率的变化如图1所示。
时均只改变某一个条件,相应反应速率的变化如图1所示。 时改变的条件是
时改变的条件是 的平衡转化率最小的是
的平衡转化率最小的是a.
 b.
b. c.
c. d.
d.

(3)将
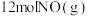 和
和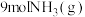 充入某一恒压(
充入某一恒压( )密闭容器内,控制不同温度使其发生反应:
)密闭容器内,控制不同温度使其发生反应: ,测得第
,测得第 时容器中
时容器中 转化率与温度的关系如图2所示。
转化率与温度的关系如图2所示。
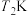 下,该反应的平衡常数
下,该反应的平衡常数
 (以分压表示,分压=总压
(以分压表示,分压=总压 物质的量分数)。
物质的量分数)。
您最近一年使用:0次
名校
5 . 已知常温下草酸( )的电离平衡常数为
)的电离平衡常数为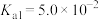 、
、 ;亚硫酸的电离平衡常数为
;亚硫酸的电离平衡常数为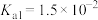 、
、 。
。
(1)草酸的一级电离方程式为___________ ;向草酸钾溶液中通入过量的 ,写出该反应的离子方程式
,写出该反应的离子方程式___________ 。
(2)实验室中用 草酸样品配制成
草酸样品配制成 溶液,然后取出
溶液,然后取出 ,用
,用 的酸性
的酸性 标准溶液滴定该
标准溶液滴定该 草酸溶液,以测定草酸样品的纯度,滴定终点时消耗
草酸溶液,以测定草酸样品的纯度,滴定终点时消耗 标准溶液。
标准溶液。
①下图中能正确表示盛有标准溶液的滴定管滴定前排气泡的操作是___________ (填字母)。
a.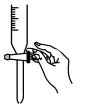 b.
b.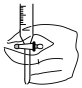 c.
c. 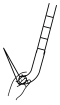 d.
d.
②达到滴定终点的现象是___________ 。该草酸样品中草酸的纯度是___________ (用含a、V的代数式表示)。
 )的电离平衡常数为
)的电离平衡常数为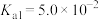 、
、 ;亚硫酸的电离平衡常数为
;亚硫酸的电离平衡常数为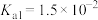 、
、 。
。(1)草酸的一级电离方程式为
 ,写出该反应的离子方程式
,写出该反应的离子方程式(2)实验室中用
 草酸样品配制成
草酸样品配制成 溶液,然后取出
溶液,然后取出 ,用
,用 的酸性
的酸性 标准溶液滴定该
标准溶液滴定该 草酸溶液,以测定草酸样品的纯度,滴定终点时消耗
草酸溶液,以测定草酸样品的纯度,滴定终点时消耗 标准溶液。
标准溶液。①下图中能正确表示盛有标准溶液的滴定管滴定前排气泡的操作是
a.
 b.
b. c.
c.  d.
d.
②达到滴定终点的现象是
您最近一年使用:0次
名校
6 . 下列事实中能证明 是弱电解质的有几项
是弱电解质的有几项
①氨水能与 溶液反应:
溶液反应:
② 的氨水与
的氨水与 的盐酸恰好完全反应
的盐酸恰好完全反应
③常温下, 的浓氨水中加水至
的浓氨水中加水至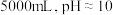
④用氨水做导电实验,灯泡很暗
⑤氯化铵溶液与 溶液反应:
溶液反应: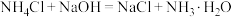
⑥常温下, 的氨水中
的氨水中
 是弱电解质的有几项
是弱电解质的有几项①氨水能与
 溶液反应:
溶液反应:
②
 的氨水与
的氨水与 的盐酸恰好完全反应
的盐酸恰好完全反应③常温下,
 的浓氨水中加水至
的浓氨水中加水至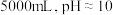
④用氨水做导电实验,灯泡很暗
⑤氯化铵溶液与
 溶液反应:
溶液反应: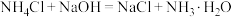
⑥常温下,
 的氨水中
的氨水中
| A.4项 | B.3项 | C.2项 | D.1项 |
您最近一年使用:0次
名校
7 . 用稀盐酸与稀 溶液(碱稍过量)测定中和反应的反应热时,下列有关说法错误的是
溶液(碱稍过量)测定中和反应的反应热时,下列有关说法错误的是
 溶液(碱稍过量)测定中和反应的反应热时,下列有关说法错误的是
溶液(碱稍过量)测定中和反应的反应热时,下列有关说法错误的是| A.酸、碱混合前应分别测量其温度 |
| B.酸碱混合时,应将碱溶液一次性快速加入到酸中 |
| C.实验中应上下抽动玻璃搅拌器 |
D.用量筒取盐酸时若仰视读数,则测得的反应热 偏大 偏大 |
您最近一年使用:0次
2023-09-25更新
|
112次组卷
|
3卷引用:安徽省淮北市第一中学2022-2023学年高二上学期11月期中化学试题
8 . 从下列实验事实所得出的现象解释或结论错误的是
| 选项 | 实验事实 | 现象解释或结论 |
| A | 将0.1mol/L5mL的Na2S2O3溶液和0.1mol/L5mL的H2SO4溶液混合后平均分装在2支试管中,一支放入冷水中,另一支放入热水中 | 放置在热水的试管中的溶液先出现浑浊,说明升高温度,化学反应速率会加快 |
| B | 锌与稀硫酸反应过程中,开始反应后速率逐渐增大 | 该反应是放热反应 |
| C | 压缩针筒内的NO2和N2O4混合气体,颜色先变深后变浅 | 颜色先变深是浓度变大的原因,后变浅是压强变化对化学平衡的影响 |
| D | 向2mL0.1mol/L的FeCl3溶液中加入1滴KSCN溶液变为红色后,再加入少量KCl固体 | 溶液红色变浅,说明增大生成物浓度会使平衡逆向移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-09-10更新
|
361次组卷
|
4卷引用:安徽省芜湖市无为襄安中学2022-2023学年高二上学期11月期中考试化学试题
名校
解题方法
9 . 在恒容容器中,对于可逆反应
 ,达到平衡后,升高温度,混合气体的密度增大,下列判断正确的是
,达到平衡后,升高温度,混合气体的密度增大,下列判断正确的是

 ,达到平衡后,升高温度,混合气体的密度增大,下列判断正确的是
,达到平衡后,升高温度,混合气体的密度增大,下列判断正确的是| A.B为气体 |
| B.向平衡体系中再加入一定量的B,能使平衡向着正反应方向移动 |
| C.在其它条件不变的情况下,缩小容器体积,平衡向若逆反应方向移动,平衡常数K值减小 |
| D.n可能为2 |
您最近一年使用:0次
10 . 工业合成氨的适宜条件是:①适宜温度(400~500℃) ②使用铁触媒作催化剂 ③压强为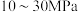 ④将混合气体中的氨气变为液氨,其中符合勒夏特列原理能提高反应物转化率的是
④将混合气体中的氨气变为液氨,其中符合勒夏特列原理能提高反应物转化率的是
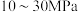 ④将混合气体中的氨气变为液氨,其中符合勒夏特列原理能提高反应物转化率的是
④将混合气体中的氨气变为液氨,其中符合勒夏特列原理能提高反应物转化率的是| A.①③④ | B.③④ | C.②③④ | D.①②③④ |
您最近一年使用:0次
2023-08-20更新
|
333次组卷
|
3卷引用:安徽省马鞍山市红星中学等3校2022-2023学年高二上学期11月期中考试化学试题



