解题方法
1 . 金属钛(22Ti)号称航天材料。回答下列问题。
(1)基态钛原子的价层电子排布式为___________ ,它位于元素周期表的___________ 区。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料,钛的硬度比铝大的原因是___________ 。
(3)TiX4的熔点如下表所示:
依F、Cl、Br、I次序,TiX4的化学键中离子键成分的百分数逐渐___________ (填“增强”、“减弱”或“不变”);分析TiCl4、TiBr4、TiI4的熔点呈现一定变化规律的原因是___________ 。
(1)基态钛原子的价层电子排布式为
(2)钛比钢轻、比铝硬,是一种新兴的结构材料,钛的硬度比铝大的原因是
(3)TiX4的熔点如下表所示:
| TiF4 | TiCl4 | TiBr4 | TiI4 | |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
您最近一年使用:0次
名校
解题方法
2 . 按要求完成下列填空。
(1)漂白粉的有效成分的化学式:___________ ,Na2O2中阴离子与阳离子个数比为:___________ 。
(2)氢氧化钡在水溶液中的电离方程式:___________ 。
(3)已知 ,在该反应中,还原剂是
,在该反应中,还原剂是___________ (填化学式)。
(1)漂白粉的有效成分的化学式:
(2)氢氧化钡在水溶液中的电离方程式:
(3)已知
 ,在该反应中,还原剂是
,在该反应中,还原剂是
您最近一年使用:0次
名校
解题方法
3 . 根据所学知识,回答下列问题:
(1)24.2g某硝酸盐M(NO3)3中含有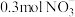 ,则该硝酸盐的摩尔质量为
,则该硝酸盐的摩尔质量为___________ 。
(2)钠长期置于空气中,最后形成的物质是___________ (填化学式),该物质的溶液与氯化钙溶液混合后,发生反应的离子方程式为___________ 。
(3)资料查得:“84消毒液”(主要成分是NaClO)与双氧水混合会反应产生一种常见的无色无味气体,且消毒能力大大降低,写出该反应的离子方程式___________ 。
(1)24.2g某硝酸盐M(NO3)3中含有
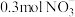 ,则该硝酸盐的摩尔质量为
,则该硝酸盐的摩尔质量为(2)钠长期置于空气中,最后形成的物质是
(3)资料查得:“84消毒液”(主要成分是NaClO)与双氧水混合会反应产生一种常见的无色无味气体,且消毒能力大大降低,写出该反应的离子方程式
您最近一年使用:0次
名校
解题方法
4 . 回答下列问题。
(1)请根据下列信息判断氢气燃烧生成水蒸气时热量变化。
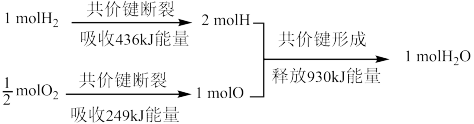
生成1mol水释放的能量___________ kJ。
(2)2SO2(g)+O2(g) 2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
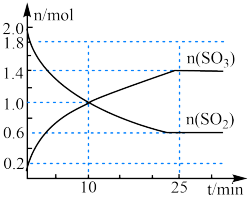
①0到10 min内, v(O2)=___________ 。
②下列情况能说明该反应达到化学平衡状态的是___________ (填字母)。
A. n(SO2) = n(SO3) B. v正 (SO2)=v逆 (SO2)
C. O2的含量保持不变 D.SO2、O2、SO3的浓度之比为2:1:2
③在密闭容器里,通入a mol SO2 (g)、b mol O2 (g)、c mol SO3 (g),发生上述反应,当改变某种条件时,反应速率会减小的是___________ (填字母)。
A.降低温度 B.加入催化剂
C.增大容器体积 D.恒容下,充入He
④工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7%,O2:11%,N2:82%):
化工生产中,为了提高反应进行的程度而调控反应条件时,需要考虑控制反应条件的成本和实际可能性。催化氧化的生产时:温度较低时,反应速率小,需要很长时间才能达到化学平衡,生产成本高;而压强越大,对动力和生产设备的要求也越高。请结合上表,分析工业生产SO2催化氧化过程的适宜条件为:___________ 。
(1)请根据下列信息判断氢气燃烧生成水蒸气时热量变化。

生成1mol水释放的能量
(2)2SO2(g)+O2(g)
 2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
2SO3(g),是工业制硫酸的主要反应之一、某条件下,在2 L恒容容器中投入2 mol SO2和1 mol O2,如图是反应体系中部分物质的物质的量随时间的变化曲线。
①0到10 min内, v(O2)=
②下列情况能说明该反应达到化学平衡状态的是
A. n(SO2) = n(SO3) B. v正 (SO2)=v逆 (SO2)
C. O2的含量保持不变 D.SO2、O2、SO3的浓度之比为2:1:2
③在密闭容器里,通入a mol SO2 (g)、b mol O2 (g)、c mol SO3 (g),发生上述反应,当改变某种条件时,反应速率会减小的是
A.降低温度 B.加入催化剂
C.增大容器体积 D.恒容下,充入He
④工业上生产硫酸时,利用催化氧化反应将SO2转化为SO3是一个关键步骤。压强及温度对SO2转化率的影响如下表(原料气各成分的体积分数为:SO2:7%,O2:11%,N2:82%):
 | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |
您最近一年使用:0次
2023-09-09更新
|
244次组卷
|
2卷引用:浙江省嘉兴八校联盟2021-2022学年高一下学期期中联考化学试题
5 . 某晶体晶胞结构如图所示,●表示X , 表示Y,请回答下列问题:
表示Y,请回答下列问题:

(1)晶体中每个X周围与之等距且距离最近的Y有___________ 个,每个Y周围与之等距且距离最近的Y有___________ 个,每个晶胞中含X的个数为___________ 个,该晶体的化学式为___________ 。
(2)若该晶胞的边长为a cm,则晶体的密度为___________ g·cm-3(列出计算式即可,已知该物质的摩尔质量为M g/mol,阿伏加德罗常数为NA)。
 表示Y,请回答下列问题:
表示Y,请回答下列问题:
(1)晶体中每个X周围与之等距且距离最近的Y有
(2)若该晶胞的边长为a cm,则晶体的密度为
您最近一年使用:0次
6 . 下列关于晶体的叙述正确的是
| A.晶体是具有一定几何外观的,所以铁粉不属于金属晶体 |
| B.金属导电和熔融电解质(或电解质溶液)导电的原理一样 |
| C.金属晶体由金属阳离子和阴离子构成 |
| D.离子晶体都是化合物 |
您最近一年使用:0次
2023-09-08更新
|
288次组卷
|
4卷引用:浙江省嘉兴八校联盟2021-2022学年高二下学期期中联考化学试题
浙江省嘉兴八校联盟2021-2022学年高二下学期期中联考化学试题安徽省淮南第二中学2023-2024学年高二下学期期中测试化学试题(已下线)选择题1-5(已下线)3.3.1 金属晶体 离子晶体(提高)
7 . 下列关于聚集状态的描述中,错误 的是
| A.物质只有气、液、固三种聚集状态 |
| B.等离子体是一种很好的导电体,在信息产业等领域有非常好的应用前景 |
| C.液晶用于各种显示仪器上 |
| D.超分子是由两个或多个分子相互“组合”在一起形成具有特定结构和功能的聚集体 |
您最近一年使用:0次
解题方法
8 . 维生素C,别称L-抗坏血酸,具有抗氧化、抗自由基的作用。其结构如下图所示,下列关于维生素C叙述错误 的是


| A.分子中含有2个手性碳原子 |
| B.分子中碳原子的杂化轨道类型为sp3和sp2 |
| C.维生素C结构中的含氧官能团为酮羰基和羟基 |
| D.该分子易溶于水 |
您最近一年使用:0次
9 . 下列关于HF的性质,与氢键无关 的是
| A.HF的酸性小于HCl | B.HF的沸点大于HCl |
| C.HF易溶于水 | D.常温常压下,HF以缔合分子形式存在 |
您最近一年使用:0次
解题方法
10 . 下列物质的变化规律与分子间作用力有关的是
| A.热稳定性:HBr<HCl |
| B.沸点由低到高:H2S<H2Se<H2Te<H2O |
| C.硬度由大到小:金刚石>碳化硅 |
| D.晶体熔点由低到高:NaF<MgO |
您最近一年使用:0次



