名校
1 . I.参考下列图表和有关要求回答问题:
(1)图I是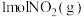 和
和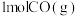 反应生成
反应生成 和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,
和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大, 的变化是
的变化是_______ (填“增大”、“减小”、“不变”,下同), 的变化是
的变化是_______ 。请写出 和CO反应的热化学方程式:
和CO反应的热化学方程式:_______ 。

Ⅱ.全球大气 浓度升高对人类生产生活产生了影响,研究二氧化碳的回收对我国2060年实现碳中和具有现实意义,碳及其化合物的资源化利用成为研究热点。
浓度升高对人类生产生活产生了影响,研究二氧化碳的回收对我国2060年实现碳中和具有现实意义,碳及其化合物的资源化利用成为研究热点。 经催化加氢可以生成低碳有机物,主要有以下反应:
经催化加氢可以生成低碳有机物,主要有以下反应:
反应I:
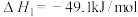
反应Ⅱ: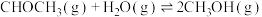
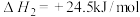
反应Ⅲ:

(2)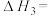
_______ kJ/mol。
(3)已知:反应Ⅱ在某温度下的平衡常数的值为2,在此温度下向密闭容器中加入等物质的量的 和
和 发生该反应,某时刻测得
发生该反应,某时刻测得 、
、 、
、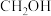 的浓度依次1.5mol/L、1.5mol/L、1mol/L,此时
的浓度依次1.5mol/L、1.5mol/L、1mol/L,此时 的转化率是
的转化率是_______ ,反应速率
_______ 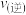 (选填“>”、“=”或“<”)。
(选填“>”、“=”或“<”)。
(4)在某压强下,反应I在不同温度、不同投料比时 的平衡转化率如图所示。则温度
的平衡转化率如图所示。则温度
_______  (用“>、=、<”填空),该反应的平衡常数
(用“>、=、<”填空),该反应的平衡常数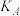 、
、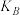 、
、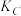 三者之间的大小关系为
三者之间的大小关系为_______ 。

(5) 在
在 催化下同时发生如下反应a、b,是解决温室效应和能源短缺的重要手段。
催化下同时发生如下反应a、b,是解决温室效应和能源短缺的重要手段。
a.
b.
保持温度T时,在体积不变的密闭容器中,充入一定量的 及
及 ,起始及达平衡时容器内各气体物质的量如表所示:
,起始及达平衡时容器内各气体物质的量如表所示:
已知起始时容器内的压强为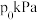 ,达平衡时容器内总压强为pkPa。若反应a、b均达平衡时,
,达平衡时容器内总压强为pkPa。若反应a、b均达平衡时,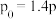 ,则表中
,则表中
_______ ;反应a的平衡常数
_______ (用含p的式子表示)。
(1)图I是
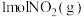 和
和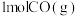 反应生成
反应生成 和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,
和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大, 的变化是
的变化是 的变化是
的变化是 和CO反应的热化学方程式:
和CO反应的热化学方程式:
Ⅱ.全球大气
 浓度升高对人类生产生活产生了影响,研究二氧化碳的回收对我国2060年实现碳中和具有现实意义,碳及其化合物的资源化利用成为研究热点。
浓度升高对人类生产生活产生了影响,研究二氧化碳的回收对我国2060年实现碳中和具有现实意义,碳及其化合物的资源化利用成为研究热点。 经催化加氢可以生成低碳有机物,主要有以下反应:
经催化加氢可以生成低碳有机物,主要有以下反应:反应I:

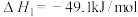
反应Ⅱ:
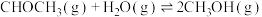
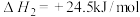
反应Ⅲ:


(2)
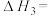
(3)已知:反应Ⅱ在某温度下的平衡常数的值为2,在此温度下向密闭容器中加入等物质的量的
 和
和 发生该反应,某时刻测得
发生该反应,某时刻测得 、
、 、
、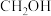 的浓度依次1.5mol/L、1.5mol/L、1mol/L,此时
的浓度依次1.5mol/L、1.5mol/L、1mol/L,此时 的转化率是
的转化率是
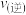 (选填“>”、“=”或“<”)。
(选填“>”、“=”或“<”)。(4)在某压强下,反应I在不同温度、不同投料比时
 的平衡转化率如图所示。则温度
的平衡转化率如图所示。则温度
 (用“>、=、<”填空),该反应的平衡常数
(用“>、=、<”填空),该反应的平衡常数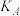 、
、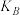 、
、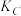 三者之间的大小关系为
三者之间的大小关系为
(5)
 在
在 催化下同时发生如下反应a、b,是解决温室效应和能源短缺的重要手段。
催化下同时发生如下反应a、b,是解决温室效应和能源短缺的重要手段。a.

b.

保持温度T时,在体积不变的密闭容器中,充入一定量的
 及
及 ,起始及达平衡时容器内各气体物质的量如表所示:
,起始及达平衡时容器内各气体物质的量如表所示: |  |  |  |  | |
| 起始/mol | 0.5 | 0.9 | 0 | 0 | 0 |
| 平衡/mol | n | 0.3 |
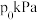 ,达平衡时容器内总压强为pkPa。若反应a、b均达平衡时,
,达平衡时容器内总压强为pkPa。若反应a、b均达平衡时,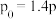 ,则表中
,则表中

您最近一年使用:0次
名校
2 . I.某实验小组用0.50mol/LNaOH溶液和0.50mol/L硫酸溶液进行中和热的测定。测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示。

简易量热计示意图
(1)仪器a的名称为_______ 。
(2)取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如表。
①请填写表中的空白:
②近似认为0.50mol/LNaOH溶液和0.50mol/L硫酸溶液的密度都是 ,中和后生成溶液的比热容
,中和后生成溶液的比热容 。则中和热
。则中和热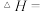
_______ (取小数点后一位)。
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是_______ (填字母)。
a.实验装置保温、隔热效果差
b.配制0.50mol/LNaOH溶液定容时俯视刻度线读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
e.用量筒量取NaOH溶液的体积时仰视读数
Ⅱ.探究化学反应的快慢和限度具有十分重要的意义。
某实验小组欲通过用酸性 和
和 (草酸)反应测定单位时间内生成
(草酸)反应测定单位时间内生成 的体积,探究影响反应速率的因素。设计的实验方案如下(
的体积,探究影响反应速率的因素。设计的实验方案如下( 溶液已酸化),实验装置如图甲所示:
溶液已酸化),实验装置如图甲所示:

(3)完成上述反应的离子方程式为:_______ 。
_______ _______
_______ _______=_______
_______=_______ _______
_______ _______
_______
该实验是探究_______ 对反应速率的影响。
(4)若实验①在2min末收集了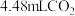 (标准状况下),则在2min末
(标准状况下),则在2min末
_______ (假设混合溶液的体积为50mL,反应前后体积变化忽略不计)。
Ⅲ.溶液中存在平衡: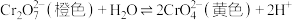 。该溶液具有强氧化性。其还原产物
。该溶液具有强氧化性。其还原产物 在水溶液中呈绿色或蓝绿色。用溶液进行下列实验:
在水溶液中呈绿色或蓝绿色。用溶液进行下列实验:
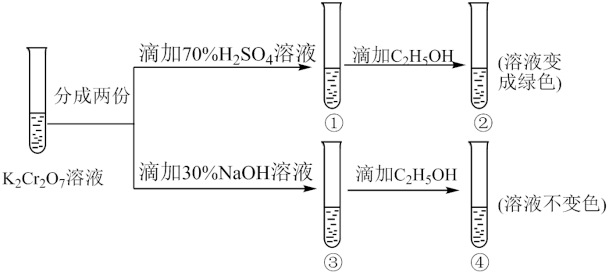
(5)向 溶液中加入30%NaOH溶液。溶液呈
溶液中加入30%NaOH溶液。溶液呈_______ 色:向 溶液中逐滴加入
溶液中逐滴加入 溶液(已知
溶液(已知 为黄色沉淀),则平衡向着
为黄色沉淀),则平衡向着_______ 方向移动,溶液颜色变化为_______ 。

简易量热计示意图
(1)仪器a的名称为
(2)取50mLNaOH溶液和30mL硫酸溶液进行实验,实验数据如表。
①请填写表中的空白:
| 温度 实验次数 | 起始温度 /℃ /℃ | 终止温度 /℃ /℃ | 温度差平均值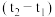 /℃ /℃ | ||
 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
 ,中和后生成溶液的比热容
,中和后生成溶液的比热容 。则中和热
。则中和热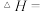
③上述实验数值结果与57.3kJ/mol有偏差,产生偏差的原因可能是
a.实验装置保温、隔热效果差
b.配制0.50mol/LNaOH溶液定容时俯视刻度线读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
e.用量筒量取NaOH溶液的体积时仰视读数
Ⅱ.探究化学反应的快慢和限度具有十分重要的意义。
某实验小组欲通过用酸性
 和
和 (草酸)反应测定单位时间内生成
(草酸)反应测定单位时间内生成 的体积,探究影响反应速率的因素。设计的实验方案如下(
的体积,探究影响反应速率的因素。设计的实验方案如下( 溶液已酸化),实验装置如图甲所示:
溶液已酸化),实验装置如图甲所示:
| 实验序号 | A溶液 | B溶液 |
| ① |  溶液 溶液 | 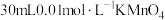 溶液 溶液 |
| ② | 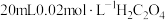 溶液 溶液 | 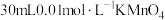 溶液 溶液 |
(3)完成上述反应的离子方程式为:
_______
 _______
_______ _______=_______
_______=_______ _______
_______ _______
_______该实验是探究
(4)若实验①在2min末收集了
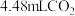 (标准状况下),则在2min末
(标准状况下),则在2min末
Ⅲ.溶液中存在平衡:
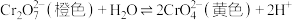 。该溶液具有强氧化性。其还原产物
。该溶液具有强氧化性。其还原产物 在水溶液中呈绿色或蓝绿色。用溶液进行下列实验:
在水溶液中呈绿色或蓝绿色。用溶液进行下列实验:
(5)向
 溶液中加入30%NaOH溶液。溶液呈
溶液中加入30%NaOH溶液。溶液呈 溶液中逐滴加入
溶液中逐滴加入 溶液(已知
溶液(已知 为黄色沉淀),则平衡向着
为黄色沉淀),则平衡向着
您最近一年使用:0次
名校
3 . 硫酸工业在国民经济中占有极其重要的地位。下图是工业制硫酸的生产流程示意图:

(1)将燃烧黄铁矿的化学方程式补充完整:4_______ 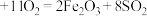
(2)转化是工业制硫酸的重要一步,即 和空气的混合物通过转化器反应生成
和空气的混合物通过转化器反应生成 ,实际生产中,反应温度选定在475℃左右。
,实际生产中,反应温度选定在475℃左右。
①写出转化器中发生反应的化学方程式是_______ 。
②反应温度选在475℃左右的依据是_______ 。
③工业上是如何加热原料气的?_______ 。这样设计的好处是_______ 。
(3)依据工艺流程图判断下列说法错误的是_______。
(4)工业制硫酸的工艺中,通常用来吸收尾气的物质是_______。
(5)下列说法错误的是_______。
(6)在硫酸的工业生产中,下列生产操作及其原因解释二者都正确的是_______。
①硫铁矿燃烧前需要粉碎,因为块状硫铁矿不能燃烧
② 氧化为
氧化为 时需要高压,这样可以提高
时需要高压,这样可以提高 的转化率
的转化率
③ 氧化为
氧化为 时需要使用催化剂,这样可以提高
时需要使用催化剂,这样可以提高 的转化率
的转化率
④用98.3%的浓 吸收
吸收 ,可以防止形成酸雾阻碍
,可以防止形成酸雾阻碍 的吸收
的吸收

(1)将燃烧黄铁矿的化学方程式补充完整:4
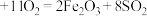
(2)转化是工业制硫酸的重要一步,即
 和空气的混合物通过转化器反应生成
和空气的混合物通过转化器反应生成 ,实际生产中,反应温度选定在475℃左右。
,实际生产中,反应温度选定在475℃左右。①写出转化器中发生反应的化学方程式是
②反应温度选在475℃左右的依据是
③工业上是如何加热原料气的?
(3)依据工艺流程图判断下列说法错误的是_______。
| A.为使黄铁矿充分燃烧,需将其粉碎 |
B.过量空气能提高 的转化率 的转化率 |
C.使用催化剂能提高 的反应速率和转化率 的反应速率和转化率 |
| D.沸腾炉排出的矿渣可供炼铁 |
(4)工业制硫酸的工艺中,通常用来吸收尾气的物质是_______。
| A.氨水 | B.硫酸 | C.氯化钙 | D.氢硫酸 |
(5)下列说法错误的是_______。
| A.化学反应速率理论是研究怎样在一定时间内加快产品的生产 |
| B.化学平衡理论是研究怎样使用有限原料提高产品的产量 |
| C.化学反应速率理论是研究怎样提高原料的转化率 |
| D.化工生产要坚持绿色环保的生产方式,实现可持续发展 |
(6)在硫酸的工业生产中,下列生产操作及其原因解释二者都正确的是_______。
①硫铁矿燃烧前需要粉碎,因为块状硫铁矿不能燃烧
②
 氧化为
氧化为 时需要高压,这样可以提高
时需要高压,这样可以提高 的转化率
的转化率③
 氧化为
氧化为 时需要使用催化剂,这样可以提高
时需要使用催化剂,这样可以提高 的转化率
的转化率④用98.3%的浓
 吸收
吸收 ,可以防止形成酸雾阻碍
,可以防止形成酸雾阻碍 的吸收
的吸收| A.①② | B.②③ | C.仅④ | D.③④ |
您最近一年使用:0次
名校
4 .  是重要的化工原料,可利用乙烯制备乙醇:
是重要的化工原料,可利用乙烯制备乙醇: 。向2L恒容密闭容器中充入
。向2L恒容密闭容器中充入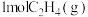 和
和 ,测得
,测得 的平衡转化率与
的平衡转化率与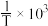 的关系如图所示,已知分压=总压×气体物质的量分数,用气体分压替代浓度计算的平衡常数叫压强平衡常数
的关系如图所示,已知分压=总压×气体物质的量分数,用气体分压替代浓度计算的平衡常数叫压强平衡常数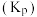 ,下列说法错误的是
,下列说法错误的是

 是重要的化工原料,可利用乙烯制备乙醇:
是重要的化工原料,可利用乙烯制备乙醇: 。向2L恒容密闭容器中充入
。向2L恒容密闭容器中充入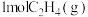 和
和 ,测得
,测得 的平衡转化率与
的平衡转化率与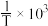 的关系如图所示,已知分压=总压×气体物质的量分数,用气体分压替代浓度计算的平衡常数叫压强平衡常数
的关系如图所示,已知分压=总压×气体物质的量分数,用气体分压替代浓度计算的平衡常数叫压强平衡常数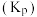 ,下列说法错误的是
,下列说法错误的是
| A.该反应为放热反应 |
B.保持其他条件不变,将容器改为恒压密闭容器,则a点对应温度下 的平衡转化率小于20% 的平衡转化率小于20% |
C.若a点的压强为pkPa,则该温度下的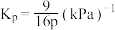 |
D.若反应从开始到b点用时5min,则0~5min内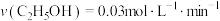 |
您最近一年使用:0次
名校
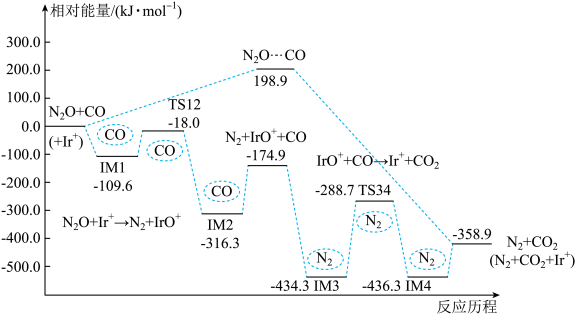
5 . 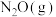 与
与 发生反应的能量变化如图所示,
发生反应的能量变化如图所示,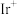 作为反应的催化剂。下列说法正确的是
作为反应的催化剂。下列说法正确的是
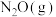 与
与 发生反应的能量变化如图所示,
发生反应的能量变化如图所示,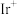 作为反应的催化剂。下列说法正确的是
作为反应的催化剂。下列说法正确的是
| A.使用催化剂时,该反应的正反应活化能为198.9kJ/mol |
| B.催化剂参与的两步反应均为吸热反应 |
C.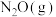 、 、 、 、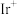 夺取O的能力依次增大 夺取O的能力依次增大 |
D.总反应的热化学方程式为: 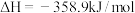 |
您最近一年使用:0次
名校
6 . 下列方程式不能准确解释相应实验现象的是
A. 和浓盐酸共热产生黄绿色气体: 和浓盐酸共热产生黄绿色气体: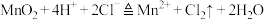 |
B.Na加入滴有酚酞的水中,溶液变红: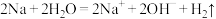 |
C.加热Fe和S的混合物生成黑色固体: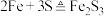 |
D. 、 、 、HI平衡混合气体加热后颜色变深: 、HI平衡混合气体加热后颜色变深:  |
您最近一年使用:0次
名校
7 . 下列说法或表示方法正确的是
A.  ; ;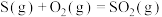  , , |
B.由“ 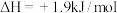 ”可知,金刚石比石墨稳定 ”可知,金刚石比石墨稳定 |
C.500℃、300MPa下,将 和 和 置于密闭的容器中充分反应生成 置于密闭的容器中充分反应生成 ,放热19.3kJ,其热化学方程式为: ,放热19.3kJ,其热化学方程式为: 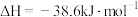 |
D.已知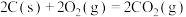  , ,  ,则 ,则 |
您最近一年使用:0次
名校
8 . 在 反应中,下列表示该反应速率
反应中,下列表示该反应速率最慢 的是
 反应中,下列表示该反应速率
反应中,下列表示该反应速率A. | B.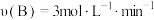 |
C.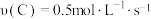 | D.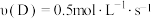 |
您最近一年使用:0次
9 . 属于氧化还原反应且反应过程中能量变化符合如图所示的是
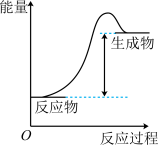

A.CaCO3 CaO+CO2↑ CaO+CO2↑ | B.CH4+2O2 CO2+2H2O CO2+2H2O |
C.C+CO2 2CO 2CO | D.2KOH+H2SO4=K2SO4+2H2O |
您最近一年使用:0次
2023-08-14更新
|
144次组卷
|
2卷引用:内蒙古第一机械制造(集团)有限公司第一中学2023-2024学年高二上学期9月月考化学试题
名校
10 . 下列叙述正确的是
| A.共价化合物中一定含有极性共价键 |
| B.外界条件发生变化,化学反应速率一定改变 |
| C.对于已平衡的可逆反应,正逆反应的反应速率发生了改变,化学平衡一定发生移动 |
| D.构成原电池的两个电极材料一定是两种活泼性不同的金属 |
您最近一年使用:0次
2023-08-10更新
|
194次组卷
|
2卷引用:内蒙古第一机械制造(集团)有限公司第一中学2023-2024学年高二上学期9月月考化学试题



