名校
1 . 回答下列问题。
(1)某课外活动小组为探究BaSO4的溶解度,分别将足量BaSO4放入:①5mL水;②20mL0.5mol·L-1的Na2SO4溶液;③40mL0.2mol·L-1的Ba(OH)2溶液;④40mL0.1mol·L-1的H2SO4溶液中,溶解至饱和。
以上各溶液中,c(Ba2+)的大小顺序正确的是___________ ,BaSO4的溶解度的大小顺序为___________ (填序号)。
(2)已知BiCl3水解生成BiOCl沉淀,若把适量固体BiCl3置于浓NaCl溶液中可得到澄清溶液。
①写出水解反应的方程式:___________ 。
②医药上把BiOCl叫做次氯酸铋,你同意此名称吗?请说出你的理由___________ 。
③把适量固体BiCl3置于浓NaCl溶液中,可得澄清溶液,可能的原因___________ 。
④实验室还可以如何配制BiCl3溶液?___________
(1)某课外活动小组为探究BaSO4的溶解度,分别将足量BaSO4放入:①5mL水;②20mL0.5mol·L-1的Na2SO4溶液;③40mL0.2mol·L-1的Ba(OH)2溶液;④40mL0.1mol·L-1的H2SO4溶液中,溶解至饱和。
以上各溶液中,c(Ba2+)的大小顺序正确的是
(2)已知BiCl3水解生成BiOCl沉淀,若把适量固体BiCl3置于浓NaCl溶液中可得到澄清溶液。
①写出水解反应的方程式:
②医药上把BiOCl叫做次氯酸铋,你同意此名称吗?请说出你的理由
③把适量固体BiCl3置于浓NaCl溶液中,可得澄清溶液,可能的原因
④实验室还可以如何配制BiCl3溶液?
您最近一年使用:0次
名校
2 . 某二元酸H2A的电离方程式是: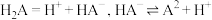 。回答下列问题:
。回答下列问题:
(1)Na2A溶液显___________ (填“酸性”、“碱性”或“中性”),理由是(用离子方程式表示)___________ 。
(2)NaHA溶液显___________ (填“酸性”、“碱性”或“中性”),理由是(用离子方程式表示)___________ 。
(3)若0.1mol·L-1NaHA溶液的pH=2,则0.1mol·L-1H2A溶液中氢离子的物质的量浓度可能___________ 0.11mol·L-1(填“<”、“>”或“=”),理由是:___________ 。
(4)0.1mol·L-1NaHA溶液中各离子浓度由大到小的顺序是___________ 。
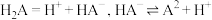 。回答下列问题:
。回答下列问题:(1)Na2A溶液显
(2)NaHA溶液显
(3)若0.1mol·L-1NaHA溶液的pH=2,则0.1mol·L-1H2A溶液中氢离子的物质的量浓度可能
(4)0.1mol·L-1NaHA溶液中各离子浓度由大到小的顺序是
您最近一年使用:0次
名校
3 . 下列两组热化学方程式中,有关 的关系正确的是
的关系正确的是
①





②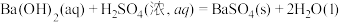



 的关系正确的是
的关系正确的是①






②
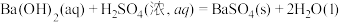



A.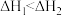 ; ;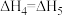 | B. ; ;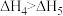 |
C. ; ;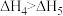 | D. ; ; |
您最近一年使用:0次
名校
4 . 一定条件下,体积一定的密闭容器中,1molX和 进行反应:
进行反应: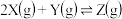 ,经
,经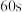 达到平衡,生成
达到平衡,生成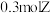 。下列说法正确的是
。下列说法正确的是
 进行反应:
进行反应: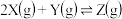 ,经
,经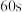 达到平衡,生成
达到平衡,生成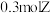 。下列说法正确的是
。下列说法正确的是A.以 浓度变化表示的反应速率为 浓度变化表示的反应速率为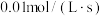 |
B.将容器体积变为原来2倍, 的平衡浓度变为原来的 的平衡浓度变为原来的 |
C.若增大压强,则物质 的转化率增大 的转化率增大 |
D.若升高温度,X的体积分数增大,则该反应的 |
您最近一年使用:0次
名校
5 . 在蒸发发皿中加热蒸干并灼烧(低于400℃)下列的溶液,可以得到该物质的固体是
| A.氯化铝溶液 | B.硫酸亚铁溶液 | C.碳酸氢钠溶液 | D.硫酸铝溶液 |
您最近一年使用:0次
6 . 雾霾严重危害人类健康和生态环境,开发稳定高效的脱硫脱硝工艺技术是国内外研究的热点。研究表明,氮氧化物 和二氧化硫在形成雾霾时与大气中的氨有关,其转化关系如图所示。
和二氧化硫在形成雾霾时与大气中的氨有关,其转化关系如图所示。 溶液中的离子浓度由大到小顺序是
溶液中的离子浓度由大到小顺序是___________ 。
(2)①已知: 生成
生成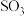 总反应的化学方程式是
总反应的化学方程式是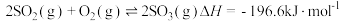 ,此反应可通过如下两步完成:
,此反应可通过如下两步完成: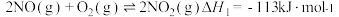 ;
;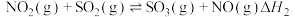 。则
。则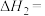
___________ 。
②一定温度下,向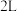 恒容密闭容器中充入
恒容密闭容器中充入 和
和 各
各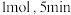 达到平衡,此时容器中
达到平衡,此时容器中 和
和 的浓度之比为
的浓度之比为 ,则
,则 的平衡转化率是
的平衡转化率是___________ 。
(3) 属于酸性氧化物,将其通入
属于酸性氧化物,将其通入 溶液中,得到
溶液中,得到 溶液。
溶液。
① 溶液呈酸性,其原因是
溶液呈酸性,其原因是___________ 。
②向 的
的 溶液中滴加一定浓度的
溶液中滴加一定浓度的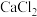 溶液,溶液中出现浑浊,
溶液,溶液中出现浑浊, 降为2,用化学平衡移动原理解释溶液
降为2,用化学平衡移动原理解释溶液 降低的原因:
降低的原因:___________ 。
(4)通过 传感器可监测
传感器可监测 的含量,其工作原理示意图如图。
的含量,其工作原理示意图如图。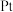 电极上发生的是
电极上发生的是___________ (填“氧化”或“还原”)反应。
②写出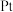 电极的电极反应式:
电极的电极反应式:___________ 。
③写出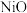 电极的电极反应式:
电极的电极反应式:___________ 。
 和二氧化硫在形成雾霾时与大气中的氨有关,其转化关系如图所示。
和二氧化硫在形成雾霾时与大气中的氨有关,其转化关系如图所示。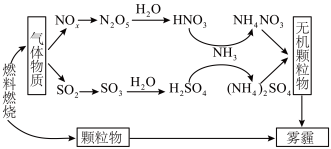
 溶液中的离子浓度由大到小顺序是
溶液中的离子浓度由大到小顺序是(2)①已知:
 生成
生成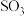 总反应的化学方程式是
总反应的化学方程式是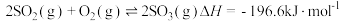 ,此反应可通过如下两步完成:
,此反应可通过如下两步完成: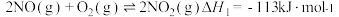 ;
;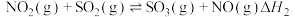 。则
。则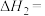
②一定温度下,向
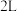 恒容密闭容器中充入
恒容密闭容器中充入 和
和 各
各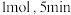 达到平衡,此时容器中
达到平衡,此时容器中 和
和 的浓度之比为
的浓度之比为 ,则
,则 的平衡转化率是
的平衡转化率是(3)
 属于酸性氧化物,将其通入
属于酸性氧化物,将其通入 溶液中,得到
溶液中,得到 溶液。
溶液。①
 溶液呈酸性,其原因是
溶液呈酸性,其原因是②向
 的
的 溶液中滴加一定浓度的
溶液中滴加一定浓度的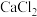 溶液,溶液中出现浑浊,
溶液,溶液中出现浑浊, 降为2,用化学平衡移动原理解释溶液
降为2,用化学平衡移动原理解释溶液 降低的原因:
降低的原因:(4)通过
 传感器可监测
传感器可监测 的含量,其工作原理示意图如图。
的含量,其工作原理示意图如图。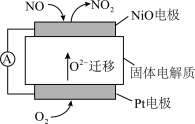
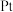 电极上发生的是
电极上发生的是②写出
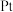 电极的电极反应式:
电极的电极反应式:③写出
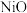 电极的电极反应式:
电极的电极反应式:
您最近一年使用:0次
名校
解题方法
7 . 目前工业上有一种方法是用 来生产燃料甲醇。一定条件下发生反应:
来生产燃料甲醇。一定条件下发生反应: ,如图表示该反应过程中能量(单位为
,如图表示该反应过程中能量(单位为 )的变化:
)的变化:
(2)为探究反应原理,现进行如下实验,在体积为 的密闭容器中,充入
的密闭容器中,充入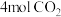 和
和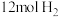 ,一定条件下发生反应:
,一定条件下发生反应: ,经测得
,经测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。 内用
内用 表示的该反应的反应速率
表示的该反应的反应速率
_____ ; 时,正反应速率
时,正反应速率_____ 逆反应速率(填“>”“=”或“<”)。
② 反应达平衡,
反应达平衡, 的转化率为
的转化率为_____ 。该反应的平衡常数
_____ 。
③下列措施中能使化学平衡向正反应方向移动的是_____ (填字母)。
A.升高温度 B.将 及时液化抽出
及时液化抽出
C.选择高效催化剂 D.保持容器的容积不变,再充入 和
和
④能说明该反应未达到化学平衡状态的是_____ 。
A.容器中混合气体的密度不再改变 B.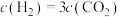
C. D.容器内的压强保持不变
D.容器内的压强保持不变
 来生产燃料甲醇。一定条件下发生反应:
来生产燃料甲醇。一定条件下发生反应: ,如图表示该反应过程中能量(单位为
,如图表示该反应过程中能量(单位为 )的变化:
)的变化: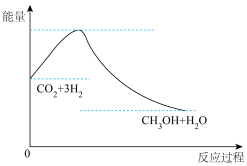
A. , , | B. , , |
C. , , | D. , , |
(2)为探究反应原理,现进行如下实验,在体积为
 的密闭容器中,充入
的密闭容器中,充入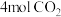 和
和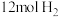 ,一定条件下发生反应:
,一定条件下发生反应: ,经测得
,经测得 和
和 的浓度随时间变化如图所示。
的浓度随时间变化如图所示。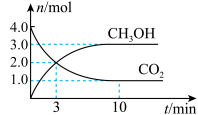
 内用
内用 表示的该反应的反应速率
表示的该反应的反应速率
 时,正反应速率
时,正反应速率②
 反应达平衡,
反应达平衡, 的转化率为
的转化率为
③下列措施中能使化学平衡向正反应方向移动的是
A.升高温度 B.将
 及时液化抽出
及时液化抽出C.选择高效催化剂 D.保持容器的容积不变,再充入
 和
和
④能说明该反应未达到化学平衡状态的是
A.容器中混合气体的密度不再改变 B.
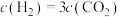
C.
 D.容器内的压强保持不变
D.容器内的压强保持不变
您最近一年使用:0次
8 . 某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣(已除去葡萄糖溶液过滤得到的),对甘蔗渣进行综合利用不仅可以提高经济效益,而且还能防止环境污染。生产流程如图所示。 的产量可以用来衡量一个国家石油化学工业的发展水平,
的产量可以用来衡量一个国家石油化学工业的发展水平, 的分子中含有醛基,
的分子中含有醛基, 是具有香味的液体。完成下列各题。
是具有香味的液体。完成下列各题。
(1)A的名称为___________ ; 的名称为
的名称为___________ 。
(2)B的结构简式为___________ ; 的结构简式为
的结构简式为___________ , 的官能团名称为
的官能团名称为___________ 。
(3)写出 的化学方程式:
的化学方程式:___________ 。
(4)写出 的化学方程式:
的化学方程式:___________ 。
(5)写出 的同分异构体中与
的同分异构体中与 互为同系物的结构简式:
互为同系物的结构简式:___________ 。

 的产量可以用来衡量一个国家石油化学工业的发展水平,
的产量可以用来衡量一个国家石油化学工业的发展水平, 的分子中含有醛基,
的分子中含有醛基, 是具有香味的液体。完成下列各题。
是具有香味的液体。完成下列各题。(1)A的名称为
 的名称为
的名称为(2)B的结构简式为
 的结构简式为
的结构简式为 的官能团名称为
的官能团名称为(3)写出
 的化学方程式:
的化学方程式:(4)写出
 的化学方程式:
的化学方程式:(5)写出
 的同分异构体中与
的同分异构体中与 互为同系物的结构简式:
互为同系物的结构简式:
您最近一年使用:0次
9 . 铁元素在细菌的作用下可发生如图所示的转化。下列说法中正确的是

| A.反硝化过程均属于氮的固定 |
| B.硝化过程中,含氮物质均发生还原反应 |
C. 将 将 转化为 转化为 的离子方程式为 的离子方程式为 |
D.在氨氧化细菌作用下,水体中的铵态氮和硝态氮可转移到大气中,该反应中每产生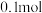 氮气时转移 氮气时转移 电子 电子 |
您最近一年使用:0次
10 . 下列叙述正确的是
A.某 溶液的 溶液的 ,将此溶液稀释10倍后,溶液的 ,将此溶液稀释10倍后,溶液的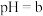 ,则 ,则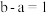 |
B.在滴有酚酞的氨水里,加入 至溶液恰好无色,则此时溶液的 至溶液恰好无色,则此时溶液的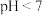 |
C.常温下,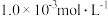 盐酸的 盐酸的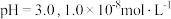 盐酸的 盐酸的 |
D.常温下,若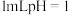 的盐酸与 的盐酸与 溶液混合后溶液的 溶液混合后溶液的 ,则 ,则 溶液的 溶液的 |
您最近一年使用:0次



