1 . 下列说法中正确的是
| A.电子云通常是用小黑点来表示电子的多少 |
| B.能量高的电子在离核近的区域运动,能量低的电子在离核远的区域运动 |
| C.处于最低能量的原子叫基态原子 |
| D.电子仅在激发态跃迁到基态时才会产生原子光谱 |
您最近一年使用:0次
2 . 空气湿度增大,水汽凝结就易形成雾,灰尘、硫酸、硝酸、有机碳氢化合物等颗粒物的浓度增大就易形成霾。下列说法不正确的是
| A.防雾霾口罩的原理与过滤类似,防雾霾效果好的口罩往往呼吸阻力较大 |
| B.PM2.5是直径小于或等于2.5微米的污染物颗粒,属于胶体粒子的直径范围 |
| C.汽车车灯在雾霾天照出“通路”的现象属于丁达尔效应 |
| D.可通过在燃煤烟囱上加装高压静电装置除去煤灰中的固体颗粒物 |
您最近一年使用:0次
3 . 宏观辨识与微观探析是化学学科核心素养之一、下列反应方程式正确的是
A.在溴的四氯化碳溶液中通入少量乙炔: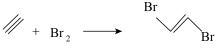 |
B.环丙烷在催化剂作用下与 反应生成丙烷: 反应生成丙烷: |
C.丙烯在一定条件下合成聚丙烯塑料: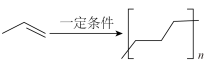 |
D.甲苯在光照条件下与氯气反应: |
您最近一年使用:0次
4 . 苯甲酸乙酯( )可用作食用香精。实验室以苯甲酸(熔点122.1℃)与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。制备方法如下:
)可用作食用香精。实验室以苯甲酸(熔点122.1℃)与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。制备方法如下:
步骤①:在烧瓶中加入苯甲酸12.2g、乙醇60.0mL、浓硫酸5.0mL、适量环己烷。按如图所示安装好装置,加热烧瓶,控制一定温度加热回流2h。
步骤②:将烧瓶中的反应液倒入盛有100.0mL水的烧杯中,加入Na2CO3至溶液呈中性。
步骤③:用分液漏斗分离出有机层,再用乙醚萃取水层中的残留产品,二者合并,加到图乙的蒸馏装置中,加入沸石与无水硫酸镁,加热蒸馏制得产品5.0mL。
回答下列问题:
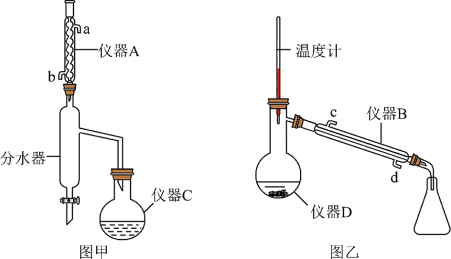
(1)仪器A的名称为___________ ,冷凝水的出水口为___________ (填“a”或“b”),本实验中浓硫酸的作用是___________ 。
(2)环己烷、乙醇和水可形成共沸物,沸点为62.1℃,仪器C的最佳加热方式为___________ 。
(3)写出制备苯甲酸乙酯反应的化学方程式:___________ 。
(4)图甲中分水器的“分水”原理是冷凝液在分水器中分层,上层有机层从支管处流回烧瓶,下层水层从分水器下口放出,反应结束的标志是___________ 。
(5)步骤②中加入Na2CO3的作用是___________ 。
(6)该实验中苯甲酸乙酯的产率为___________ %(保留三位有效数字)。
 )可用作食用香精。实验室以苯甲酸(熔点122.1℃)与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。制备方法如下:
)可用作食用香精。实验室以苯甲酸(熔点122.1℃)与乙醇为原料制备苯甲酸乙酯,制备装置如图所示(部分装置已省略)。制备方法如下:步骤①:在烧瓶中加入苯甲酸12.2g、乙醇60.0mL、浓硫酸5.0mL、适量环己烷。按如图所示安装好装置,加热烧瓶,控制一定温度加热回流2h。
步骤②:将烧瓶中的反应液倒入盛有100.0mL水的烧杯中,加入Na2CO3至溶液呈中性。
步骤③:用分液漏斗分离出有机层,再用乙醚萃取水层中的残留产品,二者合并,加到图乙的蒸馏装置中,加入沸石与无水硫酸镁,加热蒸馏制得产品5.0mL。
| 物质名称 | 苯甲酸 | 乙醇 | 环己烷 | 苯甲酸乙酯 |
| 相对分子质量 | 122 | 46 | 84 | 150 |
| 密度/g·cm-3 | 1.2659 | 0.7893 | 0.7318 | 1.0500 |
| 沸点/℃ | 249.2 | 78.3 | 80.8 | 212.61 |
(1)仪器A的名称为
(2)环己烷、乙醇和水可形成共沸物,沸点为62.1℃,仪器C的最佳加热方式为
(3)写出制备苯甲酸乙酯反应的化学方程式:
(4)图甲中分水器的“分水”原理是冷凝液在分水器中分层,上层有机层从支管处流回烧瓶,下层水层从分水器下口放出,反应结束的标志是
(5)步骤②中加入Na2CO3的作用是
(6)该实验中苯甲酸乙酯的产率为
您最近一年使用:0次
23-24高二下·黑龙江·期末
解题方法
5 . 下列化学用语表示不正确的是
A.CI4的空间填充模型: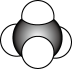 |
B.sp2杂化轨道模型: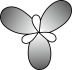 |
C.羟基的电子式: |
D.用原子轨道描述氯化氢分子中化学键的形成: |
您最近一年使用:0次
6 . 完成下列问题。___________ (填序号,下同);属于加成反应的是___________ ;属于氧化反应的是___________ 。
①乙烯使酸性高锰酸钾溶液褪色;②由乙烯制一氯乙烷;③乙醇在铜催化作用下制乙醛; ④乙酸和乙醇反应生成乙酸乙酯。
(1)现有各组物质:①O2和O3 ②CH2=CH-CH3和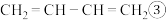
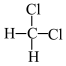 和
和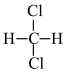
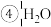 和
和 和
和 和质量数为238中子数为146的原子⑦
和质量数为238中子数为146的原子⑦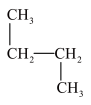 和
和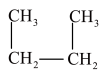 ⑧
⑧ 和CH3(CH2)3CH3。属于同种物质的是
和CH3(CH2)3CH3。属于同种物质的是
①乙烯使酸性高锰酸钾溶液褪色;②由乙烯制一氯乙烷;③乙醇在铜催化作用下制乙醛; ④乙酸和乙醇反应生成乙酸乙酯。
您最近一年使用:0次
名校
解题方法
7 . 下列说法错误的是
| A.相对分子质量为86,含有3个甲基的链状烷烃有2种 |
| B.分子式为C4H9Cl的有机物有4种 |
| C.分子式为C8H18,主链含有5个碳原子的链状烷烃有5种 |
| D.C5H12的一溴代物有8种 |
您最近一年使用:0次
名校
8 . 下列化学用语正确的是
A.丙烷分子的球棍模型: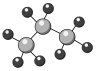 |
| B.乙醇分子式:C2 H5 OH |
C.一氯甲烷的电子式: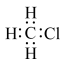 |
D.CCl4空间填充模型: |
您最近一年使用:0次
23-24高二下·黑龙江·期末
9 .  -月桂烯与
-月桂烯与 的加成反应的部分机理和反应势能变化如图所示。
的加成反应的部分机理和反应势能变化如图所示。
 -月桂烯与
-月桂烯与 的加成反应的部分机理和反应势能变化如图所示。
的加成反应的部分机理和反应势能变化如图所示。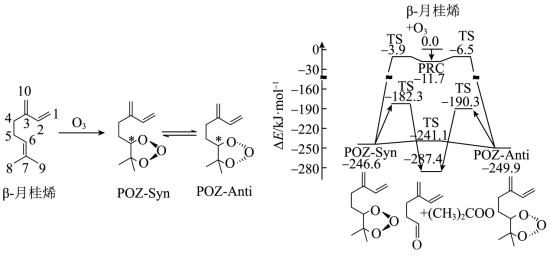
A. -月桂烯与丁基苯互为同分异构体 -月桂烯与丁基苯互为同分异构体 |
| B.POZ-Anti比POZ-Syn更稳定 |
C.升高温度,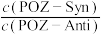 一定增大 一定增大 |
D. -月桂烯与 -月桂烯与 经历两种历程得到 经历两种历程得到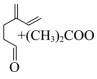 释放的能量相同 释放的能量相同 |
您最近一年使用:0次
10 . 亚稍酰氯(NOCl,熔点为-64.5℃,沸点为-5.5℃)是一种红褐色液体或黄色气体,遇水反应生成一种氢化物和两种氧化物,可用于合成清洁剂、触媒剂及中间体等。某学习小组在实验室中用Cl2和NO制备NOCl,请回答下列问题:
(1)原料气NO和Cl2的制备。________ 。实验室制备NO的反应的离子方程式为____________ 。
②实验室制备Cl2,可选择图中的装置_______ (填标号);制备并收集干燥的Cl2的装置连接顺序:_________ (按气流方向,用小写字母表示)。
(2)利用制得的NO和Cl2制备亚硝酰氯(NOCl),装置如图所示。_______ ,在装置I、Ⅱ选择通入气体时,应该先通入_______ ,原因是____________ 。
②装置Ⅳ的作用是___________ ;若无装置Ⅴ,则装置Ⅳ中NOCl可能发生反应的化学方程式为_______________ 。
③查阅资料知,王水是浓硝酸与浓盐酸的混合酸,一定条件下该混合酸可自身反应生成亚硝酰氯、氯气和水,该反应的化学方程式为______________ 。
(3)装置Ⅵ中倒置漏斗的作用为______ ,装置Ⅵ中发生反应的离子方程式为__________ 。
(1)原料气NO和Cl2的制备。
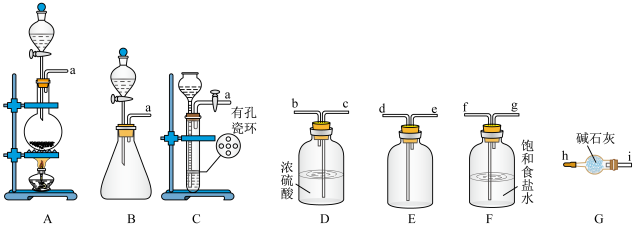
②实验室制备Cl2,可选择图中的装置
(2)利用制得的NO和Cl2制备亚硝酰氯(NOCl),装置如图所示。
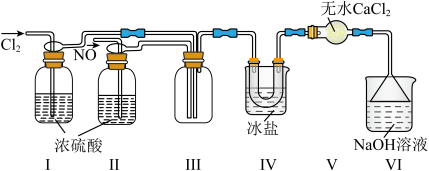
②装置Ⅳ的作用是
③查阅资料知,王水是浓硝酸与浓盐酸的混合酸,一定条件下该混合酸可自身反应生成亚硝酰氯、氯气和水,该反应的化学方程式为
(3)装置Ⅵ中倒置漏斗的作用为
您最近一年使用:0次



