解题方法
1 . 调环酸钙是一种植物生长调节剂,以下是一种合成路线(部分反应条件已简化)。
(1)顺丁烯二酸衍生物A的化学名称为_______ 。丙酮的结构简式为_______ 。
(2) 与
与 反应产生的强碱是
反应产生的强碱是_______ 。在这种碱的作用下,B中成键的碳原子是_______ 和_______ (选填数字编号)。
(3)由C转化为D的反应类型是_______ 。D中的含氧官能团名称为_______ 。
(4)由E生成调环酸钙的化学方程式为_______ 。
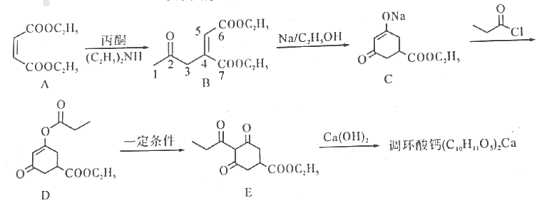
(5)写出符合下列条件的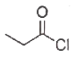 的同分异构体
的同分异构体_______ (任写两个)。
①有环氧结构;②核磁共振氢谱显示为三组峰;③不考虑立体异构。
(1)顺丁烯二酸衍生物A的化学名称为
(2)
 与
与 反应产生的强碱是
反应产生的强碱是(3)由C转化为D的反应类型是
(4)由E生成调环酸钙的化学方程式为
(5)写出符合下列条件的
 的同分异构体
的同分异构体①有环氧结构;②核磁共振氢谱显示为三组峰;③不考虑立体异构。
您最近一年使用:0次
解题方法
2 . 开发氢能源,并利用氢气对含硫物质脱硫处理,实现能源开发与环境保护。回答下列问题:
(1)天然气重整法是目前应用较为广泛的制氢方法。该工艺的基本反应如下。
第一步: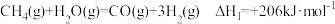 ;
;
第二步: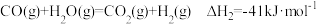 。
。
天然气重整法制氢总反应的热化学方程式为_______ 。
(2)研究用 还原
还原 废气。该反应分两步完成(未配平):
废气。该反应分两步完成(未配平): ;
; 。该过程中相关物质的浓度随时间的变化关系如图甲所示:
。该过程中相关物质的浓度随时间的变化关系如图甲所示: 脱除速率
脱除速率
_______ 。
②X为_______ (写化学式),X_______ (填“是”或“不是”)该还原过程的催化剂。
(3)研究用 对煤炭脱硫,发生反应:
对煤炭脱硫,发生反应: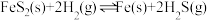
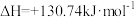 。
。
① 平衡转化率随压强增大而
平衡转化率随压强增大而_______ (填“增大”“减小”或“不变”)。
②上述反应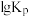 随
随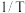 (T为热力学温度)变化关系如图乙所示。请判断表示正反应的
(T为热力学温度)变化关系如图乙所示。请判断表示正反应的 与
与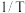 关系的是
关系的是_______ (填“A”或“B”)。 时该反应的平衡常数
时该反应的平衡常数 为
为_______ 。
④图乙中 时,向
时,向 密闭容器中加入
密闭容器中加入 ,达到平衡后,在t时刻再通入
,达到平衡后,在t时刻再通入 ,请在图丙中画出从t时刻到重新平衡时
,请在图丙中画出从t时刻到重新平衡时 体积分数的变化曲线
体积分数的变化曲线_______ 。
(1)天然气重整法是目前应用较为广泛的制氢方法。该工艺的基本反应如下。
第一步:
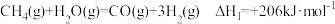 ;
;第二步:
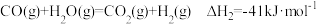 。
。天然气重整法制氢总反应的热化学方程式为
(2)研究用
 还原
还原 废气。该反应分两步完成(未配平):
废气。该反应分两步完成(未配平): ;
; 。该过程中相关物质的浓度随时间的变化关系如图甲所示:
。该过程中相关物质的浓度随时间的变化关系如图甲所示:
 脱除速率
脱除速率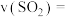
②X为
(3)研究用
 对煤炭脱硫,发生反应:
对煤炭脱硫,发生反应: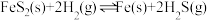
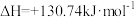 。
。①
 平衡转化率随压强增大而
平衡转化率随压强增大而②上述反应
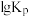 随
随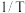 (T为热力学温度)变化关系如图乙所示。请判断表示正反应的
(T为热力学温度)变化关系如图乙所示。请判断表示正反应的 与
与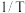 关系的是
关系的是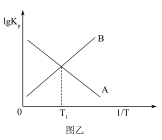
 时该反应的平衡常数
时该反应的平衡常数 为
为④图乙中
 时,向
时,向 密闭容器中加入
密闭容器中加入 ,达到平衡后,在t时刻再通入
,达到平衡后,在t时刻再通入 ,请在图丙中画出从t时刻到重新平衡时
,请在图丙中画出从t时刻到重新平衡时 体积分数的变化曲线
体积分数的变化曲线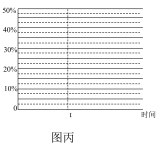
您最近一年使用:0次
解题方法
3 . 1-溴丙烷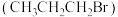 是一种重要的有机合成中间体,沸点为
是一种重要的有机合成中间体,沸点为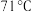 ,密度为
,密度为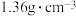 。实验室制备少量1-溴丙烷的主要步骤如下:
。实验室制备少量1-溴丙烷的主要步骤如下:
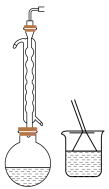
步骤1:在反应装置(如下图),尾部接气体吸收装置,用 溶液作吸收剂)的圆底烧瓶中加入搅拌磁子和
溶液作吸收剂)的圆底烧瓶中加入搅拌磁子和 水,在搅拌下缓慢加入
水,在搅拌下缓慢加入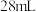 浓
浓 ,冷却至室温;再依次加入
,冷却至室温;再依次加入 正丙醇及
正丙醇及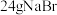 。
。 。
。
步骤3:待反应液冷却后,改为蒸馏装置(如下图),缓慢加热,直到无油状物馏出为止。
回答下列问题:
(1)步骤1缓慢加入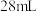 浓
浓 时使用的玻璃仪器有
时使用的玻璃仪器有_______ 。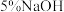 溶液用于吸收反应过程中产生的
溶液用于吸收反应过程中产生的_______ 。
(2)步骤2中回流不低于 的目的是
的目的是_____ 。回流温度太高会造成的不良后果有____ 。
(3)步骤3需将接受瓶置于冰水浴中,目的是_______ 。
(4)步骤4将馏出液转入分液漏斗,依次用等体积水、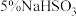 溶液、
溶液、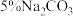 溶液、水洗涤。每次分液后须保留
溶液、水洗涤。每次分液后须保留_______ (填“上”或“下”)层液体。加入 溶液除去游离
溶液除去游离 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。“进一步提纯”的主要操作是_______ 。
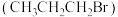 是一种重要的有机合成中间体,沸点为
是一种重要的有机合成中间体,沸点为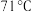 ,密度为
,密度为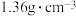 。实验室制备少量1-溴丙烷的主要步骤如下:
。实验室制备少量1-溴丙烷的主要步骤如下:步骤1:在反应装置(如下图),尾部接气体吸收装置,用
 溶液作吸收剂)的圆底烧瓶中加入搅拌磁子和
溶液作吸收剂)的圆底烧瓶中加入搅拌磁子和 水,在搅拌下缓慢加入
水,在搅拌下缓慢加入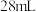 浓
浓 ,冷却至室温;再依次加入
,冷却至室温;再依次加入 正丙醇及
正丙醇及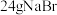 。
。
 。
。步骤3:待反应液冷却后,改为蒸馏装置(如下图),缓慢加热,直到无油状物馏出为止。
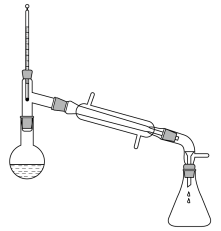
回答下列问题:
(1)步骤1缓慢加入
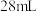 浓
浓 时使用的玻璃仪器有
时使用的玻璃仪器有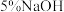 溶液用于吸收反应过程中产生的
溶液用于吸收反应过程中产生的(2)步骤2中回流不低于
 的目的是
的目的是(3)步骤3需将接受瓶置于冰水浴中,目的是
(4)步骤4将馏出液转入分液漏斗,依次用等体积水、
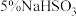 溶液、
溶液、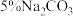 溶液、水洗涤。每次分液后须保留
溶液、水洗涤。每次分液后须保留 溶液除去游离
溶液除去游离 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
4 . 已知室温下,一元弱酸 溶液中除电离平衡外,还存在平衡
溶液中除电离平衡外,还存在平衡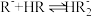
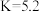 。下列说法一定正确的是
。下列说法一定正确的是
 溶液中除电离平衡外,还存在平衡
溶液中除电离平衡外,还存在平衡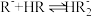
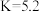 。下列说法一定正确的是
。下列说法一定正确的是A. 的 的 溶液稀释10倍后 溶液稀释10倍后 , ,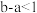 ,由此可以判定 ,由此可以判定 是弱酸 是弱酸 |
B. 的电离度随 的电离度随 浓度的增大而减小 浓度的增大而减小 |
C.向 溶液中加入一定量氨水,所得溶液 溶液中加入一定量氨水,所得溶液 时,存在 时,存在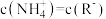 |
D.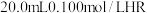 溶液中滴加 溶液中滴加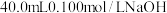 溶液时,存在 溶液时,存在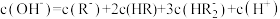 |
您最近一年使用:0次
解题方法
5 . 表示下列反应的离子方程式正确的是
A. 溶液中通入过量 溶液中通入过量 : :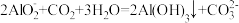 |
B. 用过量的稀硝酸处理得到 用过量的稀硝酸处理得到 |
C.钾肥 与氮肥 与氮肥 混用造成氮肥损失: 混用造成氮肥损失: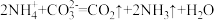 |
D. 使酸性 使酸性 溶液褪色: 溶液褪色: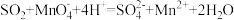 |
您最近一年使用:0次
6 . 一种药物中间体的结构如图所示。下列说法错误的是
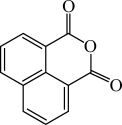
A.摩尔质量为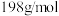 | B.该化合物所有碳原子共平面 |
| C.二氯代物有9种 | D.能使溴水和酸性 溶液褪色 溶液褪色 |
您最近一年使用:0次
解题方法
7 . 化学的社会价值之一是工业生产。下列叙述正确的是
| A.生产陶瓷需用石灰石作原料 | B.由加聚反应制得聚苯乙烯塑料 |
| C.工业上电解氧化钠制备金属钠 | D.合金的熔点一定比各组分的低 |
您最近一年使用:0次
8 . 银及其化合物在多种化学反应中都有重要作用。
(1)工业上常用 为催化剂氧化乙烯制备环氧乙烷(
为催化剂氧化乙烯制备环氧乙烷(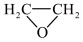 ,简称
,简称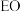 );
);
反应方程式为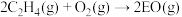 (反应a)
(反应a)
①银和铜位于同一族相邻周期,基态 原子的价层电子排布式为:
原子的价层电子排布式为:_____ 。
②已知: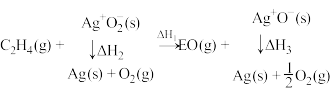
则反应a的
_____ 。
③关于反应a,下列说法正确的是_____ 。
A.加入银单质能降低该反应的活化能和焓变
B.因氧气并不直接与乙烯反应,故改变氧气浓度对反应无影响
C.移出部分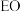 可使平衡正向移动,从而提高产率
可使平衡正向移动,从而提高产率
D.恒温恒容容器中,通入一定量的 气可增大压强,但乙烯的平衡转化率不变
气可增大压强,但乙烯的平衡转化率不变
(2)我国科学家报道了一种高效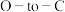 的替换反应,可在温和条件下将环氧化物快速转化为环丙烷结构。一种脱氧/环加成串联反应机理如图,其中的催化剂为
的替换反应,可在温和条件下将环氧化物快速转化为环丙烷结构。一种脱氧/环加成串联反应机理如图,其中的催化剂为_____ (填图中字母),反应物A和C消耗的物质的量之比为_____ 。(已知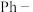 代表苯基)
代表苯基) 在
在 (A为M或N)溶液中的溶解状况。
(A为M或N)溶液中的溶解状况。
a.已知: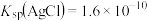 ;
;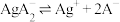
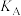
b.向 溶液中加入足量
溶液中加入足量 固体,发生反应:
固体,发生反应: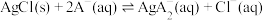 。
。
测得平衡时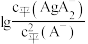 随
随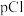 的变化曲线如图
的变化曲线如图 ,不考虑
,不考虑 的其它存在形式}。
的其它存在形式}。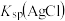
_____ 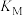 ,
,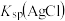
_____  。(填“>”“<”或“=”)
。(填“>”“<”或“=”)
②计算 在
在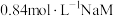 溶液中的溶解度(用物质的量浓度表示,写出计算过程,结果保留两位有效数字)
溶液中的溶解度(用物质的量浓度表示,写出计算过程,结果保留两位有效数字)_____ 。
(1)工业上常用
 为催化剂氧化乙烯制备环氧乙烷(
为催化剂氧化乙烯制备环氧乙烷( ,简称
,简称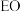 );
);反应方程式为
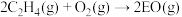 (反应a)
(反应a)①银和铜位于同一族相邻周期,基态
 原子的价层电子排布式为:
原子的价层电子排布式为:②已知:
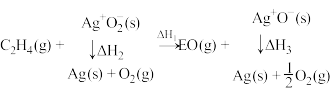
则反应a的

③关于反应a,下列说法正确的是
A.加入银单质能降低该反应的活化能和焓变
B.因氧气并不直接与乙烯反应,故改变氧气浓度对反应无影响
C.移出部分
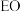 可使平衡正向移动,从而提高产率
可使平衡正向移动,从而提高产率D.恒温恒容容器中,通入一定量的
 气可增大压强,但乙烯的平衡转化率不变
气可增大压强,但乙烯的平衡转化率不变(2)我国科学家报道了一种高效
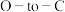 的替换反应,可在温和条件下将环氧化物快速转化为环丙烷结构。一种脱氧/环加成串联反应机理如图,其中的催化剂为
的替换反应,可在温和条件下将环氧化物快速转化为环丙烷结构。一种脱氧/环加成串联反应机理如图,其中的催化剂为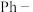 代表苯基)
代表苯基)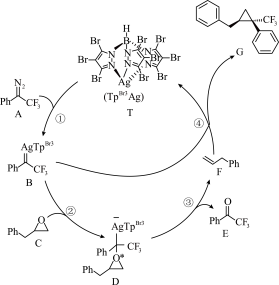
 在
在 (A为M或N)溶液中的溶解状况。
(A为M或N)溶液中的溶解状况。a.已知:
 ;
;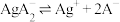
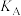
b.向
 溶液中加入足量
溶液中加入足量 固体,发生反应:
固体,发生反应: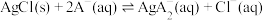 。
。测得平衡时
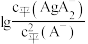 随
随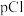 的变化曲线如图
的变化曲线如图 ,不考虑
,不考虑 的其它存在形式}。
的其它存在形式}。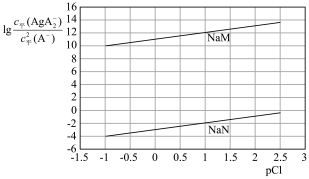
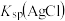
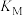 ,
,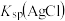
 。(填“>”“<”或“=”)
。(填“>”“<”或“=”)②计算
 在
在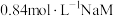 溶液中的溶解度(用物质的量浓度表示,写出计算过程,结果保留两位有效数字)
溶液中的溶解度(用物质的量浓度表示,写出计算过程,结果保留两位有效数字)
您最近一年使用:0次
解题方法
9 . 低温等离子体(NTP)技术可有效脱除烟气中的NO,其原理是在高压放电条件下,O2产生自由基(O·),自由基将NO氧化为NO2,再用Na2CO3溶液吸收,实验装置如下图所示。下列说法不正确 的是
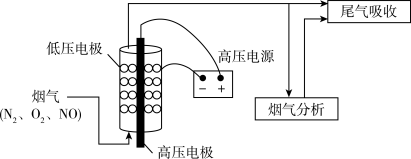
| A.氮元素既有被氧化的过程又有被还原的过程 |
| B.高压电源的功率越大,NO的脱除效果一定越好 |
| C.尾气吸收采用气、液逆流的方式可提高NO2脱除率 |
| D.单位时间内生成的自由基(O·)越多,越有利于NO的转化 |
您最近一年使用:0次
10 . 土壤中的硝酸盐可通过其中的硫化物分解,其主要化学反应原理是:5K2S+8KNO3+4H2O=4N2↑+5K2SO4+8KOH。下列表示相关微粒的化学用语正确的是
A.中子数为9的氮原子: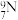 |
B.KOH的电子式: |
C.S2-的结构示意图: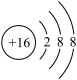 |
D.基态O的电子排布图: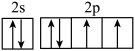 |
您最近一年使用:0次



