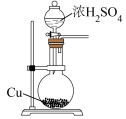
1 . 二氧化硫具有漂白性,工业上常用二氧化硫来漂白纸浆、毛、丝、草帽等。此外二氧化硫还能够抑制霉菌和细菌的滋生,可用作防腐剂。
Ⅰ.甲组同学拟利用 粉与浓硫酸反应制取
粉与浓硫酸反应制取 (标准状况下)
(标准状况下) 。实验方案设计如下:取
。实验方案设计如下:取 粉与
粉与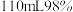 的浓硫酸(含
的浓硫酸(含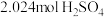 )混合,加热充分反应,待
)混合,加热充分反应,待 粉全部溶解后,干燥并收集气体。
粉全部溶解后,干燥并收集气体。
(1)写出 粉与浓硫酸反应制备
粉与浓硫酸反应制备 的化学方程式:
的化学方程式:__________________ 。
(2)乙组同学认为:按甲组同学实验方案无法达到实验目的,并且制得气体应该含有杂质,该杂质为_________ (填化学式)。
(3)为了检验甲组同学所制气体的成分,乙组同学按甲组同学的实验方案制备气体,并设计了如图所示的实验装置进行检验。(已知酸性高锰酸钾溶液及B中试剂均过量)
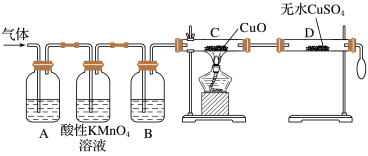
①A中试剂是品红溶液,作用是____________ 。
②B中所装试剂为____________ 。
③证明气体中混有杂质气体的实验现象是:________ 。
Ⅱ. 是常见的大气污染物,燃煤是产生
是常见的大气污染物,燃煤是产生 的主要原因。
的主要原因。
(4)工业上有多种方法可以减少 的排放。往煤中添加一些石灰石,可使燃煤过程中产生的
的排放。往煤中添加一些石灰石,可使燃煤过程中产生的 转化成硫酸钙,该反应的化学方程式是
转化成硫酸钙,该反应的化学方程式是___________ 。
(5)丙组同学认为 溶液可以做
溶液可以做 的吸收液,从而减少实验室
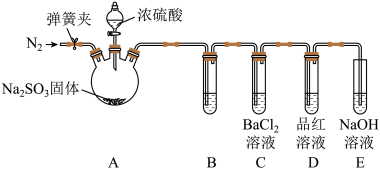
的吸收液,从而减少实验室 的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
已知: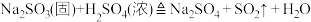
反应开始后,B、C试管中除了有气泡外,未见其他现象;D中红色褪去。通过乙组同学的实验,得出的结论是___________ 。
Ⅰ.甲组同学拟利用
 粉与浓硫酸反应制取
粉与浓硫酸反应制取 (标准状况下)
(标准状况下) 。实验方案设计如下:取
。实验方案设计如下:取 粉与
粉与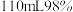 的浓硫酸(含
的浓硫酸(含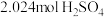 )混合,加热充分反应,待
)混合,加热充分反应,待 粉全部溶解后,干燥并收集气体。
粉全部溶解后,干燥并收集气体。(1)写出
 粉与浓硫酸反应制备
粉与浓硫酸反应制备 的化学方程式:
的化学方程式:(2)乙组同学认为:按甲组同学实验方案无法达到实验目的,并且制得气体应该含有杂质,该杂质为
(3)为了检验甲组同学所制气体的成分,乙组同学按甲组同学的实验方案制备气体,并设计了如图所示的实验装置进行检验。(已知酸性高锰酸钾溶液及B中试剂均过量)

①A中试剂是品红溶液,作用是
②B中所装试剂为
③证明气体中混有杂质气体的实验现象是:
Ⅱ.
 是常见的大气污染物,燃煤是产生
是常见的大气污染物,燃煤是产生 的主要原因。
的主要原因。(4)工业上有多种方法可以减少
 的排放。往煤中添加一些石灰石,可使燃煤过程中产生的
的排放。往煤中添加一些石灰石,可使燃煤过程中产生的 转化成硫酸钙,该反应的化学方程式是
转化成硫酸钙,该反应的化学方程式是(5)丙组同学认为
 溶液可以做
溶液可以做 的吸收液,从而减少实验室
的吸收液,从而减少实验室 的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
的排放。乙组同学认为丙组同学的假设不成立,为此乙组同学设计了如下实验(夹持装置和加热装置略,气密性已检验):
已知:
反应开始后,B、C试管中除了有气泡外,未见其他现象;D中红色褪去。通过乙组同学的实验,得出的结论是
您最近一年使用:0次
解题方法
2 . 某化学小组拟设计实验探究SO2与钙盐溶液的反应情况。
【文献资料】
①CaSO3是难溶于水、易溶于盐酸的白色固体;
②实验室用Na2SO3粉末和70%硫酸反应制备SO2;
③浓硫酸与水混合时放出大量的热,产生大量“酸雾”。
【设计实验】
实验Ⅰ:探究二氧化硫与氯化钙溶液的反应。
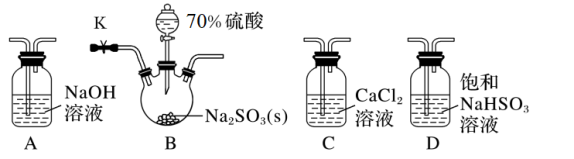
(1)若气体从左至右流动,选择装置并排序为___________ (填字母)。
(2)D装置的作用是___________ (用离子方程式表示)。
(3)连接装置进行实验,发现C装置中产生白色沉淀。
①甲同学对白色沉淀成分提出如下假设:
假设1:白色沉淀是CaSO3;
假设2:白色沉淀是CaSO4;
假设3:白色沉淀是CaSO4和CaSO3。
②乙同学设计实验证明白色沉淀是CaSO4,他的实验方法和现象是___________ 。
③丙同学认为C中生成硫酸钙的原因是装置内O2氧化了SO2。
排除装置内O2干扰采取的措施是:在启动B中反应之前,___________ (填实验步骤),重新实验,C中无明显现象,所以SO2和CaCl2溶液不反应。
实验Ⅱ:探究SO2和Ca(ClO)2溶液的反应。
丁同学仅将上述实验C装置中氯化钙溶液换成漂白精溶液,进行实验时产生了大量白色沉淀。
(4)化学反应有两种情况。
①若SO2过量,则发生的反应为Ca(ClO)2+2SO2+2H2O=CaSO4↓+2HCl+H2SO4;
②若SO2少量,则发生的反应为___________ 。
(5)为了探究C中SO2是否过量,戊同学取少量C中上层清液于试管中,加入下列物质可以达到实验目的的是___________ (填字母)。
a.NaHCO3溶液
b.品红溶液
c.AgNO3溶液
d.紫色石蕊溶液
【文献资料】
①CaSO3是难溶于水、易溶于盐酸的白色固体;
②实验室用Na2SO3粉末和70%硫酸反应制备SO2;
③浓硫酸与水混合时放出大量的热,产生大量“酸雾”。
【设计实验】
实验Ⅰ:探究二氧化硫与氯化钙溶液的反应。

(1)若气体从左至右流动,选择装置并排序为
(2)D装置的作用是
(3)连接装置进行实验,发现C装置中产生白色沉淀。
①甲同学对白色沉淀成分提出如下假设:
假设1:白色沉淀是CaSO3;
假设2:白色沉淀是CaSO4;
假设3:白色沉淀是CaSO4和CaSO3。
②乙同学设计实验证明白色沉淀是CaSO4,他的实验方法和现象是
③丙同学认为C中生成硫酸钙的原因是装置内O2氧化了SO2。
排除装置内O2干扰采取的措施是:在启动B中反应之前,
实验Ⅱ:探究SO2和Ca(ClO)2溶液的反应。
丁同学仅将上述实验C装置中氯化钙溶液换成漂白精溶液,进行实验时产生了大量白色沉淀。
(4)化学反应有两种情况。
①若SO2过量,则发生的反应为Ca(ClO)2+2SO2+2H2O=CaSO4↓+2HCl+H2SO4;
②若SO2少量,则发生的反应为
(5)为了探究C中SO2是否过量,戊同学取少量C中上层清液于试管中,加入下列物质可以达到实验目的的是
a.NaHCO3溶液
b.品红溶液
c.AgNO3溶液
d.紫色石蕊溶液
您最近一年使用:0次
名校
解题方法
3 . 如图所示实验装置不能达到实验目的的是
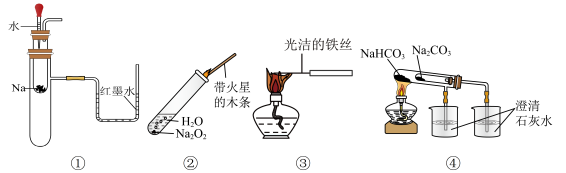
| A.利用装置①验证Na和水反应为放热反应 |
| B.利用装置②检验Na2O2与H2O反应有O2生成 |
| C.利用装置③观察纯碱的焰色试验的现象 |
| D.利用装置④比较Na2CO3和NaHCO3的热稳定性 |
您最近一年使用:0次
2024-01-05更新
|
146次组卷
|
3卷引用:河北省石家庄市第二十三中学2023-2024学年高一上学期期中考试化学试题
解题方法
4 . 用如图装置检验浓硫酸与木炭在加热条件下反应的产物 和
和 。
。不正确 的是
 和
和 。
。
A.①中现象说明产物中有 |
B.②中利用了 的氧化性 的氧化性 |
| C.将②③对调也能够达到实验目的 |
D.浓硫酸与木炭的反应: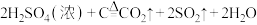 |
您最近一年使用:0次
名校
解题方法
5 . 实验室可用如图装置(略去部分夹持仪器)制取SO2并验证其性质。____ 。
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择______ (填代号)。
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为_______ 。
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案____ (填“Ⅰ”“Ⅱ”或“Ⅲ”);试管D中发生反应的离子方程式为_____ 。
(5)装置E的作用是______ 。装置F中为_____ 溶液。
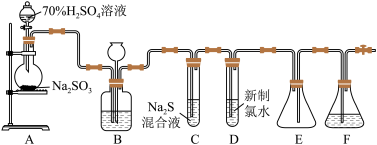
(2)装置B的作用之一是通过观察产生气泡的多少判断SO2生成的快慢,其中的液体最好选择
a.蒸馏水 b.饱和NaHCO3溶液 c.饱和NaHSO3溶液 d.饱和NaOH溶液
(3)C试管中的试剂可以验证二氧化硫的氧化性,现象为
(4)为验证二氧化硫的还原性,充分反应后,取试管D中的溶液分成三份,分别进行如下实验:
方案Ⅰ:向第一份溶液中加入AgNO3溶液,有白色沉淀生成;
方案Ⅱ:向第二份溶液中加入品红溶液,红色褪去;
方案Ⅲ:向第三份溶液中加入BaCl2溶液,产生白色沉淀。
上述方案中能达到实验目的的是方案
(5)装置E的作用是
您最近一年使用:0次
2024-04-04更新
|
125次组卷
|
2卷引用:天津市静海区第一中学2023-2024学年高一下学期3月月考化学试题
名校
6 . 下列实验装置或操作不能达到实验目的的是
甲 | 乙 | 丙 | 丁 |
|
|
|
|
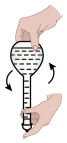
| A.图甲的操作为将定容后的溶液摇匀 |
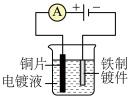
| B.以铜氨溶液为电镀液,用乙装置进行铁制镀件镀铜 |
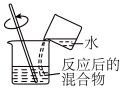
| C.用丙装置观察钠在空气中燃烧的现象 |
D.用丁装置检验浓硫酸与铜反应后的产物中是否含有 |
您最近一年使用:0次
2024-03-18更新
|
262次组卷
|
3卷引用:河北省保定市部分高中2023-2024学年高三下学期开学化学试题
名校
解题方法
7 . 下列实验装置或现象正确且能达到实验目的的是
| A | B | C | D |
|
|
|
|
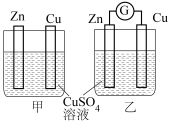
| 形成红色喷泉 | 甲中Zn片有红色固体析出,乙中铜片质量增加 | 制取得到干燥的NH3 | 制备SO2 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-12更新
|
79次组卷
|
2卷引用:黑龙江省牡丹江市第一高级中学2022-2023学年高一下学期5月期中考试化学试题
名校
8 . 下列实验设计可以达到实验目的的是
| 选项 | 实验目的 | 实验设计 |
| A | 证明金属活动性: | 将金属钠投入 溶液中 溶液中 |
| B | 检验待测液中含有 | 用玻璃棒蘸取待测液在无色火焰上灼烧,观察现象 |
| C | 制备 胶体 胶体 | 将5~6滴饱和 溶液滴加到煮沸的蒸馏水中,继续煮沸至液体呈红褐色为止 溶液滴加到煮沸的蒸馏水中,继续煮沸至液体呈红褐色为止 |
| D | 探究钠在空气中燃烧产物为 | 将燃烧后的物质置于水中,滴入无色酚酞溶液,一段时间后,溶液为红色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-08-20更新
|
450次组卷
|
4卷引用:江西省赣州教育发展联盟2022-2023学年高一上学期12月月考化学试题
名校
解题方法
9 . 下列实验方案能达到目的的是
实验目的 | 实验方案 | |
| A | 证明稀硝酸的氧化性比浓硝酸强 | 常温下将铁片分别插入稀硝酸和浓硝酸中,前者产生无色气体,后者无明显现象 |
| B | 比较铁和铜的活泼性 | 将铜丝放入氯化铁溶液中,观察溶液的颜色变化 |
| C | 制备氢氧化亚铁 | 把装有氢氧化钠溶液的长胶头滴管伸入硫酸亚铁溶液中滴加液体 |
| D | 检测新制氯水的pH | 用玻璃棒取少量样品滴到干燥pH试纸上,待显色完全后与标准比色卡对比 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
10 . 已知X、Y、Z、R均为元素周期表中的短周期主族元素,它们具有如下特征:
(1)Z在元素周期表的位置_______ 。
(2)R的+1价含氧酸的电子式_______ 。
(3)Y的简单氢化物不能用Y的最高价氧化物对应水化物的浓溶液干燥的原因是_______ 。(用方程式表达)
(4)某同学设计了如下装置来探究X、Y、Z元素的非金属性强弱。

①试管D中盛放_______ 溶液。
②酸性KMnO4溶液的作用是_______ 。D中实验现象为_______ 。
③另一同学从实验目的上分析认为该实验设计部分正确,即该实验能够得出的结论仅为_______ 。
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 最高正价和最低负价代数和为4 |
| Z | 最高价氧化物对应水化物难溶于水,是一种很弱的酸 |
| R | M层上有7个电子 |
(2)R的+1价含氧酸的电子式
(3)Y的简单氢化物不能用Y的最高价氧化物对应水化物的浓溶液干燥的原因是
(4)某同学设计了如下装置来探究X、Y、Z元素的非金属性强弱。

①试管D中盛放
②酸性KMnO4溶液的作用是
③另一同学从实验目的上分析认为该实验设计部分正确,即该实验能够得出的结论仅为
您最近一年使用:0次