2024高三·全国·专题练习
解题方法
1 . 化学需氧量(COD)是指用强氧化剂将1 L废水中的还原性物质氧化为二氧化碳和水所消耗的氧化剂的量,并换算成以O2为氧化剂时所消耗O2的质量。水体COD值常作为水体中有机污染物相对含量的综合指标之一,Fenton(Fe2+/H2O2)法能产生Fe3+和具有强氧化性的羟基自由基(·OH)引发一系列链式反应,被广泛应用于有机废水的治理。
(1)羟基自由基(·OH)的电子式为___________ 。
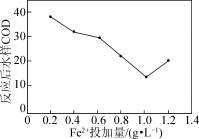
(2)分别取初始pH=4、COD=80的废水200 mL,加入200 mL H2O2,改变起始投加FeSO4·7H2O的量,反应相同时间。测得反应后水样COD随Fe2+投加量的关系如图所示。当Fe2+投加量超过1 g·L-1时,反应后水样COD不降反升的原因可能是___________ 。 )的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O
)的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O 产生SO
产生SO 具有很好的效果。S2O
具有很好的效果。S2O 结构如图所示。
结构如图所示。 的使用范围更广。SO
的使用范围更广。SO 在强碱性条件下反应生成·OH,写出该反应的离子方程式:
在强碱性条件下反应生成·OH,写出该反应的离子方程式:___________ 。
② 一种制取Mn3O4—石墨烯纳米复合材料的物种转化关系可表示如下(GO表示石墨烯):___________ mol。
③利用该复合材料催化活化S2O 并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为
并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为___________ 。
(1)羟基自由基(·OH)的电子式为
(2)分别取初始pH=4、COD=80的废水200 mL,加入200 mL H2O2,改变起始投加FeSO4·7H2O的量,反应相同时间。测得反应后水样COD随Fe2+投加量的关系如图所示。当Fe2+投加量超过1 g·L-1时,反应后水样COD不降反升的原因可能是
 )的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O
)的氧化技术引起关注。研究发现,一种Mn3O4石墨烯纳米复合材料对催化活化S2O 产生SO
产生SO 具有很好的效果。S2O
具有很好的效果。S2O 结构如图所示。
结构如图所示。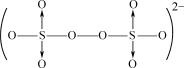
 的使用范围更广。SO
的使用范围更广。SO 在强碱性条件下反应生成·OH,写出该反应的离子方程式:
在强碱性条件下反应生成·OH,写出该反应的离子方程式:② 一种制取Mn3O4—石墨烯纳米复合材料的物种转化关系可表示如下(GO表示石墨烯):
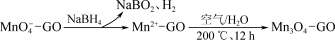
③利用该复合材料催化活化S2O
 并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为
并去除废水中有机污染物的可能反应机理如图所示。该机理可描述为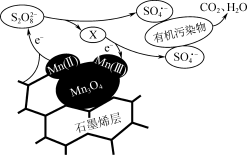
您最近一年使用:0次
22-23高二下·广东佛山·期中
解题方法
2 . 氯化亚砜(SOCl2)是一种很重要的化学试剂。下列关于氯化亚砜分子的说法正确的是
| A.为极性键形成的非极性分子 | B.立体构型为平面三角形 |
C.中心S原子采取 杂化 杂化 | D.氯化亚砜的结构式为: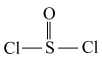 |
您最近一年使用:0次
2023·江苏南通·三模
3 . 常温下,肼 的水溶液显碱性,存在如下平衡:
的水溶液显碱性,存在如下平衡: ;
;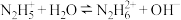 。平衡时溶液中含氮微粒的分布分数
。平衡时溶液中含氮微粒的分布分数 与溶液
与溶液 的关系如图所示。向
的关系如图所示。向 的水溶液中逐滴滴加
的水溶液中逐滴滴加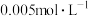 的稀硫酸,下列说法正确的是
的稀硫酸,下列说法正确的是

 的水溶液显碱性,存在如下平衡:
的水溶液显碱性,存在如下平衡: ;
;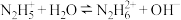 。平衡时溶液中含氮微粒的分布分数
。平衡时溶液中含氮微粒的分布分数 与溶液
与溶液 的关系如图所示。向
的关系如图所示。向 的水溶液中逐滴滴加
的水溶液中逐滴滴加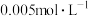 的稀硫酸,下列说法正确的是
的稀硫酸,下列说法正确的是
A. 的电子式: 的电子式: |
B. 的平衡常数为 的平衡常数为 |
C.当加入5.00mL稀硫酸时,溶液中: |
D.当加入10.00mL稀硫酸时,溶液中: |
您最近一年使用:0次
2023-05-07更新
|
1078次组卷
|
4卷引用:专题16 水溶液中的离子平衡
2023·全国·模拟预测
4 . “2022年中国十大科技”之一--------谢和平团队开创全新原理海水无淡化原位直接电解制氢。该技术以疏水多孔聚四氟乙烯透气膜作为气路界面,以氢氧化钾溶液作为电解质溶液,将分子扩散、界面相平衡与电化学结合,破解科技界难题。下列说法正确的是
| A.聚四氟乙烯可通过乙烯为单体制备,其孔径限制海水离子通过 |
B.KOH的电子式: ,其浓度不影响制氢速率 ,其浓度不影响制氢速率 |
| C.该技术破解了析氯反应、钙镁沉积、催化剂失活等难题,有极大推广价值 |
| D.有效控制水蒸气的迁移速率大于水的电解速率时,可实现海水稳定制氢 |
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
5 . Na与S反应可以生成多种产物:Na2S,Na2S2……Na2S5。已知Na2S2的电子式为 ,则S
,则S 的电子式为
的电子式为_______ 。
 ,则S
,则S 的电子式为
的电子式为
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
6 . 化合物CuAl2Cl8的-1价阴离子与CH4具有相同的空间结构,写出该阴离子的电子式_______ 。
您最近一年使用:0次
2023高三·全国·专题练习
解题方法
7 . 化合物A是一种不稳定的物质,它的分子组成可用OxFy表示,10mLA气体能分解生成15mLO2和10mLF2(同温同压下)。
(1)A的分子式_______ ;
(2)已知A分子中X个氧原子是…-O-O-O-…链状排列,都达到8电子的稳定结构,则A分子的结构式是_______ 。
(1)A的分子式
(2)已知A分子中X个氧原子是…-O-O-O-…链状排列,都达到8电子的稳定结构,则A分子的结构式是
您最近一年使用:0次
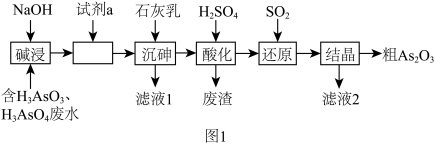
8 . 某含砷( )的有毒工业废水经如图1所示流程转化为粗
)的有毒工业废水经如图1所示流程转化为粗 。已知:亚砷酸钙微溶于水,砷酸钙难溶于水。
。已知:亚砷酸钙微溶于水,砷酸钙难溶于水。
(1)砷是氮的同族元素,且比氮多2个电子层,则 的电子式为
的电子式为____________ 。
(2)“碱浸”的目的是将废水中的 和
和 转化为盐,
转化为盐, 转化为
转化为 的离子方程式为
的离子方程式为____________________________________ 。
(3)试剂a可选用______ ;加入试剂a的目的是____________________________________ 。
(4)“沉砷”是将砷元素转化为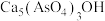 沉淀,发生的主要反应有
沉淀,发生的主要反应有
①
②
资料表明:“沉砷”的最佳温度是 ,温度高于
,温度高于 时,随温度升高,沉淀率减小,从平衡移动角度分析其原因是
时,随温度升高,沉淀率减小,从平衡移动角度分析其原因是________________________________________________ 。
(5)流程中先“沉砷”后“酸化”的优点是________________________________________________ 。
(6)通过对 溶液进行加热,再过滤可制得粗
溶液进行加热,再过滤可制得粗 。
。 在不同温度和不同浓度的硫酸溶液中的溶解度(S)曲线如图2所示。为提高粗
在不同温度和不同浓度的硫酸溶液中的溶解度(S)曲线如图2所示。为提高粗 的沉淀率,“结晶”过程应控制的最佳条件是
的沉淀率,“结晶”过程应控制的最佳条件是____ 。

(7)从绿色化学和综合利用的角度考虑,滤液2需要处理,可将滤液2返回“________ ”环节循环使用。
 )的有毒工业废水经如图1所示流程转化为粗
)的有毒工业废水经如图1所示流程转化为粗 。已知:亚砷酸钙微溶于水,砷酸钙难溶于水。
。已知:亚砷酸钙微溶于水,砷酸钙难溶于水。
(1)砷是氮的同族元素,且比氮多2个电子层,则
 的电子式为
的电子式为(2)“碱浸”的目的是将废水中的
 和
和 转化为盐,
转化为盐, 转化为
转化为 的离子方程式为
的离子方程式为(3)试剂a可选用
(4)“沉砷”是将砷元素转化为
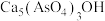 沉淀,发生的主要反应有
沉淀,发生的主要反应有①

②

资料表明:“沉砷”的最佳温度是
 ,温度高于
,温度高于 时,随温度升高,沉淀率减小,从平衡移动角度分析其原因是
时,随温度升高,沉淀率减小,从平衡移动角度分析其原因是(5)流程中先“沉砷”后“酸化”的优点是
(6)通过对
 溶液进行加热,再过滤可制得粗
溶液进行加热,再过滤可制得粗 。
。 在不同温度和不同浓度的硫酸溶液中的溶解度(S)曲线如图2所示。为提高粗
在不同温度和不同浓度的硫酸溶液中的溶解度(S)曲线如图2所示。为提高粗 的沉淀率,“结晶”过程应控制的最佳条件是
的沉淀率,“结晶”过程应控制的最佳条件是
(7)从绿色化学和综合利用的角度考虑,滤液2需要处理,可将滤液2返回“
您最近一年使用:0次
名校
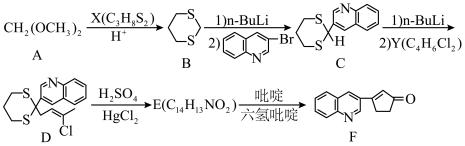
9 . 有机工业制备的重要的中间体F的合成工艺流程如图:
(1)X的结构简式为______ 。E的结构简式为______ 。
(2)下列说法正确的是______ 。
(3)根据题中信息,写出Y在NaOH溶液中反应化学反应方程式______ 。
(4)写出所有符合下列条件的化合物C的同分异构体:______ 。
①结构中含有苯环,无其他环状结构;苯环上的一元取代物只有一种
②IR光谱显示结构中含“-CN”和“C=S”结构;
③1H-NMR谱显示结构中有3种化学环境的氢原子,个数比为1:6:6。
(5)请以化合物CH2=CH2、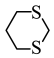 为原料,设计化合物
为原料,设计化合物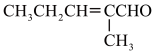 的合成路线:
的合成路线:______ (无机试剂任选)。
已知:R1COR2+RCH2COR′
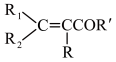
(1)X的结构简式为
(2)下列说法正确的是
| A.-SH的性质类似于-OH,化合物X一定条件下可发生缩聚反应 |
| B.化合物C中有一个手性C原子,所有原子可以在同一平面上 |
| C.化合物F可发生还原反应、加聚反应、水解反应 |
D.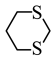 的结构中,4个C和2个S的杂化方式均相同 的结构中,4个C和2个S的杂化方式均相同 |
(4)写出所有符合下列条件的化合物C的同分异构体:
①结构中含有苯环,无其他环状结构;苯环上的一元取代物只有一种
②IR光谱显示结构中含“-CN”和“C=S”结构;
③1H-NMR谱显示结构中有3种化学环境的氢原子,个数比为1:6:6。
(5)请以化合物CH2=CH2、
 为原料,设计化合物
为原料,设计化合物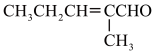 的合成路线:
的合成路线:
您最近一年使用:0次
2023-01-02更新
|
1687次组卷
|
5卷引用:浙江省杭州学军中学2022-2023学年高三上学期模拟考试化学试题
22-23高三上·浙江·阶段练习
解题方法
10 . 金属镍及其化合物在合成材料以及催化剂等方面应用广泛。请回答下列问题:
(1)基态Ni原子的原子结构示意图为_____ 。
(2)NiO、FeO晶体类型与晶胞与NaCl相同,则NiO晶胞结构中Ni2+的配位数为_____ ;又知Ni2+、Fe2+的离子半径分别为69pm、78pm,则NiO熔点_____ FeO(填“>”、“<”、“=”)。
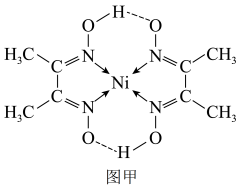
(3)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图甲所示,则该沉淀中Ni2+的配位数为_____ ;元素H、C、N、O、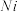 电负性由大到小的顺序为
电负性由大到小的顺序为____ 。
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图及晶胞参数如图乙所示。该晶体的化学式为_____ ;晶体密度为_____ g•cm-3(列出含a、b、NA计算表达式,NA表示阿伏加德罗常数的值)。

(1)基态Ni原子的原子结构示意图为
(2)NiO、FeO晶体类型与晶胞与NaCl相同,则NiO晶胞结构中Ni2+的配位数为
(3)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结构如图甲所示,则该沉淀中Ni2+的配位数为
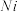 电负性由大到小的顺序为
电负性由大到小的顺序为
(4)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图及晶胞参数如图乙所示。该晶体的化学式为

您最近一年使用:0次



