解题方法
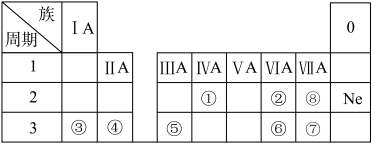
1 . 下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素,请根据要求回答问题:
①___________ ;⑤___________ ;⑦___________ ;⑧___________ 。
(2)②和③元素所组成的化合物中可做供氧剂的是___________ (写化学式)。
(3)⑥元素的原子结构示意图为___________ 。②元素的原子结构示意图为___________ 。
(4)①元素的氧化物中是酸性氧化物的是___________ (写化学式)。
①
(2)②和③元素所组成的化合物中可做供氧剂的是
(3)⑥元素的原子结构示意图为
(4)①元素的氧化物中是酸性氧化物的是
您最近一年使用:0次
名校
解题方法
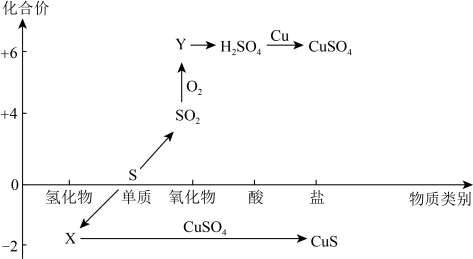
2 . 硫及其化合物的“价-类”二维图如下图所示,回答下列问题:___________ ,Y的化学式是___________ 。
(2)X与 反应的化学方程式是
反应的化学方程式是___________ ,氧化剂是___________ (填化学式)。
(3)
___________ (填“是”、或“不是”)电解质,检验 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入___________ ,无明显现象,再加入___________ 溶液,若产生白色沉淀,则溶液中含有 。
。
(2)X与
 反应的化学方程式是
反应的化学方程式是(3)

 时,取少量待测液于试管中,先加入
时,取少量待测液于试管中,先加入 。
。
您最近一年使用:0次
名校
解题方法
3 . 完成下列问题。
(1)某短周期元素组成的分子的球棍模型如图所示。已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连。下列有关说法错误的是_______(填字母)。
(2)若上述模型中Y原子最外层达到2电子稳定结构且其相对分子质量与O2相同,则该物质的分子式为_______ ,它与P2H4常温下均为气体,但比P2H4易液化,常用作火箭燃料,其主要原因是_______ 。
(1)某短周期元素组成的分子的球棍模型如图所示。已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连。下列有关说法错误的是_______(填字母)。
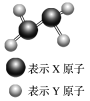
| A.X原子可能为ⅤA族元素 |
| B.Y原子一定为ⅠA族元素 |
| C.该分子中,既含极性键,又含非极性键 |
| D.从圆球的大小分析,该分子可能为N2F4 |
您最近一年使用:0次
名校
4 . 表格为门捷列夫元素周期表的一部分,其中的编号代表对应的元素。用元素符号回答下列问题:
(1)基态F原子有___________ 种运动状态的电子。
(2)元素③⑪电负性较大的是___________ ﹔Se的原子结构示意图为___________ 。
(3)元素铬的基态原子的价电子排布式为:___________ 。
(4)Cu基态原子中,能量最高的电子占据的原子轨道的形状为___________ 。
(5)该表格中电负性最大的元素与第一电离能最小的元素形成的化合物的电子式为___________ 。
(6)②③的简单气态氢化物中较稳定的是___________ (填化学式),元素⑥⑦的最高价氧化物的水化物相互反应的离子方程式为___________ 。

(1)基态F原子有
(2)元素③⑪电负性较大的是
(3)元素铬的基态原子的价电子排布式为:
(4)Cu基态原子中,能量最高的电子占据的原子轨道的形状为
(5)该表格中电负性最大的元素与第一电离能最小的元素形成的化合物的电子式为
(6)②③的简单气态氢化物中较稳定的是
您最近一年使用:0次
5 . 回答下列问题:
(1)①Fe3O4的俗称为______ ;②HCN的电子式______ 。
(2)①工业制漂白粉的化学方程式______ 。
②Al2O3与NaOH溶液反应的离子方程式______ 。
(1)①Fe3O4的俗称为
(2)①工业制漂白粉的化学方程式
②Al2O3与NaOH溶液反应的离子方程式
您最近一年使用:0次
解题方法
6 . 按要求回答下列问题:
(1)键线式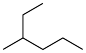 的系统命名为
的系统命名为___________ ;
(2)2-甲基-1-丁烯的结构简式___________ ;
(3)相对分子质量为72且一氯代物只有一种的烷烃的结构简式___________ ;
(4)聚丙烯的结构简式___________ ;
(5)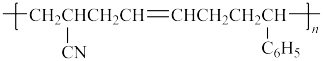 ,该物质属
,该物质属___________ (填“纯净物”或“混合物”),单体为:___________ ;
(6) 的有效利用可以缓解温室效应和能源短缺问题。我国科研人员在
的有效利用可以缓解温室效应和能源短缺问题。我国科研人员在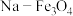 和
和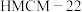 的表面将
的表面将 转化为烷烃,其过程如图所示:
转化为烷烃,其过程如图所示:___________ ;
②推测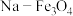 和
和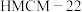 在反应中的作用为
在反应中的作用为___________ ;
③写出X的所有同分异构体的结构简式:___________ ;
④下列关于X和Y的说法正确的是___________ (填序号)。
A.最简式相同 B.都有4种一氯代物(不考虑立体异构)
C.都能使酸性 溶液褪色 D.互为同分异构体
溶液褪色 D.互为同分异构体
⑤在同温同压下,蒸气密度是 的15倍的气态烷烃M的结构简式为
的15倍的气态烷烃M的结构简式为___________ ,其与氯气反应生成一氯代烃的化学方程式___________ 。
(1)键线式
 的系统命名为
的系统命名为(2)2-甲基-1-丁烯的结构简式
(3)相对分子质量为72且一氯代物只有一种的烷烃的结构简式
(4)聚丙烯的结构简式
(5)
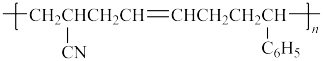 ,该物质属
,该物质属(6)
 的有效利用可以缓解温室效应和能源短缺问题。我国科研人员在
的有效利用可以缓解温室效应和能源短缺问题。我国科研人员在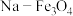 和
和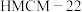 的表面将
的表面将 转化为烷烃,其过程如图所示:
转化为烷烃,其过程如图所示: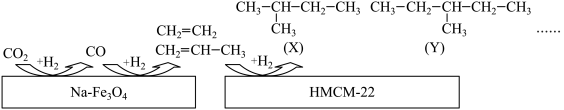
②推测
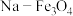 和
和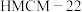 在反应中的作用为
在反应中的作用为③写出X的所有同分异构体的结构简式:
④下列关于X和Y的说法正确的是
A.最简式相同 B.都有4种一氯代物(不考虑立体异构)
C.都能使酸性
 溶液褪色 D.互为同分异构体
溶液褪色 D.互为同分异构体⑤在同温同压下,蒸气密度是
 的15倍的气态烷烃M的结构简式为
的15倍的气态烷烃M的结构简式为
您最近一年使用:0次
7 . 已知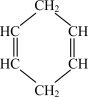 可用键线式表示为
可用键线式表示为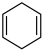 。现有某化合物W的分子结构为
。现有某化合物W的分子结构为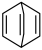 。
。
(1)W的分子式为___________________________ 。
(2)W的一氯代物有_________ 种。
(3)写出W的芳香族同分异构体(只含一个环)的结构简式:_______________ 。
(4)W属于_________ (填字母)。
a.芳香烃 b.脂环烃 c.不饱和烃 d.炔烃
(5)某有机物经分析知其分子中共含有3个 、2个
、2个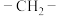 和1个
和1个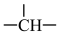 ,则它可能的结构简式和名称分别为
,则它可能的结构简式和名称分别为________________________________ 。
(6)2,4,6-三甲基-5-乙基辛烷分子中含有_________ 个 原子团。
原子团。
(7)分子中有六个甲基,而一卤代物只有一种的烷烃的化学式是_________ ,结构简式是____ 。
(8)有机物的结构简式可用“键线式”表示,如异丁烷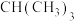 的结构简式用键线表示为
的结构简式用键线表示为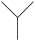 。则
。则 表示的有机物的系统名称为
表示的有机物的系统名称为__________________ 。
 可用键线式表示为
可用键线式表示为 。现有某化合物W的分子结构为
。现有某化合物W的分子结构为 。
。(1)W的分子式为
(2)W的一氯代物有
(3)写出W的芳香族同分异构体(只含一个环)的结构简式:
(4)W属于
a.芳香烃 b.脂环烃 c.不饱和烃 d.炔烃
(5)某有机物经分析知其分子中共含有3个
 、2个
、2个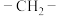 和1个
和1个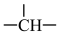 ,则它可能的结构简式和名称分别为
,则它可能的结构简式和名称分别为(6)2,4,6-三甲基-5-乙基辛烷分子中含有
 原子团。
原子团。(7)分子中有六个甲基,而一卤代物只有一种的烷烃的化学式是
(8)有机物的结构简式可用“键线式”表示,如异丁烷
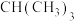 的结构简式用键线表示为
的结构简式用键线表示为 。则
。则 表示的有机物的系统名称为
表示的有机物的系统名称为
您最近一年使用:0次
8 . 磷酸亚铁锂(LiFePO4)和锰酸锂(LiMn2O4)均可用作锂电池的正极材料。回答下列问题:
(1)在周期表中,与Li化学性质最相似的邻族元素是___________ (填元素符号)。基态O原子的价电子排布图为___________ 。基态P原子电子占据最高能级的电子云在空间有___________ 个伸展方向。
(2)写出H2O2的电子式___________ 。
(3)原子核外电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为___________ 。
(4)第三周期元素中,第一电离能介于A1和P之间的元素有___________ 种。
(5)Fe元素位于周期表的___________ 区。已知:I3(Mn)=3248kJ/mol,I3(Fe)=2957kJ/mol。第三电离能I3(Mn)>I3(Fe),其主要原因是___________ 。
(1)在周期表中,与Li化学性质最相似的邻族元素是
(2)写出H2O2的电子式
(3)原子核外电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数。基态Mn原子的价电子自旋磁量子数的代数和为(4)第三周期元素中,第一电离能介于A1和P之间的元素有
(5)Fe元素位于周期表的
您最近一年使用:0次
9 . 氰化钾是一种剧毒的物质,贮存和使用时必须注意安全。已知: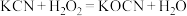 。回答下列问题:
。回答下列问题:
(1)KCN的电子式为______ 。
(2)KOCN中K、O、C、N的电负性由大到小的顺序为______ (用元素符号表示),1mol 中含有的
中含有的 键数目为
键数目为______ , 的空间结构为
的空间结构为______ 。
(3)① 与
与 相似,分子中的共价键类型为
相似,分子中的共价键类型为______ (填“ 键”或“
键”或“ 键”),
键”), 在水中的溶解度比
在水中的溶解度比 的小,其主要原因为
的小,其主要原因为______ 。
② 和
和 结构如图所示。
结构如图所示。

请说明 中
中 略大于
略大于 的原因:
的原因:______ 。
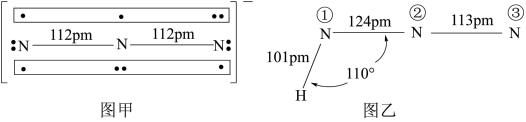
(4) 中
中 结构如图甲,
结构如图甲, 中存在两个大
中存在两个大 键可用符号
键可用符号 (3个原子共享4个电子)表示,一个
(3个原子共享4个电子)表示,一个 中键合电子(形成化学键的电子)总数为
中键合电子(形成化学键的电子)总数为______ 。叠氮酸( )结构如图乙,分子中②号N原子的杂化方式为
)结构如图乙,分子中②号N原子的杂化方式为______ ,叠氮酸( )在常温下是液体,沸点相对较高,为308.8K,主要原因是
)在常温下是液体,沸点相对较高,为308.8K,主要原因是______ 。
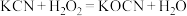 。回答下列问题:
。回答下列问题:(1)KCN的电子式为
(2)KOCN中K、O、C、N的电负性由大到小的顺序为
 中含有的
中含有的 键数目为
键数目为 的空间结构为
的空间结构为(3)①
 与
与 相似,分子中的共价键类型为
相似,分子中的共价键类型为 键”或“
键”或“ 键”),
键”), 在水中的溶解度比
在水中的溶解度比 的小,其主要原因为
的小,其主要原因为②
 和
和 结构如图所示。
结构如图所示。
请说明
 中
中 略大于
略大于 的原因:
的原因:(4)
 中
中 结构如图甲,
结构如图甲, 中存在两个大
中存在两个大 键可用符号
键可用符号 (3个原子共享4个电子)表示,一个
(3个原子共享4个电子)表示,一个 中键合电子(形成化学键的电子)总数为
中键合电子(形成化学键的电子)总数为 )结构如图乙,分子中②号N原子的杂化方式为
)结构如图乙,分子中②号N原子的杂化方式为 )在常温下是液体,沸点相对较高,为308.8K,主要原因是
)在常温下是液体,沸点相对较高,为308.8K,主要原因是
您最近一年使用:0次
名校
解题方法
10 . Ⅰ硒(Se)是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在自然界中稀少而分散,常从精炼铜的废渣中提取而得。
(1)Se在元素周期表中位置表示为__________ 。
(2)写出 的电子式:
的电子式:__________ , 的结构式:
的结构式:__________ 。
(3)用电子式表示 的形成过程:
的形成过程:__________ 。
Ⅱ某学习小组探究B及其化合物的性质。
(4)元素周期表中虚线相连的元素的性质具有一定的相似性,即对角线法则。
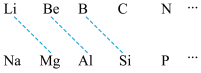
B最高价氧化物的化学式为__________ ,与氢氧化钠溶液反应的化学方程式为__________ 。
(5)某科研团队研究发现硼氢化钠( )在催化剂表面与水反应可生成
)在催化剂表面与水反应可生成 。
。
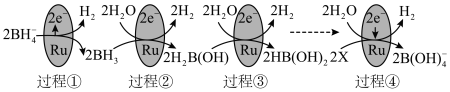
①上图中X的化学式为__________ 。
②图中反应的总化学方程式为__________ 。
③__________  的还原能力与标准状况下
的还原能力与标准状况下 的还原能力相当(还原能力即生成
的还原能力相当(还原能力即生成 失去电子的量)。
失去电子的量)。
(1)Se在元素周期表中位置表示为
(2)写出
 的电子式:
的电子式: 的结构式:
的结构式:(3)用电子式表示
 的形成过程:
的形成过程:Ⅱ某学习小组探究B及其化合物的性质。
(4)元素周期表中虚线相连的元素的性质具有一定的相似性,即对角线法则。

B最高价氧化物的化学式为
(5)某科研团队研究发现硼氢化钠(
 )在催化剂表面与水反应可生成
)在催化剂表面与水反应可生成 。
。
①上图中X的化学式为
②图中反应的总化学方程式为
③
 的还原能力与标准状况下
的还原能力与标准状况下 的还原能力相当(还原能力即生成
的还原能力相当(还原能力即生成 失去电子的量)。
失去电子的量)。
您最近一年使用:0次



