1 . 碘及其化合物在合成杀菌剂、药物等方面具有广泛用途。回答下列问题:
(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为_______ 。
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中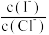 为:
为:_______ ,已知Ksp(AgCl)=1.8×10-10,Ksp(AgI)=8.5×10-17。
(3)已知反应2HI(g) =H2(g) + I2(g)的ΔH= +11kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为_______ kJ。
(4)Bodensteins研究了下列反应:2HI(g)⇌H2(g) + I2(g)
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
①根据上述实验结果,该反应的平衡常数K的计算式为:_______ 。
②上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数,则k逆为_______ (以K和k正表示)。若k正 = 0.0027min-1,在t=40min时,v正=_______ min-1
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为_______ (填字母)

(1)大量的碘富集在海藻中,用水浸取后浓缩,再向浓缩液中加MnO2和H2SO4,即可得到I2,该反应的还原产物为
(2)上述浓缩液中含有I-、Cl-等离子,取一定量的浓缩液,向其中滴加AgNO3溶液,当AgCl开始沉淀时,溶液中
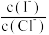 为:
为:(3)已知反应2HI(g) =H2(g) + I2(g)的ΔH= +11kJ·mol-1,1mol H2(g)、1mol I2(g)分子中化学键断裂时分别需要吸收436kJ、151kJ的能量,则1molHI(g)分子中化学键断裂时需吸收的能量为
(4)Bodensteins研究了下列反应:2HI(g)⇌H2(g) + I2(g)
在716K时,气体混合物中碘化氢的物质的量分数x(HI)与反应时间t的关系如下表:
| t/min | 0 | 20 | 40 | 60 | 80 | 120 |
| x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
| x(HI) | 0 | 0.60 | 0.73 | 0.773 | 0.780 | 0.784 |
①根据上述实验结果,该反应的平衡常数K的计算式为:
②上述反应中,正反应速率为v正= k正·x2(HI),逆反应速率为v逆=k逆·x(H2)·x(I2),其中k正、k逆为速率常数,则k逆为
③由上述实验数据计算得到v正~x(HI)和v逆~x(H2)的关系可用下图表示。当升高到某一温度时,反应重新达到平衡,相应的点分别为

您最近一年使用:0次
2019-01-30更新
|
7110次组卷
|
9卷引用:2015年全国普通高等学校招生统一考试化学(新课标I卷)
2 . 氮是一种重要的元素,在很多物质中都含有它的身影。
(1)在9.3胜利日阅兵活动中,我国展示了多款导弹,向世界展示了我们捍卫和平的决心和能力。偏二甲肼(CH3)2NNH2是一种无色易燃的液体,常与N2O4作为常用火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2 (l )+2N2O4 (l)=2CO2 (g)+3N2(g)+4H2O(g)
①该反应(Ⅰ)中氧化剂是_____________ 。
②火箭残骸中常现红棕色气体,原因为:N2O4 (g) 2NO2 (g),一定温度下,该反应的焓变为ΔH。现将2 mol NO2 充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是
2NO2 (g),一定温度下,该反应的焓变为ΔH。现将2 mol NO2 充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是_________ 。
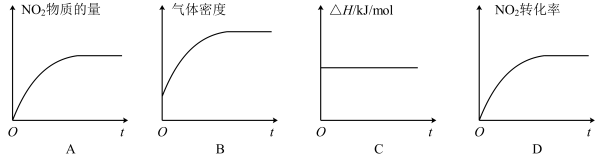
若在相同温度下,将上述反应改在体积为2L的恒容密闭容器中进行,平衡常数____________ (填“增大”“不变”或“减小”),反应4min后N2O4的物质的量为0.8mol,则0~4min内的平均反应速率v(NO2)=_________________ 。
(2)硝酸铵(NH4NO3)是一种重要的铵盐,它的主要用途作肥料及工业用和军用炸药。在25℃时,将1mol 硝酸铵溶于水,溶液显酸性,原因是__________________ (用离子方程式表示)。向该溶液滴加50mL氨水后溶液呈中性,则滴加氨水的过程中的水的电离平衡将__________ (填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为___________ mol·L-1。(NH3·H2O的电离平衡常数Kb=2×10-5 mol·L-1)
(1)在9.3胜利日阅兵活动中,我国展示了多款导弹,向世界展示了我们捍卫和平的决心和能力。偏二甲肼(CH3)2NNH2是一种无色易燃的液体,常与N2O4作为常用火箭推进剂,二者发生如下化学反应:
(CH3)2NNH2 (l )+2N2O4 (l)=2CO2 (g)+3N2(g)+4H2O(g)
①该反应(Ⅰ)中氧化剂是
②火箭残骸中常现红棕色气体,原因为:N2O4 (g)
 2NO2 (g),一定温度下,该反应的焓变为ΔH。现将2 mol NO2 充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是
2NO2 (g),一定温度下,该反应的焓变为ΔH。现将2 mol NO2 充入一恒压密闭容器中,下列示意图正确且能说明反应达到平衡状态的是
若在相同温度下,将上述反应改在体积为2L的恒容密闭容器中进行,平衡常数
(2)硝酸铵(NH4NO3)是一种重要的铵盐,它的主要用途作肥料及工业用和军用炸药。在25℃时,将1mol 硝酸铵溶于水,溶液显酸性,原因是
您最近一年使用:0次
2013·河北石家庄·二模
3 . 世界环保联盟建议全面禁止使用氯气用于饮用水的消毒,而建议采用高效“绿色” 消毒剂二氧化氯。二氧化氯是一种极易爆炸的强氧化性气体,易溶于水、不稳定、呈黄绿色,在生产和使用时必须尽量用稀有气体进行稀释,同时需要避免光照、震动或加热。实验室以电解法制备C1O2的流程如下:
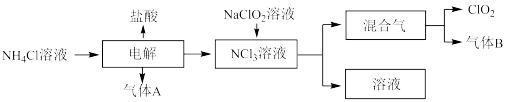
(1)C1O2中所有原子______(填“是”或“不是”)都满足8电子结构。上图所示电解法制得的产物中杂质气体B能使石蕊试液显蓝色,除去杂质气体可选用______
(2)稳定性二氧化氯是为推广二氧化氯而开发的新型产品,下列说法正确的是______(填选项字母)。
(3)欧洲国家主要采用氯酸钠氧化浓盐酸制备,化学方程式为______ 。此法缺点主要是产率低、产品难以分离,还可能污染环境。
(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式为______ 此法相比欧洲方法的优点是______ 。
(5)科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学方程式为______ 。此法提高了生产及储存、运输的安全性,原因是______

(1)C1O2中所有原子______(填“是”或“不是”)都满足8电子结构。上图所示电解法制得的产物中杂质气体B能使石蕊试液显蓝色,除去杂质气体可选用______
| A.饱和食盐水B.碱石灰 C.浓硫酸D.蒸馏水 |
| A.二氧化氯可广泛用于工业和饮用水处理 |
| B.二氧化氯应用在食品工业中能有效地延长食品贮藏期 |
| C.稳定性二氧化氯的出现大大增加了二氧化氯的使用范围 |
| D.在工作区和成品储藏室内,要有通风装置和检测及警报装置 |
(4)我国广泛采用经干燥空气稀释的氯气与固体亚氯酸钠(NaClO2)反应制备,化学方程式为
(5)科学家又研究出了一种新的制备方法,利用硫酸酸化的草酸(H2C2O4)溶液还原氯酸钠,化学方程式为
您最近一年使用:0次
2019-01-30更新
|
1051次组卷
|
6卷引用:2013届河北省石家庄市高中毕业班第二次模拟考试理综化学试卷
(已下线)2013届河北省石家庄市高中毕业班第二次模拟考试理综化学试卷(已下线)2014届湖北省孝感市高三第二次统考理综化学试卷(已下线)2014届江西省金溪一中高三理科综合训练题(三)化学试卷(已下线)2013届江西省临川一中高三最后一次模拟考试理科综合试卷2016届黑龙江省哈尔滨三中高三上第三次检测理综化学试卷2016届河南省三门峡市陕州中学高三下学期尖子生专题训练五化学试卷
4 . [化学-选修2:化学与技术]
双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法,其反应原理和生产流程如图所示:

A.氢化釜 B.过滤器 C.氧化塔 D.萃取塔 E.净化塔 F.工作液再生装置 G.工作液配制装置
生产过程中,把乙基蒽醌溶于有机溶剂配制成工作液,在一定的温度、压力和催化剂作用下进行氢化,再经氧化、萃取、净化等工艺得到双氧水。回答下列问题:
(1)蒽醌法制备双氧水理论上消耗的原料是_______ ,循环使用的|原料是______ ,配制工作液时采用有机溶剂而不采用水的原因是______ 。
(2)氢化釜A中反应的化学方程式为_______ ,进入氧化塔C的反应混合液中的主要溶质为_______ 。
(3)萃取塔D中的萃取剂是____ ,选择其作萃取剂的原因是______ 。
(4)工作液再生装置F中要除净残留的H2O2,原因是______ 。
(5)双氧水浓度可在酸性条件下用KMnO4溶液测定,该反应的离子方程式为_______ 。一种双氧水的质量分数为27.5%,(密度为1.10g·cm3),其浓度为______ mol/L。
双氧水是一种重要的氧化剂、漂白剂和消毒剂。生产双氧水常采用蒽醌法,其反应原理和生产流程如图所示:

A.氢化釜 B.过滤器 C.氧化塔 D.萃取塔 E.净化塔 F.工作液再生装置 G.工作液配制装置
生产过程中,把乙基蒽醌溶于有机溶剂配制成工作液,在一定的温度、压力和催化剂作用下进行氢化,再经氧化、萃取、净化等工艺得到双氧水。回答下列问题:
(1)蒽醌法制备双氧水理论上消耗的原料是
(2)氢化釜A中反应的化学方程式为
(3)萃取塔D中的萃取剂是
(4)工作液再生装置F中要除净残留的H2O2,原因是
(5)双氧水浓度可在酸性条件下用KMnO4溶液测定,该反应的离子方程式为
您最近一年使用:0次
2019-01-30更新
|
2867次组卷
|
5卷引用:2016年全国普通高等学校招生统一考试化学(新课标2卷精编版)
5 . 某科研小组探究工业废Cu粉(杂质含有SiO2、Al2O3、Fe2O3中的一种或几种)的组成并制备少量CuSO4·5H2O,实现废物综合利用,实验过程如下:
过程Ⅰ:
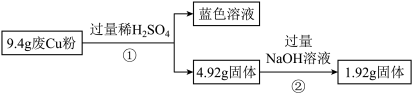
(1)废Cu粉中一定含有的杂质是________ (填化学式)。
(2)写出过程②发生反应的离子方程式:_____________ 。
过程Ⅱ:
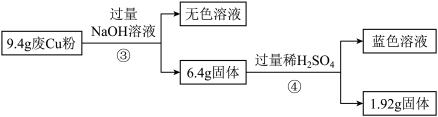
(3)综合过程Ⅰ、Ⅱ,计算废Cu粉中各成分的质量之比是_______ (化为最简整数比)
过程Ⅲ:已知25℃时:
(4)在Ⅱ中所得蓝色溶液中加入一定量的H2O2溶液,调节溶液的pH范围为________ ,然后过滤、结晶,可得CuSO4·5H2O。
(5)下列与 Ⅲ方案 相关的叙述中,正确的是_______ 填字母)。
过程Ⅰ:

(1)废Cu粉中一定含有的杂质是
(2)写出过程②发生反应的离子方程式:
过程Ⅱ:

(3)综合过程Ⅰ、Ⅱ,计算废Cu粉中各成分的质量之比是
过程Ⅲ:已知25℃时:
| 电解质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶度积(Ksp) | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
| 开始沉淀时的pH | 5.4 | 6.5 | 3.5 |
| 完全沉淀时的pH | 6.4 | 9.6 | 4.0 |
(5)下列与 Ⅲ方案 相关的叙述中,正确的是
| A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染 |
| B.将Fe2+ 氧化为Fe3+ 的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤 |
| C.调节溶液pH选择的试剂可以是氢氧化铜或氧化铜 |
| D.在pH>4的溶液中Fe3+一定不能大量存在 |
您最近一年使用:0次
2019-01-30更新
|
173次组卷
|
4卷引用:2015届河北省冀州中学高三上学期期中化学A试卷
名校
6 . 电解精炼铜的阳极泥主要成分为Cu2Te、Ag2Se,工业上从其中回收硒(Se)、碲(Te)的一种工艺流程如下:
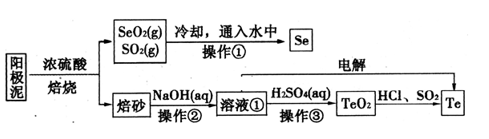
已知:I.TeO2是两性氧化物、微溶于水;
Ⅱ.元素碲在溶液中主要以Te4+、TeO32-、HTeO3-等形式存在;
(1)SeO2与SO2通入水中反应的化学方程式为_____________________________ 操作①的名称为__________ 。
(2)焙砂中碲以TeO2形式存在。溶液①中的溶质主要成分为NaOH、_______ 。工业上通过电解溶液①也可得到单质碲。已知电极均为石墨,则阴极的电极反应式为___________________________ 。
(3)向溶液①中加入硫酸,控制溶液的pH为4.5~5.0,生成TeO2沉淀。如果H2SO4过量,将导致碲的回收率偏低,其原因是_________________________________ 。
(4)将纯净的TeO2先溶于盐酸得到四氯化碲溶液,然后将SO2通入到溶液中得到Te单质。由四氯化碲得到Te单质的离子方程式为__________________ 。

已知:I.TeO2是两性氧化物、微溶于水;
Ⅱ.元素碲在溶液中主要以Te4+、TeO32-、HTeO3-等形式存在;
(1)SeO2与SO2通入水中反应的化学方程式为
(2)焙砂中碲以TeO2形式存在。溶液①中的溶质主要成分为NaOH、
(3)向溶液①中加入硫酸,控制溶液的pH为4.5~5.0,生成TeO2沉淀。如果H2SO4过量,将导致碲的回收率偏低,其原因是

(4)将纯净的TeO2先溶于盐酸得到四氯化碲溶液,然后将SO2通入到溶液中得到Te单质。由四氯化碲得到Te单质的离子方程式为
您最近一年使用:0次
2019-01-22更新
|
1280次组卷
|
3卷引用:【校级联考】甘肃省宁县2019届高三上学期期末联考化学试题
7 . 氯化亚铜(CuCl)是微溶于水但不溶于乙醇的白色粉末,溶于浓盐酸会生成HCuCl2,常用作催化剂。一种由海绵铜(Cu和少量CuO等)为原料制备CuCl的工艺流程如下:
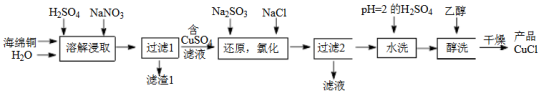
(1)“溶解浸取”时,需将海绵铜粉碎成细颗粒,其目的是___________ 。
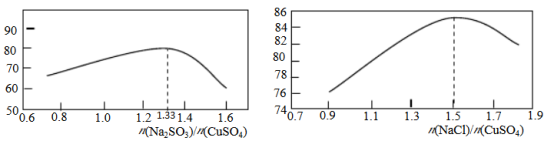
(2)“还原,氯化”时,Na2SO3和NaCl的用量对CuCl产率的影响如图所示:
①CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl的离子方程式为___________ 。
②当n(Na2SO3)/n(CuSO4)>1.33时,比值越大CuCl产率越小,其原因是___________ 。
③当1.0<n(NaCl)/n(CuSO4)<1.5时,比值越大CuCl产率越大,其原因是___________ 。
(3)“粗产品”用pH=2的H2SO4水洗,若不慎用稀硝酸进行稀释,则对产品有何影响___________ 。
(4)用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为Cu2(OH)3Cl。CuCl被氧化为Cu2(OH)3Cl的化学方程式为______________________ 。
(5)某同学拟测定产品中氯化亚铜的质量分数。实验过程如下:准确称取制备的氯化亚铜产品1.600g,将其置于足量的FeCl3溶液中,待样品全部溶解后,加入适量稀硫酸,用0.2000mol·L-1的KMnO4标准溶液滴定到终点,消耗KMnO4溶液15.00mL,反应中MnO4-被还原为Mn2+,则产品中氯化亚铜的质量分数为______________________ 。

(1)“溶解浸取”时,需将海绵铜粉碎成细颗粒,其目的是

(2)“还原,氯化”时,Na2SO3和NaCl的用量对CuCl产率的影响如图所示:
①CuSO4与Na2SO3、NaCl在溶液中反应生成CuCl的离子方程式为
②当n(Na2SO3)/n(CuSO4)>1.33时,比值越大CuCl产率越小,其原因是
③当1.0<n(NaCl)/n(CuSO4)<1.5时,比值越大CuCl产率越大,其原因是
(3)“粗产品”用pH=2的H2SO4水洗,若不慎用稀硝酸进行稀释,则对产品有何影响
(4)用“醇洗”可快速去除滤渣表面的水,防止滤渣被空气氧化为Cu2(OH)3Cl。CuCl被氧化为Cu2(OH)3Cl的化学方程式为
(5)某同学拟测定产品中氯化亚铜的质量分数。实验过程如下:准确称取制备的氯化亚铜产品1.600g,将其置于足量的FeCl3溶液中,待样品全部溶解后,加入适量稀硫酸,用0.2000mol·L-1的KMnO4标准溶液滴定到终点,消耗KMnO4溶液15.00mL,反应中MnO4-被还原为Mn2+,则产品中氯化亚铜的质量分数为
您最近一年使用:0次
8 . 从宏观现象探究微观本质是重要的化学学科素养。
I. 以亚硫酸钠(Na2SO3)为实验对象,探究其性质。实验如下:
【资料1】亚硫酸(H2SO3)易分解生成SO2和H2O。
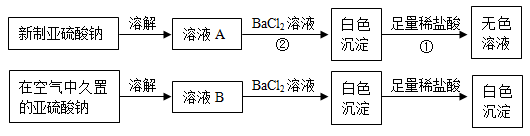
(1)写出上述实验中①、②的离子方程式_________________ ,_________________ 。
(2)通过上述实验可知,在空气中久置的亚硫酸钠固体中会混有_____________ (填化学式),亚硫酸钠在空气中变质体现了亚硫酸钠的_________________ 性。
II. 以FeCl3溶液为实验对象,探究其与碱性物质之间反应的复杂多样性。实验如下:
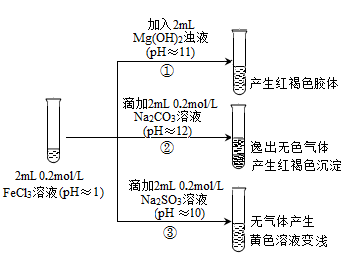
【资料2】含Fe3+的溶液中加入KSCN溶液,溶液由黄色变为红色;
含Fe2+的溶液中加入K3Fe(CN)6溶液,生成蓝色沉淀。
(1)①中反应的离子方程式是_____________________________ 。
(2)②中逸出的无色气体是_______________________________ 。
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
甲组:取③中反应后溶液少许,滴入稀盐酸酸化,再滴加BaCl2溶液,产生白色沉淀。得出结论:FeCl3与Na2SO3发生了氧化还原反应,离子方程式是_______________ 。
乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是_________ 。
(4)由上述实验可知,下列说法正确的是________ (填字母)。
a. 盐与碱反应时,盐和碱都必须可溶于水
b. 盐溶液可能呈中性、碱性、酸性
c. 盐与盐反应时,不一定生成两种新盐
d. 盐与盐反应时,发生的不一定是复分解反应
I. 以亚硫酸钠(Na2SO3)为实验对象,探究其性质。实验如下:
【资料1】亚硫酸(H2SO3)易分解生成SO2和H2O。

(1)写出上述实验中①、②的离子方程式
(2)通过上述实验可知,在空气中久置的亚硫酸钠固体中会混有
II. 以FeCl3溶液为实验对象,探究其与碱性物质之间反应的复杂多样性。实验如下:

【资料2】含Fe3+的溶液中加入KSCN溶液,溶液由黄色变为红色;
含Fe2+的溶液中加入K3Fe(CN)6溶液,生成蓝色沉淀。
(1)①中反应的离子方程式是
(2)②中逸出的无色气体是
(3)对于③中的实验现象,同学们有诸多猜测,继续进行实验:
甲组:取③中反应后溶液少许,滴入稀盐酸酸化,再滴加BaCl2溶液,产生白色沉淀。得出结论:FeCl3与Na2SO3发生了氧化还原反应,离子方程式是
乙组:认为甲组的实验不严谨,重新设计并进行实验,证实了甲组的结论是正确的。其实验方案是
(4)由上述实验可知,下列说法正确的是
a. 盐与碱反应时,盐和碱都必须可溶于水
b. 盐溶液可能呈中性、碱性、酸性
c. 盐与盐反应时,不一定生成两种新盐
d. 盐与盐反应时,发生的不一定是复分解反应
您最近一年使用:0次
名校
解题方法
9 . 聚合硫酸铁可用于水的净化,其化学式可表示为[Fea(OH)b(SO4)c]m。取一定量聚合硫酸铁样品与足量盐酸反应,将所得溶液平均分为两份。向一份溶液中加入足量的BaCl2溶液,得到白色沉淀1.747 5 g。取另一份溶液,先将Fe3+还原为Fe2+(还原剂不是Fe,且加入的还原剂恰好将Fe3+还原为Fe2+),再用0.020 00 mol/LK2Cr2O7标准溶液滴定至终点,消耗K2Cr2O7标准溶液50.00 mL。该聚合硫酸铁样品中a∶b为[已知:K2Cr2O7+6FeSO4+7H2SO4=K2SO4+Cr2(SO4)3+3Fe2(SO4)3+7H2O]( )
| A.1∶1 | B.2∶1 | C.3∶1 | D.2∶5 |
您最近一年使用:0次
2018-12-15更新
|
1547次组卷
|
7卷引用:2016-2017学年江苏省徐州一中高一上期中化学卷
2016-2017学年江苏省徐州一中高一上期中化学卷(已下线)2019高考热点题型和提分秘籍 第二章 化学物质及其变化 第3讲 氧化还原反应 (题型专练)(已下线)2019年1月2日 《每日一题》高考二轮复习-以物质的量为核心的计算【全国百强校】内蒙古鄂尔多斯市第一中学2018-2019学年高二下学期第三次月考化学试题辽宁省铁岭市六校2020-2021学年高二下学期期末联考化学试题辽宁省沈阳市东北育才学校2020届高三上学期第一次模拟考试化学试题苏教2020版化学必修第二册专题9第三单元 金属材料的性能及应用课后习题
名校
10 . 已知反应:2Cu(IO3)2+24KI+12H2SO4=2CuI↓+13I2+12K2SO4+12H2O ,下列说法正确的是
| A.CuI既是氧化产物又是还原产物 |
| B.每转移1.1mol电子,有0.2molIO3-被氧化 |
| C.每生成1molCuI,有12molKI发生氧化反应 |
| D.Cu(IO3)2作氧化剂,Cu(IO3)2中的铜和碘元素被还原 |
您最近一年使用:0次



