名校
解题方法
1 . 从矿物学资料查得,一定条件下自然界中存在反应 。(其中
。(其中 中Fe为+2价S为-1价)下列说法正确的是
中Fe为+2价S为-1价)下列说法正确的是
 。(其中
。(其中 中Fe为+2价S为-1价)下列说法正确的是
中Fe为+2价S为-1价)下列说法正确的是A. 既是氧化产物又是还原产物 既是氧化产物又是还原产物 |
B.参与反应的 与转移电子数之比为1∶2 与转移电子数之比为1∶2 |
C. 只作还原剂 只作还原剂 |
D.产物中的 有一部分是氧化产物 有一部分是氧化产物 |
您最近一年使用:0次
2022-01-13更新
|
2085次组卷
|
4卷引用:湖南省长沙市实验中学2022-2023学年高一上学期第一次月考化学试题
名校
解题方法
2 . X、Y、Z、M为短周期元素,原子序数依次增大。A~J均由该四种元素构成的单质或化合物,其转化关系如图所示,部分生成物省略。
已知:①A、B、C、G都是由两种元素构成的化合物,其中A、G分子所含的电子数为10e-,B、C分子所含的电子数为18e-;D为空气的主要成分之一、
②另取16.8gJ在真空条件下,控制温度350~400oC加热至完全分解,得到F和8.96L(已折算成标准状况)A两种物质。

请回答下列问题:
(1)写出C的化学式是___________ ;D的电子式是___________ 。
(2)请写出金属单质E在生产生活中的一种作用___________ 。
(3)写出次氯酸钠与过量气体A反应生成B的化学方程式是___________ ;B在制备过程中,气体A需要过量的理由是___________ 。
(4)写出F和G反应生成H和A的化学方程式是___________ 。
(5)B在加热条件下与CuO反应可生成气体D和金属单质,请设计实验方案,验证B与CuO反应后固体的成分(不考虑其他反应)___________ 。
(6)写出J在已知②条件下受热分解的化学方程式是___________ 。
已知:①A、B、C、G都是由两种元素构成的化合物,其中A、G分子所含的电子数为10e-,B、C分子所含的电子数为18e-;D为空气的主要成分之一、
②另取16.8gJ在真空条件下,控制温度350~400oC加热至完全分解,得到F和8.96L(已折算成标准状况)A两种物质。

请回答下列问题:
(1)写出C的化学式是
(2)请写出金属单质E在生产生活中的一种作用
(3)写出次氯酸钠与过量气体A反应生成B的化学方程式是
(4)写出F和G反应生成H和A的化学方程式是
(5)B在加热条件下与CuO反应可生成气体D和金属单质,请设计实验方案,验证B与CuO反应后固体的成分(不考虑其他反应)
(6)写出J在已知②条件下受热分解的化学方程式是
您最近一年使用:0次
2021-11-05更新
|
1096次组卷
|
2卷引用:湖北省华中师范大学第一附属中学2022-2023学年高一上学期竞赛生10月测试化学试题
20-21高二下·浙江·阶段练习
3 . 某兴趣小组对化合物X开展实验探究。
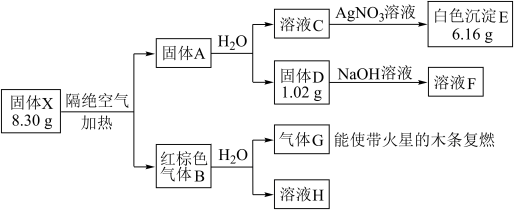
其中:X是易溶于水的强酸盐,由4种元素组成;D、E、G均为纯净物,B为混合物;溶液C、F、H均为单一溶质溶液,溶液H中含溶质0.06 mol,溶液C的焰色反应通过蓝色钴玻璃观察为紫色。
(1)组成X的4种元素是_______________ (填元素符号),E的化学式是______________ 。
(2)固体X隔绝空气加热分解的化学方程式____________________________ 。
(3)写出溶液F与少量溶液H反应的离子方程式____________________________ 。
(4)标况下,将红棕色气体B收集在一个大试管中,再倒插在水槽中,得到溶液的浓度为_______ mol/L (设溶质不扩散,)。
(5)写出红棕色气体B中的化合物气体(在答案中写出化学式)与溴蒸气的鉴别方法:______________ 。

其中:X是易溶于水的强酸盐,由4种元素组成;D、E、G均为纯净物,B为混合物;溶液C、F、H均为单一溶质溶液,溶液H中含溶质0.06 mol,溶液C的焰色反应通过蓝色钴玻璃观察为紫色。
(1)组成X的4种元素是
(2)固体X隔绝空气加热分解的化学方程式
(3)写出溶液F与少量溶液H反应的离子方程式
(4)标况下,将红棕色气体B收集在一个大试管中,再倒插在水槽中,得到溶液的浓度为
(5)写出红棕色气体B中的化合物气体(在答案中写出化学式)与溴蒸气的鉴别方法:
您最近一年使用:0次
名校
4 . 酸性废水中的砷元素主要以亚砷酸(H3AsO3)形式存在。已知As2S3难溶于水,也不溶于稀硫酸、稀盐酸等无机酸。
(1)工业上采用硫化法(通常用Na2S)去除废水中的砷。
①向酸性废水中加入Na2S,产生的H2S与H3ASO3反应生成As2S3的化学方程式为_______ 。
②沉淀后,若废水中c(S2-)=1.0×10-4mol·L-1,则c(As3+)=_______ 。[Ksp(As2S3)=4.0×10-38]。
③为了防止As2S3与过量的S2-形成络合离子而溶解,通常需添加适量的FeSO4溶液,形成FeS,与As2S3共沉淀。验证沉淀中含有FeS的实验方法是_______ 。
(2)用硫代硫酸钠(Na2S2O3)替代Na2S处理含砷酸性废水可避免H2S污染。
①Na2S2O3去除酸性废水中H3AsO3的反应机理如图1所示,S2O 经过“途径I”的除砷过程可描述为
经过“途径I”的除砷过程可描述为________ (图中“HS·”为自由基,“·”表示孤单电子)。
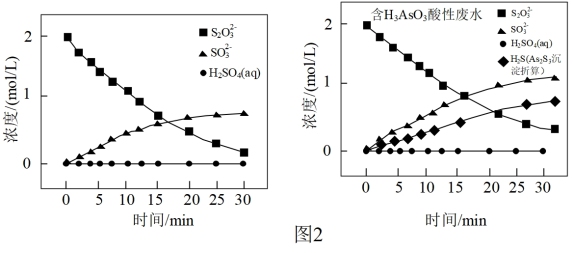
②其他条件相同时,在紫外线照射下,将Na2S2O3分别加入到不含H3AsO3的酸性废水和含H3AsO3的酸性废水中,监测到反应过程中部分物质的浓度变化如图2所示,发现均不释放H2S,其原因是_______ 。
(1)工业上采用硫化法(通常用Na2S)去除废水中的砷。
①向酸性废水中加入Na2S,产生的H2S与H3ASO3反应生成As2S3的化学方程式为
②沉淀后,若废水中c(S2-)=1.0×10-4mol·L-1,则c(As3+)=
③为了防止As2S3与过量的S2-形成络合离子而溶解,通常需添加适量的FeSO4溶液,形成FeS,与As2S3共沉淀。验证沉淀中含有FeS的实验方法是
(2)用硫代硫酸钠(Na2S2O3)替代Na2S处理含砷酸性废水可避免H2S污染。
①Na2S2O3去除酸性废水中H3AsO3的反应机理如图1所示,S2O
 经过“途径I”的除砷过程可描述为
经过“途径I”的除砷过程可描述为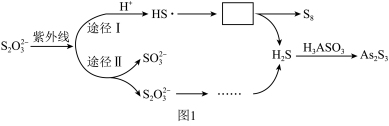
②其他条件相同时,在紫外线照射下,将Na2S2O3分别加入到不含H3AsO3的酸性废水和含H3AsO3的酸性废水中,监测到反应过程中部分物质的浓度变化如图2所示,发现均不释放H2S,其原因是

您最近一年使用:0次
2021-03-27更新
|
1496次组卷
|
2卷引用:湖北省华中师范大学第一附属中学2022-2023学年高一上学期竞赛生10月测试化学试题
19-20高二·浙江·期中
名校
5 . 由一种阳离子与两种酸根离子组成的盐称为混盐,CaOCl2是一种常见的混盐,下列说法不正确的是
| A.CaOCl2有较强的氧化性 |
| B.CaOCl2水溶液呈碱性 |
| C.由氯气为原料,每生成1 mol CaOCl2,转移的电子数为2NA |
| D.CaOCl2的溶液中加入足量浓硫酸,可有黄绿色的气体产生 |
您最近一年使用:0次
名校
解题方法
6 . 常温下,向1L 1.0mol/L的NaClO溶液中缓慢通入SO2气体,使其充分吸收,溶液pH与通入SO2物质的量关系如图所示(忽略溶液体积的变化和NaClO、HClO的分解)。下列说法错误的是
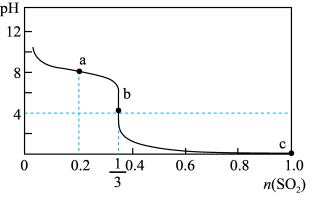

| A.常温下,HClO电离平衡常数的数量级为10﹣8 |
| B.a点溶液中存在 4c(Cl-)=c(HClO)+c(ClO-) |
C.b点溶液中存在c(Na+)>c(SO )>c(Cl-)>c(H+)>c(OH-) )>c(Cl-)>c(H+)>c(OH-) |
| D.c点溶液中c(H+)=2mol/L |
您最近一年使用:0次
2020-11-12更新
|
1729次组卷
|
5卷引用:陕西省汉中市2021-2022学年高二下学期期末联考化学试题
名校
解题方法
7 . 已知还原性:SO >I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )
>I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )
 >I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )
>I-。向含a mol KI和a mol K2SO3的混合液中通入b mol Cl2充分反应(不考虑Cl2与I2之间的反应)。下列说法不正确的是 ( )A.当a=b时,发生的离子反应为SO +Cl2+H2O=SO +Cl2+H2O=SO +2H++2Cl- +2H++2Cl- |
B.当5a=4b时,发生的离子反应为4SO +2I-+5Cl2+4H2O=4SO +2I-+5Cl2+4H2O=4SO +I2+8H++10Cl- +I2+8H++10Cl- |
C.当a≤b≤ a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol a时,反应中转移电子的物质的量n(e-)为a mol≤n(e-)≤3a mol |
D.当a<b< a时,溶液中SO a时,溶液中SO 、I-与Cl-的物质的量之比为a∶(3a-2b)∶2b 、I-与Cl-的物质的量之比为a∶(3a-2b)∶2b |
您最近一年使用:0次
2020-08-18更新
|
3400次组卷
|
7卷引用:福建省泉州市永春第一中学2022-2023学年高一上学期期末考试化学试题
福建省泉州市永春第一中学2022-2023学年高一上学期期末考试化学试题浙江省瑞安市上海新纪元高级中学2019-2020学年高一下学期期末考试化学试题(2)(已下线)解密04 离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)解密04 离子反应(讲义)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练黑龙江省哈尔滨师范大学附属中学2020-2021学年高二下学期期末考试化学试题(已下线)课时06 与量有关的离子方程式书写-2022年高考化学一轮复习小题多维练(全国通用)辽宁省实验中学2021-2022学年高一上学期11月期中阶段测试化学试题
名校
8 . 足量的铜与一定量的浓硝酸充分反应,得到4.48L(标准状况)NO2与NO的混合气体,这些气体与一定体积的O2混合后通入水中,恰好被完全吸收生成硝酸。向所得硝酸铜溶液中加入100mL4mol·L-1NaOH溶液,Cu2+恰好沉淀完全。下列说法正确的是
| A.此反应过程中转移了0.5mol的电子 |
| B.消耗氧气的体积为1.12L(标准状况) |
| C.参加反应的HNO3是0.45mol |
| D.混合气体中含2.24L(标准状况)NO |
您最近一年使用:0次
2020-07-22更新
|
3036次组卷
|
11卷引用:黑龙江省鹤岗市第一中学2021-2022学年高一下学期4月月考化学试题
黑龙江省鹤岗市第一中学2021-2022学年高一下学期4月月考化学试题辽宁省大连市旅顺口区2019-2020学年高一下学期期末考试化学试题辽宁省大连市2019-2020学年高一下学期期末考试化学试题重庆市缙云教育联盟2020-2021学年高一9月月考化学试题山西省实验中学2020-2021学年高一下学期第一次月考化学试题辽宁省大连市一0三中学2020-2021学年高一4月月考化学试题辽宁省部分中学2019-2020高一下学期期末考试化学试题云南省曲靖市第一中学2022-2023学年高一下学期期末考试化学试题安徽省铜陵市第一中学2022-2023 学年高一下学期期中教学质量检测化学试题云南省开远市第一中学校2022-2023学年高一下学期期末考试化学试题重庆市万州第二高级中学2023-2024学年高一下学期3月月考试题 化学试题
名校
9 . 铋(Bi)位于元素周期表中第VA族,其价态为+3时较稳定,铋酸钠(NaBiO3)溶液呈无色。现取一定量的硫酸锰MnSO4溶液,向其中依次滴加下列溶液,对应现象如表所示:
在上述实验条件下,下列结论正确的是
| 加入溶液 | ①适量铋酸钠溶液 | ②过量双氧水 | ③适量KI-淀粉溶液 |
| 实验现象 | 溶液呈紫红色 | 溶液紫红色消失,产生气泡 | 溶液缓慢变成蓝色 |
| A.氧化性强弱顺序为:BiO3->MnO4->H2O2>I2 |
| B.H2O2被高锰酸根离子还原成O2 |
| C.H2O2具有氧化性,把KI氧化成I2 |
| D.KI-淀粉溶液中滴加铋酸钠溶液,溶液不一定变蓝色 |
您最近一年使用:0次
2020-04-30更新
|
1220次组卷
|
3卷引用:河北省秦皇岛市昌黎第一中学2023届高三第六次调研考试化学试题
名校
10 . 工业上用草酸“沉钴”,再过滤草酸钴得到的母液A经分析主要含有下列成分:
为了有效除去母液A中残留的大量草酸,一般用氯气氧化处理草酸,装置如下:

回答下列问题:
(1)母液A中c(Co2+)为____ mol·L-1。 ,
(2)分液漏斗中装入盐酸,写出制取氯气的离子方程式____________ 。反应后期使用调温电炉加热,当锥形瓶中____ (填现象)时停止加热。
(3)三颈烧瓶反应温度为50℃,水浴锅的温度应控制为____ (填序号)。
(4)氯气氧化草酸的化学方程式为________ 。
(5)搅拌器能加快草酸的去除速率,若搅拌速率过快则草酸去除率反而降低,主要原因是__________ 。
(6)若用草酸铵代替草酸“沉钴”,其优点是____ ,其主要缺点为________ 。
| H2C2O4 | Co2+ | Cl- | |
| 质量浓度 | 20.0g/L | 1.18g/L | 2.13g/L |

回答下列问题:
(1)母液A中c(Co2+)为
(2)分液漏斗中装入盐酸,写出制取氯气的离子方程式
(3)三颈烧瓶反应温度为50℃,水浴锅的温度应控制为
A.50℃ B.5l-52℃ C.45 - 55℃ D.60℃
(4)氯气氧化草酸的化学方程式为
(5)搅拌器能加快草酸的去除速率,若搅拌速率过快则草酸去除率反而降低,主要原因是
(6)若用草酸铵代替草酸“沉钴”,其优点是
您最近一年使用:0次
2020-04-12更新
|
874次组卷
|
2卷引用:河南省河南大学附属中学2022届高三最后一卷化学试题



